实验室获取氮气有很多种途径,常见的3种方法是:
方法一:将氨气通入灼热的氧化铜粉末,得到纯净的氮气和铜;
方法二:将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
方法三:将亚硝酸钠(NaNO
2)和氯化铵的混合溶液加热,氮元素全部转化为氮气.
进行实验时可选择的实验仪器如下图所示(省略夹持装置与加热装置):
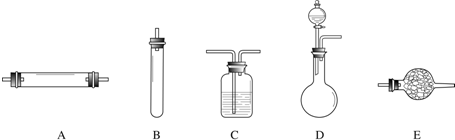
(1)方法一:制氮气所需的氨气可以用浓氨水滴加到生石灰中得到,此反应的发生装置最好选用
D
D
(选填装置编号).请写出生石灰在此反应中的两个作用:
生石灰和水反应放热,促使氨水挥发、分解而得到氨气(或降低氨气的溶解度)
生石灰和水反应放热,促使氨水挥发、分解而得到氨气(或降低氨气的溶解度)
,
生石灰与水反应,减少了溶剂
生石灰与水反应,减少了溶剂
.
(2)方法二:为保证所得氮气尽可能纯净,除了使用铜外,还可以向装置
E
E
(选填装置编号)中加入
碱石灰
碱石灰
以除去其它杂质气体.
(3)方法三:制氮气的化学方程式为:
.
(4)绿色化学是指在制造和应用化学产品时应有效利用(最好可再生)原料,消除废物和避免使用有毒的和危险的试剂与溶剂.在制取氮气的3种方法中,联合使用方法一和方法二与单独使用方法三相比,具有很多优越性,请从绿色化学的角度进行评价:
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
铜和氧化铜可循环使用,节省试剂(或避免使用有毒物质而造成污染)
.
(5)1892年,英国科学家瑞利(Rayleigh)发现,采用方法二得到的氮气在相同条件下比方法三得到的氮气密度总是偏大5‰左右.若上述实验设计与操作均无错误,且氮气已完全干燥,请解释产生这一现象的原因:
方法二制得的氮气中含有密度(或相对分子质量)比氮气大的稀有气体,导致密度偏大
方法二制得的氮气中含有密度(或相对分子质量)比氮气大的稀有气体,导致密度偏大
.

 亚硝酸钠(NaNO2)是一种常用的防腐剂.请回答:
亚硝酸钠(NaNO2)是一种常用的防腐剂.请回答:


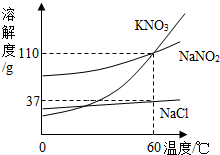 (2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.
(2013?历下区二模)亚硝酸钠(NaNO2)常用作食品的发色剂和防腐剂,但食品中的亚硝酸钠含量超标会危害人体健康.亚硝酸钠具有咸味,外形和食盐很相似,亚硝酸钠的水溶液呈碱性.建筑行业常用亚硝酸钠作水泥添加剂,近年来,在建筑工地多次发生误将亚硝酸钠当作食盐食用导致中毒的事件.