
化学是一门以实验为基础的科学。
(1)根据如图所示实验,回答以下问题。

①A为测定空气中氧气含量的实验装置,有关反应的化学方程式为 ;通过该实验可得出氧气约占空气总体积的 的结论。
②集气瓶B中的现象:铁丝在氧气中剧烈燃烧, ,放出大量的热,有黑色固体生成,该反应的化学方程式为 。
③取一朵用石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入集气瓶C中,观察到的现象是 。
(2)某实验小组模拟高炉炼铁的化学反应原理实验,其装置如图所示。

①A处的现象是 ;发生反应的化学方程式为 。
②C处酒精灯的作用是 。
科目:初中化学 来源:山东省淄博市桓台县2017届九年级中考一模化学试卷 题型:选择填充题
科学合理的分析和判断是解决化学问题的重要依据。下列分析不正确的是
A. 物质燃烧后的残余物质量都是减少的
B. 向20℃的饱和硝酸钾溶液中再加入硝酸钾固体,溶液质量不变
C. 向稀盐酸中加入一定量铝粉,完全反应后溶液质量增加
D. 把硝酸铵和某物质研磨后产生刺鼻的氨气,可判断该物质一定是碱性的
查看答案和解析>>
科目:初中化学 来源:江苏省兴化市顾庄学区三校2017届九年级第三次网上阅卷适应性训练(三模)化学试卷 题型:选择填充题
生活中的许多变化涉及化学知识,下列过程没有涉及化学变化的是
A. 鸡蛋煮熟 B. 光合作用 C. 石油分馏 D. 食物腐败
查看答案和解析>>
科目:初中化学 来源:辽宁省营口市2017届九年级中考模拟化学试卷 题型:选择填充题
葡萄糖(C6H12O6)是一种重要营养物质,下列关于葡萄糖的说法中,正确的是( )
A. 葡萄糖由6种碳元素、12种氢元素和6种氧元素组成
B. 葡萄糖由6个碳原子、12个氢原子和6个氧原子构成
C. 每个葡萄糖分子中所含原子个数为24
D. 每个葡萄糖分子中碳、氢、氧元素质量比为1:2:1
查看答案和解析>>
科目:初中化学 来源:辽宁省营口市2017届九年级中考模拟化学试卷 题型:选择填充题
下列物质中,属于混合物的是( )
A. 矿泉水 B. 冰水混合物 C. 高锰酸钾 D. 氢氧化钙
查看答案和解析>>
科目:初中化学 来源:辽宁省营口市2017届九年级中考模拟化学试卷 题型:信息分析题
生活中处处有化学。
(1)市场上销售的食盐种类有加钙盐、加锌盐、加碘盐等,这里的“钙”、“锌”、“碘”是指 (填“分子”、“原子”、“离子”或“元素”)。
所谓“加碘盐”是指在一定量的食盐中加入一定量的碘酸钾(化学式为KIO3),则
碘酸钾中碘元素的化合价为 。
(2)煤、石油和_________常被称为化石燃料,大量燃煤(含杂质硫、氮等)造成的主要环境问题有 (答出一点即可)。
(3)氢化钙(CaH2)固体可用于登山队员的能源提供剂,它和水反应生成氢氧化钙和氢气。则该反应的化学方程式为
查看答案和解析>>
科目:初中化学 来源:辽宁省营口市2017届九年级中考模拟化学试卷 题型:选择题
某河水中的物质R在氧气的作用下发生反应,其反应的化学方程式为2R+2H2O+7O2 = 2FeSO4+2H2SO4,则R的化学式是
A.FeS B.FeS2 C.FeO D.Fe2S3
查看答案和解析>>
科目:初中化学 来源:广西省柳州市柳南区2017届九年级中考三模化学试卷 题型:信息分析题
化学与我们的生活有着密切的联系。请在下列物质中,作出正确选择,并用序号填空。
①醋酸 ②甲烷 ③稀盐酸 ④石墨 ⑤干冰 ⑥氮气
(1)可用于生产铅笔芯的是_____;(2)一种家庭常用调味品中含有的成份_____;
(3)空气中含量最多的气体_____;(4)可用于金属除锈的是_____;
(5)可用于人工降雨的是_____;(6)天然气的主要成分是_____。
查看答案和解析>>
科目:初中化学 来源:江苏省镇江市润州区2017届九年级中考二模化学试卷 题型:信息分析题
钙及其化合物在生产、生活中具有广泛的应用。
(一)钙的广泛用途
(1)高钙奶中含钙,这里的钙是指_____。(选填序号,下同)
a.单质 b.元素 c.原子
(2人体中钙元素主要存在于骨骼和牙齿中,以羟基磷酸钙[Ca10(PO4)6(OH)2]形式存在,其中磷元素化合价为___________。
(3)混凝土中也含有一定量的含钙物质,钢筋与混凝土混合形成钢筋混凝土,以上叙述中不涉及的材料是____。
a.无机材料 b.合成材料 c.复合材料
(二)轻质CaCO3的制备
某实验小组利用石灰石残渣(杂质不溶于水也不溶于酸)制备轻质CaCO3,同时得到K2SO4,流程如下:
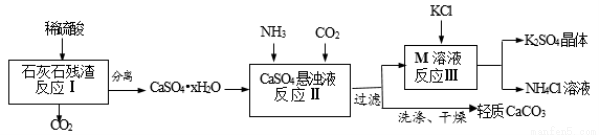
(1)反应Ⅱ中先通NH3,再通CO2的目的是_______,化学方程式为______。
(2)反应Ⅲ中相关物质的溶解度如下表。你认为反应Ⅲ在常温下能实现的原因是______。
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(3)判断CaCO3固体已洗涤干净的方法是____________________;
K2SO4晶体洗涤时,不可选用下列________洗涤剂(填字母编号)。
A.热水 B.冰水 C.饱和K2SO4溶液
(三)CaSO4•xH2O成分测定
上述流程中分离所得的CaSO4•xH2O中含有一定量的CaCO3。实验小组为了测定CaSO4•xH2O中x的值及含量,取22.20g样品加热至900℃,将得到的气体先通过浓硫酸,再通入碱石灰,测得实验数据如下表:
名称 | 浓硫酸 | 碱石灰 |
实验前 | 100.00 | 100.00 |
实验后 | 103.60 | 102.20 |
【资料】已知CaSO4•xH2O在160℃生成CaSO4, CaCO3在900℃时分解完全。
(1)CaSO4•xH2O的质量为_____。
(2)x的值___________。
(四)CaSO4•xH2O的性质探究
CaSO4•xH2O受热会逐步失去结晶水,1350℃时 CaSO4开始分解;取纯净CaSO4•xH2O固体3.44g,加热,测定固体质量随温度的变化情况如下图所示。

(1)0~T1固体质量没有发生变化的原因可能是_____________。
(2)G点固体的化学式是_________。
(3)将T2~1400℃温度段加热固体所产生的气体通入酸性KMnO4溶液中,溶液褪色,反应后的固体为氧化物,则则H~I段发生反应的化学方程式为__________;m=______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com