
科目: 来源: 题型:多选题
| A. | 若a+b=3,则滤液中一定不含AgNO3 | |
| B. | 若a+b=4,则滤纸上一定有Ag和Cu,滤液中一定含有Zn(NO3)2和Cu(NO3)2 | |
| C. | 若溶液呈蓝色,则a=1 | |
| D. | 若向固体中滴加稀盐酸,有气泡产生,则a+b=4 |
查看答案和解析>>
科目: 来源: 题型:多选题
 如图为某固体饱和溶液的浓度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度.当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断错误的是( )
如图为某固体饱和溶液的浓度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度.当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断错误的是( )| A. | 保持温度不变,蒸发溶剂时,先是M点不动,N点向左平移至曲线;继续蒸发溶剂,M、N点都不动 | |
| B. | 都升温10℃后,M、N点均向右平移 | |
| C. | 都降温10℃后,M点沿曲线向左下移,N点向左平移 | |
| D. | 保持温度不变,加水稀释时,M、N点均向下移动 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 16% | B. | 10% | C. | 9.2% | D. | 6.5% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 16克 | B. | 9克 | C. | 36克 | D. | 18克 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将氢氧化钠固体放在滤纸上称量 | |
| B. | 用10mL量筒量取8.58mL蒸馏水 | |
| C. | 氯化钠、硝酸银、碳酸钠三种无色溶液可以用稀盐酸来鉴别 | |
| D. | 制取氧气时,用二氧化锰与过氧化氢溶液在常温下反应,并用向下排空气法收集 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氧化物 | B. | 酸 | C. | 碱 | D. | 盐 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
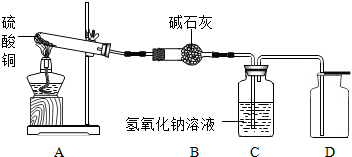
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 42.0克 | 75.0克 | 140.0克 |
| 反应后 | 37.0克 | 79.5克 | 140.0克 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com