
科目: 来源:2020年5月湖北省武汉市部分学校中考(5月调研)模拟化学试卷 题型:单选题
下列选项中,仅利用选项中提供的实验仪器( 规格和数量不限,药品试剂省略)能够完成相应实验的是( )
选项 | 实验仪器 | 相应实验 |
A | 铁架台、大试管、水槽、集气瓶、玻璃片 | 用高锰酸钾固体制取氧气 |
B | 托盘天平、烧杯、玻璃棒、药匙、量筒、胶头滴管 | 用氯化钠固体配制20.0g质量分数为 6.0%的氯化钠溶液 |
C | 集气瓶、橡胶塞、烧杯、弹簧夹 | 用红磷测定空气里氧气的含量 |
D | 锥形瓶、长颈漏斗、集气瓶、导气管、单孔橡胶塞 | 用锌粒与稀硫酸制取氢气 |
A.A B.B C.C D.D
查看答案和解析>>
科目: 来源:2020年5月湖北省武汉市部分学校中考(5月调研)模拟化学试卷 题型:单选题
有一包固体粉末X,可能含有碳酸钙、硫酸铜、硫酸亚铁、锌粉,为确定固体粉末的成分,现取X进行下列实验,实验过程及现象如下图所示(不考虑水、稀盐酸的挥发),下列说法中正确的是( )

A.若气体1为纯净物,则溶液2中可能含有三种阳离子
B.若气体1为混合物,则溶液2中可能含有Fe2+
C.若溶液1呈无色,则固体粉末X中不可能含有硫酸铜
D.若溶液2呈浅绿色,则沉淀2不可能是纯净物
查看答案和解析>>
科目: 来源:2020年5月湖北省武汉市部分学校中考(5月调研)模拟化学试卷 题型:实验题
为了证明人呼出的气体中CO2含量大于空气中CO2含量,小明设计了下图所示装置。

(1)乙装置中球形干燥管的作用是_____。
(2)经多次呼吸操作后,能说明人呼出的气体中 CO2含量大于空气中CO2含量的实验现象是_______________________________________。
(3)装置中产生上述实验现象的原因是_________( 用化学方程式表示)。
查看答案和解析>>
科目: 来源:2020年5月湖北省武汉市部分学校中考(5月调研)模拟化学试卷 题型:填空题
下图为固体物质X的饱和溶液温度与其质量分数的变化曲线。
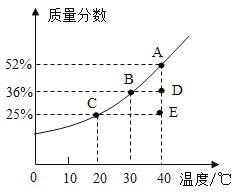
请回答下列问题:
(1)若将E点的溶液降温至30℃,所得溶液为___________(填“ 饱和” 或“ 不饱和”)溶液。
(2) 若将D点的溶液恒温蒸发溶剂时,D点将向_____点移动(选填A∽E) 。
(3)若将50gA点的溶液降温至20℃,则溶液中析出X的质量为_________。
(4) 30℃时,若要使mg质量分数为30%的X溶液变为36%,采用的方法可以是_____ (填序号) 。
a蒸发掉m/6g水
b蒸发掉原溶液中溶剂质量的1/2
c再溶解0.005mg的X粉末
d加入1.2mg40%的X溶液
查看答案和解析>>
科目: 来源:2020年5月湖北省武汉市部分学校中考(5月调研)模拟化学试卷 题型:实验题
氯酸钾有多种用途,常作氧化剂、火箭推进剂等,它易溶于水,在加热时可缓慢释放氧气,但在氧化铜等催化作用下加热会快速放出氧气。小华利用氯酸钾制取氧气来验证氧化铜的催化作用,并探究反应后剩余固体的成分。
(查阅资料)①氯化钾、氧化铜加热不分解;
②硫酸铜易溶于水,溶解度随温度的升高而增大;
③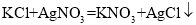
I.催化剂的制备

(1)步骤1的目的是除去不溶性杂质,步骤1所用到的玻璃仪器有_____。
(2)步骤2的目的是得到CuSO4.5H2O晶体,实验操作是_____、降温结晶、过滤、洗涤、干燥。
Ⅱ.加热氯酸钾制取氧气并探究剩余固体的成分
小华设计了以下两组实验,在相同条件下加热,并记录产生VL氧气所需要的时间,实验发现t1>t2,说明氧化铜可以加快氯酸钾的分解,相关数据如下表。
实验编号 | 反应前氯酸钾的质量 | 加入氧化铜的质量 | 生成VL 氧气所用的时间 | 反应后剩余固体的质量 |
ⅰ | 24.5g | 0 | t1 | m |
ⅱ | 24.5g | 2.0g | t2 | 21.7g |
(1)实验ⅰ中反应后剩余固体的质量m=_____。
(2)探究实验ⅱ反应后剩余固体的成分和氧化铜的催化作用,部分数据如下表。
实验步骤 | 现象或结论 |
①将反应后剩余固体继续加热,直至冷却后连续两次称量固体的质量保持不变。 | 若有气体生成,则说明含有氯酸钾,该反应的化学方程式为_____。 |
②将①加热后剩余固体在足量水中充分溶解,过滤、洗涤、干燥、称量 | 若滤渣的质量为_____,可进一步说明氧化铜对氯酸钾分解有催化作用。 |
③收集、合并②的滤液和洗涤液,加入过量硝酸银溶液,充分反应后过滤、洗涤、干燥、称量 | 理论上可得到沉淀的质量为_____。 |
查看答案和解析>>
科目: 来源:2020年5月湖北省武汉市部分学校中考(5月调研)模拟化学试卷 题型:推断题
下图所示转化关系涉及的物质均为初中化学常见的物质。 其中人体胃液中含有甲,乙为赤铁矿的主要成分,丙为绿色植物光合作用的原料,己在常温下为气体。 这些物质之间的反应与转化关系如图所示( “ →” 表示某一物质通过一步能转化为另一物质,“—” 表示连接的两物质之间能反应,部分反应物、生成物及反应条件已略去)。

请回答下列问题:
(1)丁的名称为_____。
(2) 丁与戊反应时可观察到的实验现象是_____。
(3)写出甲与乙反应的化学方程式_____。
(4)下列关于丙与己的说法正确的是_____( 填序号)。
①己可能是单质
②己可能是氧化物
③丙→己的反应可能是分解反应
④丙→己的反应可能是化合反应
⑤丙→己的反应可能是吸热反应
⑥丙→己的反应可能是放热反应
查看答案和解析>>
科目: 来源:2020年5月湖北省武汉市部分学校中考(5月调研)模拟化学试卷 题型:填空题
工业废水会对水体产生严重污染。 某工厂利用中和法处理含硫酸的工业废水和含氢氧化钠的工业废水( 已知两种工业废水的密度均为1.05g.L-1,所含溶质的质量分数均为 5%)。废水处理示意图如下:
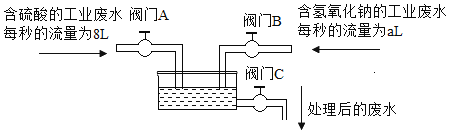
请回答下列问题:
(1)若a=8则紫色石蕊试液遇到处理后的废水呈________________色。
(2) 室温下,若要使处理后的废水pH=7,试计算a的值( 结果保留两位小数)________。
查看答案和解析>>
科目: 来源:2020年湖北省武汉市中考模拟化学试卷 题型:单选题
垃圾是放错了位置的资源,应该分类回收,生活中废弃的铁锅、铝制易拉罐、铜导线等可以归为一类加以回收,它们属于( )
A.氧化物 B.化合物 C.金属或合金 D.非金属
查看答案和解析>>
科目: 来源:2020年湖北省武汉市中考模拟化学试卷 题型:单选题
下列物质的用途中,利用其物理性质的是
A.氧气用于炼钢 B.浓硫酸做干燥剂
C.铁粉用作食品保鲜吸氧剂 D.氮气用作保护气
查看答案和解析>>
科目: 来源:2020年湖北省武汉市中考模拟化学试卷 题型:单选题
青蒿素的化学式为C15H22O5。下列关于青蒿素的说法正确的是( )
A.每个青蒿素由42个原子构成 B.一个青蒿素分子中有11个氢分子
C.青蒿素属于氧化物 D.青蒿素中碳元素的质量分数最大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com