
利用反应2NO(g)+2CO(g) 2CO2(g)+N2(g) ∆H<0 可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
2CO2(g)+N2(g) ∆H<0 可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
A.降低温度 B.增大压强
C.充入N2 D.及时将CO2和N2从反应体系中移走
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河北省高一12月月考化学卷(解析版) 题型:选择题
某物质灼烧时,焰色反应为黄色,下列判断正确的是
A.该物质一定是钠的化合物 B.该物质一定含钠元素
C.该物质一定是金属钠 D.该物质中不可能含有钾元素
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市部分区高一上学期期末化学试卷(解析版) 题型:选择题
在硫酸铁溶液中,加入ag铜完全溶解后再加入bg铁,充分反应后得到cg残余固体,且a>c,则下列说法中正确的是
A.残余固体可能为铁和铜的混合物
B.最后得到的溶液可能含有Fe3+
C.残余固体是铁,溶液中一定不含Cu2+
D.残余固体全部是铜
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市部分区高二上学期期末化学试卷(解析版) 题型:填空题
根据要求回答下列有关问题。
(1)高炉炼铁是冶炼铁的主要方法,发生的主要反应为:
Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ∆H=-28.5kJ/mol
2Fe(s)+3CO2(g) ∆H=-28.5kJ/mol
冶炼铁反应的平衡常数表达式K=____________,
温度升高后,K 值________(填“增大”、“不变”或“减小”)。
(2)己知:①Fe2O3(s)+3C(石墨) 2Fe(s)+3CO(g) ∆H1=+489.0kJ/mol
②Fe2O3(s)+3CO(g) 2Fe(s)+3
2Fe(s)+3 CO2(g) ∆H2=-28.5kJ/mol
CO2(g) ∆H2=-28.5kJ/mol
③C(石墨)+ CO2(g)=2CO(g) ∆H3=akJ/mol
则a=__________kJ/mol。
(3)在T℃时,反应Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知
2Fe(s)+3CO2(g)的平衡常数K=64,在2L恒容密闭容器中,按下表所示加入物质,经过一段时间后达到平衡。(已知 =4)
=4)
Fe2O3 | CO | Fe | CO2 | |
始态mol | 1.0 | 1.0 | 1.0 | 1.0 |
①平衡时CO 的转化率为___________。
②下列情况标志反应达到平衡状态正确的 是________(填字母)。
是________(填字母)。
a.容器内气体密度保持不变
b.容器内气体压强保持不变
c.CO的消耗速率和CO2的生成速率相等
(4)一定条件下发生反应:N2(g)+ 3H2(g) 2NH3(g)∆H<0。
2NH3(g)∆H<0。
① 在某温度时,向容积固定的容器中加入1mol N2和3mol H2,达到平衡后:
a.若向容器中通入N2,则N2的转化率将___________(填“增大”、“减小”或“不变”,下同)。
b.若再通入1mol N2和3mol H2,氮气的转化率将________。
②三个相同的容器中各充入1molN2和3molH2,在不同条件下分别达到平衡,氨气的体积分数随时间变化如图,下列说法正确的是___________。
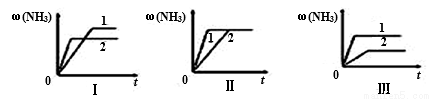
a.图Ⅰ可能是不同温度对反应的影响,且T1>T2
b.图Ⅱ可能是同温同压下有无催化剂, 1表示没加入催化剂, 2表示加入了催化剂
c.图Ⅲ可能是不同压强对反应的影响,且p1>p2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市部分区高二上学期期末化学试卷(解析版) 题型:选择题
反应mA(s)+ nB(g) eC(g)+ fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是
eC(g)+ fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是

A.达到平衡后,加入催化剂则C%增大
B.达到平衡后,增加A的量有利于平衡向正向移动
C.化学方程式中n>e+f
D.达到平衡后,若升温,平衡正向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市部分区高二上学期期末化学试卷(解析版) 题型:选择题
为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂过滤后,再加入适量的盐酸,这种试剂是
A.NH3·H2O B.NaOH C.Na2CO3 D.MgCO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高一上学期期末化学试卷(解析版) 题型:推断题
有一瓶无色澄清溶液,其中可能含有H+、K+、Ba2+ 、Al3+、Cl-、SO42-、CO32-、MnO4-离子。现进行以下实验:
①用pH试纸检验溶液,发现溶液呈强酸性;
②取部分溶液逐滴加入NaOH溶液,使溶液由酸性变为碱性,始终无沉淀产生;
③取少量②中的碱性溶液,滴加Na2CO3溶液,有白色沉淀产生。
(1)根据上述事实确定:该溶液中肯定存在的离子有 ;肯定不存在的离子有 。
(2)写出③中发生反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省资阳市高一上学期期末化学试卷(解析版) 题型:选择题
若一氧化碳和二氧化碳的混合气体的密度与同温同压下氧气的密度相同,混合气体中一氧化碳和二氧化碳的物质的量之比是
A.1∶3 B.3∶1 C.2∶1 D.1∶2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高一上学期期末化学试卷(解析版) 题型:填空题
氧化铜矿石含有CuO和难溶于水的Cu2(OH) 2CO3,还含有Fe2O3、FeO和SiO2等。铜、铁是畜禽所必需的微量元素。某厂生产硫酸铜和硫酸亚铁流程如下:
(1)氧化铜矿石粉碎的目的是 ,KMnO4的作用是将Fe2+氧化成Fe3+。
(2)写出“酸浸”中Cu2(OH) 2CO3发生反应的离子方程式 。
(3)“中和/过滤”中加入CaCO3的目的是 ,使Fe3+ 水解成沉淀而除去。
(4)流程中多处涉及“过滤”,实验室中过滤需要使用的玻璃仪器有烧杯、 。
(5)加入铁屑的作用是使母液中Fe3+转化为Fe2+、 。
(6)下表为硫酸铜晶体“烘干粉碎”的试验结果。

表中m为CuSO4·5H2O晶体的质量,x为干燥后所得晶体中结晶水个数。据此可确定由CuSO4·5H2O脱水得流程所示产品的适宜工艺条件为 (指出条件的温度和时间)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com