
��±�顱����Ҫ�ɷ�ΪMgCl2(��Fe2+��Fe3+��Mn2+����������)��������Ϊԭ�ϣ������¹�������ͼ�������Ƶ���������þ�����Ҫ���Ʒ���������������ӣ����ҳɱ��ϵͣ������������Լ���pH���ƿɲ����±�ȷ����
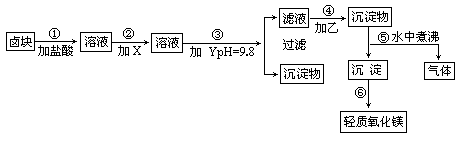
����ע��
����Fe2+�����������״�����״���Һ��ȥ�����Գ�����������ΪFe3+����Fe(OH)3��������ȥ��
����д���¿հף�
(1)�ڲ���ڼ�����Լ�X�����ѡ��Ӧ________����������________��
(2)�ڲ���ۼ�����Լ�Y��Ӧ��________֮����Ҫ����pH��9.8����Ŀ����________��
(3)�ڲ����ʱ�����Ļ�ѧ����ʽ��________��
|
�����𰸣�(1)NaClO����Fe2+����Fe3+ ����(2)Na2CO3,�����е����ʽ������Ӷ�����������������ȥ�� ����(3)MgCO3��H2O ����[����]������1���ݺ����ԣ�����۵�����pH��9.8����Ϊ�˽����е����ʽ������Ӷ�����������������ȥ�����ܴ�ʱMg2+Ҳ���ܲ�������Mg(OH)2�������Ӷ�Ӱ����ʣ�����Ϊ±��۸���ˣ���ʧһЩ�����Ա�֤��Ʒ(MgO)�Ĵ��ȣ����ǿ��еļ���·�ߣ��ٻ�ͷ��������ɱ�1עFe(OH)2������ʵ�ʲ����в��׳�������Fe(OH)3ȴ���׳�����ȫ(pH��3.7)�����Լ����Լ�XӦ����һ�����������ɱ�2������ѡ�ü�����ƯҺ��Ϊ���ʣ��䷴ӦʽΪ��2Fe2+��ClO����2H+ |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��±�顱����Ҫ�ɷ�ΪMgCl2����Fe2+��Fe3+��Mn2+���������ӣ���������Ϊԭ�ϣ������¹�������ͼ�������Ƶá���������þ�������Ҫ���Ʒ���������������ӣ����ҳɱ��ϵͣ������������Լ���PHֵ���ƿɲο����и���ȷ��
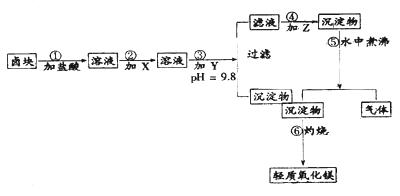
��������þ������������ͼ
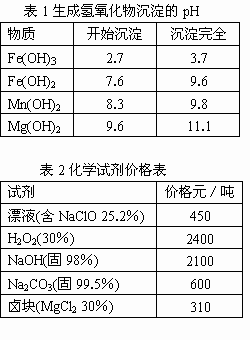
��1 �����������������PHֵ
| ���� | ��ʼ���� | ������ȫ |
| Fe��OH��3 Fe��OH��2 Mn��OH��2 Mg��OH��2 | 2��7 7��6 8��3 9��6 | 3��7 9��6 9��8 11��1 |
*��ע��Fe2+�����������״�����״���Һ�г�ȥ�����Գ�������������ΪFe3+������
Fe��OH��3������ȥ��֮��
��2 ��ѧ�Լ���ֵ��
| �Լ� | �۸�Ԫ/t�� |
| ƯҺ����NaClO25.2%�� H2O2��30%�� NaOH����98%�� Na2CO3����99.5%�� ±�飨MgCl2��30%�� | 450 2400 2100 600 310 |
����д���¿հף�
��1���ڲ���ڼ�����Լ�X�����ѡ��Ӧ�� ���������� ��
��2������ۼ�����Լ�YӦ�� ��֮����Ҫ����pH=9.8����Ŀ���� ��
��3���ڲ����ʱ�����Ļ�ѧ��Ӧ����ʽ�ǣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�긣��ʡ����һ�и߶���ѧ�ڵ�һѧ�ο��Ի�ѧ�Ծ����������� ���ͣ������
��±�顱����Ҫ�ɷ�ΪMgCl2����Fe2+��Fe3+��Mn2+���������ӣ���������Ϊԭ�ϣ������¹�������ͼ�������Ƶá���������þ�������Ҫ���Ʒ���������������ӣ����ҳɱ��ϵͣ������������Լ���pHֵ���ƿɲο����и���ȷ������������þ��������ͼ���£�

��1�� ��ѧ�Լ��۸������������
| �Լ� | �۸�Ԫ/ t �� |
| ƯҺ����NaClO25.2%�� H2O2��30%�� NaOH����98%�� Na2CO3����99.5%�� ±�飨MgCl2��30%�� | 450 2400 2100 600 310 |
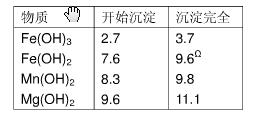 ������������������
������������������| ���� | ��ʼ���� | ������ȫ |
| Fe(OH)3 Fe(OH)2 Mn(OH)2 Mg(OH)2 | 2.7 7.6 8.3 9. 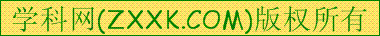 6 6 | 3.7 9.6�� 9.8 11.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�����ʡ��У������һ���������ۻ�ѧ�Ծ��������棩 ���ͣ������
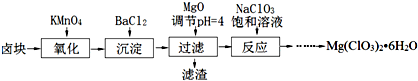
����þ[Mg(ClO3)2]����������������ݼ��ȣ�ʵ�����Ʊ�����Mg(ClO3)2��6H2O���������£�

��֪����±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
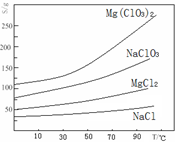
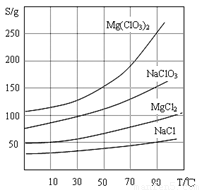
�����ֻ�������ܽ��(S)���¶�(T)�仯������ͼ��ʾ��
��1����������Ҫ����Ҫ���������� ��
��2������BaCl2��Ŀ���� ����MgO�����������������Ҫ�ɷ�Ϊ ��
��3������NaClO3������Һ������Ӧ�Ļ�ѧ����ʽΪ ���ٽ�һ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ���������ᾧ���� ���� ���ܹ��ˡ�ϴ�ӡ�
��4����Ʒ��Mg(ClO3)2��6H2O�����IJⶨ��
����1��ȷ����3.50 g��Ʒ���100 mL��Һ��
����2��ȡ10.00 mL����ƿ�У�����10.00 mLϡ�����20 .00mL 1.000 mol��L��1��FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100 mol��L��1 K2Cr2O7 ��Һ�ζ�ʣ���Fe2�����յ㣬�˹����з�Ӧ�����ӷ���ʽΪ��Cr2O72����6Fe2����14H����2Cr3����6Fe3����7H2O��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7 ��Һ15.00 mL��
��д������2�з�����Ӧ�����ӷ���ʽ�� ��
�ڲ�Ʒ��Mg(ClO3)2��6H2O����������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�����и�����ǰģ�⻯ѧ�Ծ��������棩 ���ͣ�ʵ����
����þ[Mg(ClO3)2]����������������ݼ��ȣ�ʵ�����Ʊ�����Mg(ClO3)2��6H2O���������£�
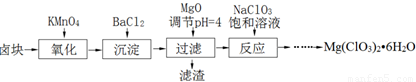
��֪����±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
�����ֻ�������ܽ��(S)���¶�(T)�仯������ͼ��ʾ��
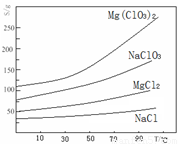
��1����������Ҫ����Ҫ���������� ����MgO�����������������Ҫ�ɷ�Ϊ ��
��2������BaCl2��Ŀ���dz�ȥSO42������μ���SO42���ѳ�����ȫ���� ��
��3������NaClO3������Һ������ӦΪ��MgCl2��2NaClO3��Mg(ClO3)2��2NaCl���ٽ�һ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ���� ���� ���� ���ܹ��ˡ�ϴ�ӡ�
��4����Ʒ��Mg(ClO3)2��6H2O�����IJⶨ��
����1��ȷ����3.50 g��Ʒ���100 mL��Һ��
����2��ȡ10 mL����ƿ�У�����10 mLϡ�����20 mL 1.000 mol��L��1��
FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100 mol��L��1 K2Cr2O7 ��Һ�ζ����յ㣬�˹����з�Ӧ�����ӷ���ʽΪ��Cr2O72����6Fe2����14H����2Cr3����6Fe3����7H2O��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7 ��Һ15.00 mL��
��д������2�з�����Ӧ�����ӷ���ʽ��
�ڲ�Ʒ��Mg(ClO3)2��6H2O����������Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com