
【题目】水中的溶解氧是水生生物生存不可缺少的条件,某课外小组采用碘量法测定学校周边河水中的溶解氧,实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样,记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2![]() +I2=2I+
+I2=2I+![]() )。
)。
回答下列问题:
(1)氧的固定”中发生反应的化学方程式为_________________________________。
(2)Na2S2O3溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、胶头滴管、试剂瓶和_________________________,配制溶液定容时俯视会导致Na2S2O3溶液的浓度__________,(填“偏高”或“偏低”)蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除________________及二氧化碳。
(3)取100.00 mL水样经固氧、酸化后,用0.5 mol·L1Na2S2O3溶液滴定,以_________作指示剂,如何判断该反应到达终点_________________________________________________;若反应中消耗Na2S2O3溶液的体积为10 mL,则水样中溶解氧的含量为_________mg·L1。
(4)上述滴定完成时,若滴定前平视,滴定后仰视会导致测量结果___________。(填“偏高”或“偏低”)
【答案】![]() 容量瓶和玻璃棒偏高氧气淀粉溶液当滴加最后一滴Na2S2O3溶液时蓝色刚好褪去,且半分钟内不变色400偏高
容量瓶和玻璃棒偏高氧气淀粉溶液当滴加最后一滴Na2S2O3溶液时蓝色刚好褪去,且半分钟内不变色400偏高
【解析】
(1)由题述信息可知“氧的固定”中发生反应的化学方程式为![]() ;(2)配制一定物质的浓度的溶液所需的玻璃仪器有烧杯、胶头滴管、试剂瓶、玻璃棒、容量瓶等,故答案为容量瓶和玻璃棒;定容时俯视会造成溶液的体积偏大,所配溶液的浓度偏高,故答案为偏高;(3)水样经固氧、酸化后,滴入淀粉,溶液呈蓝色,用0.5 mol·L1Na2S2O3溶液滴定至终点时溶液的蓝色恰好完全褪去;根据关系式O2~2MnO(OH)2~2I2~4Na2S2O3,可知水样中溶解氧含量为[(0.5×10×10-3)÷4×32×103]÷0.1=400(mg·L1),故答案为:淀粉、当滴加最后一滴Na2S2O3溶液时蓝色刚好褪去,且半分钟内不变色、400;(4)若滴定前平视,滴定后仰视会造成消耗Na2S2O3溶液的体积偏大,从而导致测量结果偏高,故答案为偏高。
;(2)配制一定物质的浓度的溶液所需的玻璃仪器有烧杯、胶头滴管、试剂瓶、玻璃棒、容量瓶等,故答案为容量瓶和玻璃棒;定容时俯视会造成溶液的体积偏大,所配溶液的浓度偏高,故答案为偏高;(3)水样经固氧、酸化后,滴入淀粉,溶液呈蓝色,用0.5 mol·L1Na2S2O3溶液滴定至终点时溶液的蓝色恰好完全褪去;根据关系式O2~2MnO(OH)2~2I2~4Na2S2O3,可知水样中溶解氧含量为[(0.5×10×10-3)÷4×32×103]÷0.1=400(mg·L1),故答案为:淀粉、当滴加最后一滴Na2S2O3溶液时蓝色刚好褪去,且半分钟内不变色、400;(4)若滴定前平视,滴定后仰视会造成消耗Na2S2O3溶液的体积偏大,从而导致测量结果偏高,故答案为偏高。


科目:高中化学 来源: 题型:
【题目】无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如图,主要步骤如下:
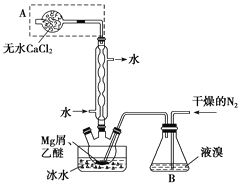
步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入15 mL液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至常温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0 ℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 室温下用苯溶解粗品,冷却至0 ℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160 ℃分解得无水MgBr2产品。
已知:
①Mg与Br2反应剧烈放热;MgBr2具有强吸水性;
②MgBr2+3C2H5OC2H5![]() MgBr2·3C2H5OC2H5。
MgBr2·3C2H5OC2H5。
请回答:
(1)仪器A的名称是________。实验中不能用干燥空气代替干燥N2,原因是__________。
(2)如将装置B改为装置C(如图),可能会导致的后果是______________________。
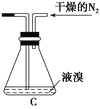
(3)步骤3中,第一次过滤除去的物质是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃ 时,下列酸的电离常数: 醋酸(CH3COOH):1.75×10-5氢氰酸(HCN) :6.2×10-10,氢氟酸(HF):7.2×10-4,甲酸(HCOOH): 1.77×10-4。下列说法不正确的是( )
A. 物质的量浓度均为0.1mol·L-1的上述溶液酸性最强的是:氢氟酸
B. 物质的量浓度均为0.1mol·L-1的CH3COONa和NaF溶液中,CH3COOH 的浓度大于HF的浓度,NaF溶液的pH比CH3COONa溶液大
C. 0.1mol·L-1的HCN和NaCN溶液等体积混合的溶液中:c(CN-)+)
D. 等浓度的NaCN 和HCOONa 混合溶液中:c(OH-)=c(H+)+c(HCN)+c(HCOOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。工艺流程图如图所示:
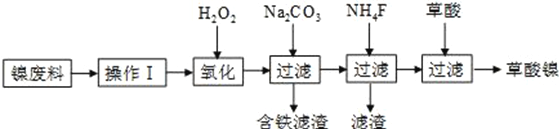
请回答下列问题:
(1)操作Ⅰ为__________________________。
(2)①加入H2O2发生的主要反应的离子方程式为_____________________________;
②加入碳酸钠溶液目的是调溶液的pH值在4.0~5.0,用化学用语回答加入碳酸钠的目的_________________________________________________________________。
(3)草酸镍(NiC2O4·2H2O)在热空气中干燥脱水后在高温下煅烧,可制得Ni2O3,同时获得混合气体,NiC2O4受热分解的化学方程式为___________________________________。
(4)加入草酸后如何证明沉淀完全______________________________________________;
过滤NiC2O4沉淀时如何洗涤沉淀_________________________________________________。
(5)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,则该电池负极的电极反应式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列有关问题。
(1)已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) △H1=+489.0kJ/mol
②Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g)△H2=-28.0kJ/mol
2Fe(s)+3CO2(g)△H2=-28.0kJ/mol
③C(石墨)+CO2(g)=2CO(g)△H3=akJ/mol
则a=_______kJ/mol。
(2)工业合成氨时,合成塔中每产生1molNH3放出46.1kJ的热量。
某小组研究在500℃下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
容器 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化/kJ | ||
N2 | H2 | NH3 | |||
a | 1 | 4 | 0 | t1min | 放出热量:27.66kJ |
b | 2 | 8 | 0 | t2min | 放出热量:Q |
①容器a中,0~t1时间的平均反应速率为v(H2)=_______。
②容器b中反应达平衡状态时,Q_______55.32kJ;平衡时,容器中H2的转化率:a_______b(填“>”或“<”或“=”)。
(3)以氨为原料,合成尿素的反应原理为:2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)△H=akJ·mol-1。
CO(NH2)2(l)+H2O(g)△H=akJ·mol-1。
为研究平衡时CO2的转化率与反应物投料比[![]() ]及温度的关系,研究小组在10L恒容密闭容器中进行模拟反应,(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
]及温度的关系,研究小组在10L恒容密闭容器中进行模拟反应,(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
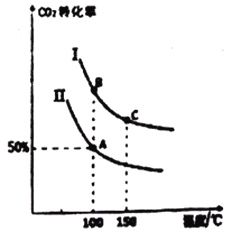
①a_______0(填“>”或“<”)。
②若n(CO2)起始=10mol,曲线Ⅱ的投料比为0.5,在100℃条件下发生反应,达平衡至
③A点平衡常数与B点平衡常数间的关系:KA_______KB;
B点平衡常数与C点平衡常数间的关系,KB_______KC(填“>”或“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组利用下图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl36H2O晶体(图中夹持及尾气处理装置均已略去)。请回答下列问题:

(1)装置B中发生反应的化学方程式是______________________________.
(2)E中出现的现象是______________________.
(3)该小组把B中反应后的产物加入到足量的盐酸中,用该溶液制取FeCl36H2O晶体.
①欲检验溶液中含有Fe3+,选用的试剂为________________,现象是_______________.
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的原因:_______________________.
③将此滤液中FeCl2完全氧化为FeCl3最好选择下列物质中的_______.
A.酸性KMnO4溶液 B.Cl2 C.Na2O2 D.FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在恒容密闭容基中,能表示反应X(气)+2Y(气)![]() 2Z(气)一定达到化学平衡状态的是( )
2Z(气)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为1∶2∶2②X、Y、Z的浓度不再发生变化③容器中的压强不再发生变化④单位时间内生成nmolZ,同时消耗nmolY
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某市售“84消毒液”瓶体部分标签如下图所示,该“84 消毒液”通常稀释100 倍(体积之比)后使用.请回答下列问题:

(1)该“84 消毒液”的物质的量浓度约为__mol/L.( 保留小数点后 1 位)
(2)该同学参阅此“84 消毒液”的配方,欲用NaClO固体配制480mL 与市售物质的量浓度相同的“84 消毒液”,下列说法中正确的是__( 填序号).
A.如下图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0g

(3)“84 消毒液”与稀硫酸混合使用可增强其消毒能力,某消毒小组人员用 98%( 密度为1.84g/cm3)的浓硫酸配制 500mL 2.3mol/L 的稀硫酸用于增强“84 消毒液”的消毒能力.
①需用浓硫酸的体积为__mL.
②取用任意体积的浓硫酸时,下列物理量中不随所取体积的多少而变化的是__。
A.溶液中H2SO4的物质的量 B.溶液的浓度
C.溶液的质量 D.溶液的密度
③对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于2.3mol/L有__。
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com