
【题目】不饱和聚酯(UP)![]() 是生产复合材料“玻璃钢”的基体树脂材料。如图是以基础化工原料合成UP流程:
是生产复合材料“玻璃钢”的基体树脂材料。如图是以基础化工原料合成UP流程:
![]()
下列说法不正确的是( )
A.丙可被KMnO4酸性溶液直接氧化制单体1
B.单体2可能是乙二醇
C.单体1、2、3经缩聚反应制得UP
D.调节单体的投料比,控制m和n的比值,获得性能不同的高分子材料
【答案】A
【解析】
根据缩聚反应的高聚物与单体之间的关系可推知,不饱和聚酯(UP)的单体有三个,分别是HOCH2CH2OH、HOOCCH=CHCOOH、![]() ,从合成UP流程来看,甲含4个C,2个不饱和度,应该是合成单体HOOCCH=CHCOOH的原料,结合随后的与溴的四氯化碳的加成反应可推出甲应为基本化工原料1,4丁二烯(CH2=CH-CH=CH2),甲与溴单质发生加成反应生成乙,推出乙为
,从合成UP流程来看,甲含4个C,2个不饱和度,应该是合成单体HOOCCH=CHCOOH的原料,结合随后的与溴的四氯化碳的加成反应可推出甲应为基本化工原料1,4丁二烯(CH2=CH-CH=CH2),甲与溴单质发生加成反应生成乙,推出乙为![]() ,乙水解可得到丙,则丙为
,乙水解可得到丙,则丙为![]() ,丙与HBr发生加成反应可得到
,丙与HBr发生加成反应可得到![]() ,再经过连续氧化会得到丁,则丁为
,再经过连续氧化会得到丁,则丁为![]() ,丁发生消去反应得到最终的单体1(HOOCCH=CHCOOH),最终经过缩聚反应得到UP,据此分析作答。
,丁发生消去反应得到最终的单体1(HOOCCH=CHCOOH),最终经过缩聚反应得到UP,据此分析作答。
A. 根据上述分析可知,丙为![]() ,碳碳双键和羟基均可被KMnO4酸性溶液氧化,不能直接得到单体1(HOOCCH=CHCOOH),故A错误;
,碳碳双键和羟基均可被KMnO4酸性溶液氧化,不能直接得到单体1(HOOCCH=CHCOOH),故A错误;
B. 单体2可能是乙二醇(HOCH2CH2OH),故B正确;
C. 单体1、2、3经脱水缩聚反应可制得UP,故C正确;
D. 调节单体的投料比,控制m和n的比值,可获得性能不同的高聚物,故D正确;
答案选A。


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】根据下列信息判断氢气燃烧生成水时的热量变化,其中一定正确的是( )

A. H2O分解为H2与O2时放出热量
B. 生成1mol H2O时吸收热量245 kJ
C. 甲、乙、丙中物质所具有的总能量大小关系为乙>甲>丙
D. 氢气和氧气的总能量小于水的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在固定体积的密闭容器中发生下列反应:2HI![]() H2+I2。若c(HI)由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么c(HI)由0.07 mol·L-1降到0.05 mol·L-1时,所需反应的时间为 ( )
H2+I2。若c(HI)由0.1 mol·L-1降到0.07 mol·L-1时,需要15 s,那么c(HI)由0.07 mol·L-1降到0.05 mol·L-1时,所需反应的时间为 ( )
A. 5 sB. 10 sC. 大于10 sD. 小于10 s
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应m A(g)+n B(g) ![]() p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
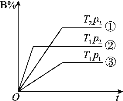
A.T1<T2 p1>p2 m+n>p 放热反应B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 C(s)+ H2O (g) ![]() CO (g)+H2 (g) △H>0 在某一时间段中反应速率与反应过程的曲线关系如图,下列说法正确的是( )
CO (g)+H2 (g) △H>0 在某一时间段中反应速率与反应过程的曲线关系如图,下列说法正确的是( )

A.CO的体积分数最高的一段时间为t5-t6
B.t2-t3和t3-t4时间段H2的体积分数相等
C.t1时刻改变的条件是降低温度
D.t4-t5时间段平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,一定不能自发进行的是( )
A. 2KClO3(s)===2KCl(s)+3O2(g) ΔH=-78.03kJ/mol ΔS=1110 J/(mol·K)
B. CO(g)===C(s,石墨)+![]() O2(g) ΔH=110.5kJ/mol ΔS=-89.36 J/(mol·K)
O2(g) ΔH=110.5kJ/mol ΔS=-89.36 J/(mol·K)
C. 4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s) ΔH=-444.3kJ/mol ΔS=-280.1 J/(mol·K)
D. NH4HCO3(s)+CH3COOH(aq)===CO2(g)+CH3COONH4(aq)+H2O(l) ΔH=37.301kJ/mol ΔS=184.05 J/(mol·K)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液W由下列离子中的若干种组成:H+、![]() 、Fe3+、Ba2+、Mg2+、
、Fe3+、Ba2+、Mg2+、![]() 、I-、OH-、
、I-、OH-、![]() 。向W中加入铝粉后有气体Y、含铝元素的离子X等生成。若不考虑水的电离,则下列说法中正确的是
。向W中加入铝粉后有气体Y、含铝元素的离子X等生成。若不考虑水的电离,则下列说法中正确的是
A.X一定是Al3+B.Y一定是H2
C.W中最多含有6种离子D.溶液中不可能含![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(CaCO3)=2.8×10-9,CaSO4在水中的沉淀溶解平衡曲线如图所示。下列判断错误的是

A.a点是CaSO4的饱和溶液而b点不是
B.蒸发水可使溶液由b点变化到a点
C.常温下,CaCO3(s)+![]() (aq)
(aq)![]() CaSO4(s)+
CaSO4(s)+![]() (aq)的K=3.1×10-4
(aq)的K=3.1×10-4
D.除去锅炉中的CaSO4时,可用Na2CO3溶液将其转化为CaCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2A(g)+B(g) ![]() 2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
(1)比较a___b(填“>”“=”或“<”)。
(2)下表为不同温度下该反应的平衡常数。由此可推知,表中T1____T2(填“>” “=”或“<”)。
T/K | T1 | T2 | T3 |
K | 1.00×107 | 2.45×105 | 1.88×103 |
若在原来的容器中,只加入2molC,500℃时充分反应达平衡后,吸收热量为c kJ,C的浓度___(填“>”、“=”或“<”)ωmol/L,a、b、c之间满足何种关系_______(用代数式表示)。
(3)在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是_____。
A.4molA和2molB B.4molA、2molB和2molC C.4molA和4molB D.6molA和4molB
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是____。
A.及时分离出C气体 B.适当升高温度 C.增大B的浓度 D.选择高效催化剂
(5)若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和1molB,500℃时充分反应达平衡后,放出热量为d kJ,则d_____b(填“>”“=”或“<”),理由是_________。
(6)在一定温度下,向一个容积可变的容器中,加入3molA和2molB及固体催化剂,使之反应:2A(g)+B(g)![]() 2C(g),平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量_____(填“不变”“变大”“变小”或“无法确定”)。
2C(g),平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量_____(填“不变”“变大”“变小”或“无法确定”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com