
| A、将空气通过灼热的铜网可以除去O2 |
| B、用点燃的方法可以除去CO2中的CO |
| C、pH试纸使用前,先用蒸馏水湿润,再测定未知溶液的pH |
| D、稀释浓硫酸时,向浓硫酸中缓缓加入蒸馏水,用玻璃棒搅拌 |


 百年学典课时学练测系列答案
百年学典课时学练测系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下:
某红色固体粉末样品可能含有Fe2S3和Cu2O中的一种或两种,某校化学自主探究实验小组拟对其组成进行探究,探究方案设计如下:查看答案和解析>>
科目:高中化学 来源: 题型:

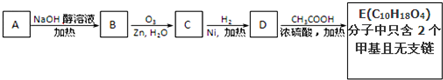
查看答案和解析>>
科目:高中化学 来源: 题型:
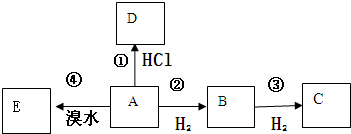
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用碱式滴定管量取一定体积的待测白醋放入锥形瓶中 |
| B、称取4.0gNaOH到1000mL容量瓶加水至刻度,配成1.00 mol?L-1NaOH标准溶液 |
| C、用NaOH溶液滴定白醋,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不退色时,为滴定终点 |
| D、滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解、NaOH溶液 |
| B、蒸馏、Na2CO3溶液 |
| C、酯化反应、石蕊试液 |
| D、中和滴定、pH试纸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com