
一定量 Fe和 Fe2O3的混合物投入250 mL 2 mol/L HNO3溶液中,固体完全溶解后,生成1.12 L(标准状况) NO (HNO3的还原产物假定仅此一种)再向反应后的溶液中加1 mol/L NaOH 溶液,要使铁元素完全沉淀下来,所加入的NaOH溶液的体积最少是 ( )
A.450 mL B.500 mL C.400 mL D.无法确定
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
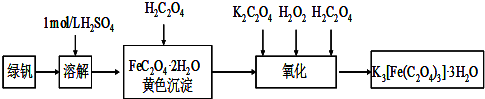
查看答案和解析>>
科目:高中化学 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高一化学(上) 题型:013
将一定量Fe粉和Fe(OH)3的混合粉末在空气中灼烧到质量不再变化为止,发现加热前后混合物质量不变,则原混合物中Fe和Fe(OH)3的物质的量之比为
[ ]
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com