
| ʵ����� | KClO3���� | ������������ | �������� |
| �� | 1.2g | ���������� | |
| �� | 1.2g | CuO 0.5g | |
| �� | 1.2g | MnO2 0.5g |
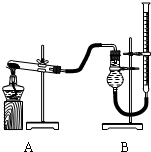


 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��2009?��ɽһģ��X��Y��Z��W����Ԫ���ڶ����ڱ������λ����ͼ��Y��W������֮��Ϊ23������˵����ȷ���ǣ�������
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
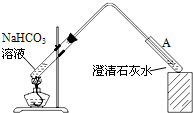 ��2009?��ɽһģ��10��ʱ�����ձ��м���0.1mol/L�� NaHCO3��Һ400mL�����ȣ���ø���Һ��pH�������±仯��
��2009?��ɽһģ��10��ʱ�����ձ��м���0.1mol/L�� NaHCO3��Һ400mL�����ȣ���ø���Һ��pH�������±仯��| �¶ȣ��棩 | 10 | 20 | 30 | 50 | 70 |
| pH | 8.3 | 8.4 | 8.5 | 8.9 | 9.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
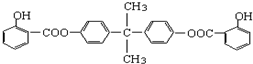

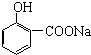
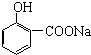


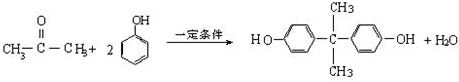

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com