
可逆反应:2NO(g)+O2(g) 2NO2(g),在体积不变的密闭容器中反应,一定达到平衡状态的标志是( )
2NO2(g),在体积不变的密闭容器中反应,一定达到平衡状态的标志是( )
A.单位时间内生成n mol O2的同时生成n mol NO2
B.混合气体的颜色不再改变的状态
C.ν(NO2):ν(NO):ν(O2)=2:2:1的状态
D.混合气体的密度不再改变的状态
科目:高中化学 来源:2016-2017学年湖北省高二上学期期中化学试卷(解析版) 题型:选择题
在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0
CO2(g)+H2(g) ΔH<0

下列分析中不正确的是( )
A.图Ⅰ研究中的是t0时升高温度对反应速率的影响
B.图Ⅱ研究的是t0时增大压强(缩小体积)或使用催化剂对反应速率的影响
C.图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂
D.图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期第一次月考化学试卷(解析版) 题型:选择题
由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同。则该混合气体中CO2、H2和CO的体积比为( )
A.29∶8∶13 B.22∶1∶14 C.13∶16∶29 D.26∶16∶57
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上学期第一次月考化学试卷(解析版) 题型:选择题
下列实验目的能够实现的是( )
A. 用托盘天平称取3.23 g NaCl固体 B. 用50 mL量筒量取30.12 mL水
C. 向小试管中加入100 mL稀盐酸 D. 用胶头滴管取约1 mL溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:选择题
关于下列各装置图的叙述中,不正确的是( )

A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.用装置①进行电镀,镀件接在b极上
C.装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+
D.装置③中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.对于有气体参与的反应,增大压强,活化分子总数增多,化学反应速率增大
B.对放热反应而言,升高温度,活化分子百分数减少,化学反应速率减小
C.活化分子间发生的碰撞为有效碰撞
D.使用催化剂,活化分子百分数增多,化学反应速率增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上期中化学试卷(解析版) 题型:填空题
(1) 物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中CH3COO-和Na+浓度相等,则醋酸体积__________氢氧化钠溶液体积 (填“>”“=”“<”)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液,溶液中c(Na+)___________c(CH3COO-)(填“>”“=”“<”)。
(3)某温度(t℃)时,水的KW=10-13,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4的溶液bL混合,若所得混合液为中性,则a∶b___________;若所得混合液的pH=2,则a∶b___________。
(4)室温下,若某pH值的硫酸溶液中水电离的c(H+)=1.0×10-amol·L-1,而相同pH值的硫酸铝溶液中水电离出的c(H+)=1.0×10-b mol·L-1,(已知a.b均小于14的正整数),那么a和b之间满足的数量关系是____________(用一个等式和一个不等式表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上期中化学试卷(解析版) 题型:选择题
在研宄物质变化时,人们可以从不同的角度、不同的层面来认识物质变化时所引起的化学键及能置变化。据此判断以下叙述错误的是
A.金属钠与氯气反应生成氯化钠后,稳定性增强,体系的能量降低
B.物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能释放出来
C.氮分子内部存在着很强的共价键,故通常状况下氮气的化学性质很不活泼
D.需加热才能发生的反应不一定是吸收能量的反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:选择题
在一定条件下,对于反应mA(g)+nB(g) cC(g)+dD(g),C物质的含量(c%)与温度、压强的关系如图所示,下列判断正确的是( )
cC(g)+dD(g),C物质的含量(c%)与温度、压强的关系如图所示,下列判断正确的是( )
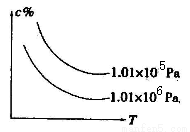
A.ΔH<0 ΔS>0 B.ΔH>0 ΔS<0
C.H>0 ΔS>0 D.H<0 ΔS<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com