
ΓΨΧβΡΩΓΩά§ΜχΖ÷άύ’ΐ‘Ύ»ΪΙζ÷πΫΞΆΤΙψΘ§ά§ΜχΉ ‘¥Μ· «Ω…≥÷–χΓΔ¬Χ…ΪΖΔ’ΙΒΡ÷Ί“ΣΆΨΨΕΓΘ”…Ϋπ τΖœΝœ(÷ς“ΣΚ§ΧζΓΔΆ≠ΚΆΥϋΟ«ΒΡ―θΜ·Έο)÷ΤΒΟΦν ΫΧΦΥαΆ≠ΚΆΡΠΕϊ―Έ[(NH4)2SO4ΓΛFeSO4ΓΛxH2O]ΒΡΙΛ“’Νς≥Χ»γΆΦΥυ ΨΘΚ
“―÷ΣΘΚKsp[Fe(OH)3]=1ΓΝ10-38Θ§Ksp[Cu(OH)2]=2.2ΓΝ10-20Θ§“ΜΑψ»œΈΣΡ≥άκΉ”≈®Ε»–Γ”ΎΜρΒ»”Ύ10-5mol/L ±Θ§ΗΟάκΉ”ΉΣΜ·Μρ»Ξ≥ΐΆξ»ΪΓΘ
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)»»¥ΩΦνΒΡΉς”Ο «__Θ§H2O2ΒΡΒγΉ” ΫΈΣ__ΓΘ
(2)ΒςpH≤Ϋ÷ηΩ…―Γ”ΟΒΡ ‘ΦΝΈΣ__ΓΘ
AΘ°CuO BΘ°Cu(OH)2 CΘ°Fe2O3 DΘ°Fe(OH)3
(3)»τΥυΒΟ»ή“Κ÷–c(Cu2+)=0.22molΓΛL-1Θ§‘ρ–η“ΣΒςΫΎΒΡpHΖΕΈß «__ΓΘ
(4)»ή“Κ1Ψ≠ΙΐΦ”»»ΓΔ’τΖΔ÷Ν__ ±Θ§Ή‘»Μά以֥مΒΟΒΫΨßΧεΘ§»ΜΚσ≥ι¬ΥΘ§”ΟΨΤΨΪœ¥Β”ΨßΧεΘ§ΨΤΨΪœ¥Β”ΒΡΡΩΒΡ «__ΓΘ
(5)–¥≥ωΗΟΝς≥Χ÷–…ζ≥…Φν ΫΧΦΥαΆ≠ΒΡάκΉ”ΖΫ≥Χ Ϋ__ΓΘ
(6)»Γ3.92gΡΠΕϊ―Έ≤ζΤΖΘ§‘ΎΗτΨχΩ’ΤχΒΡΧθΦΰœ¬Φ”»»÷Ν135ΓψC ±Άξ»Ϊ ß»ΞΫαΨßΥ°Θ§¥Υ ±ΙΧΧε÷ ΝΩΈΣ2.84gΘ§‘ρΗΟΡΠΕϊ―ΈΫαΨßΥ°Ηω ΐx=__ΓΘ
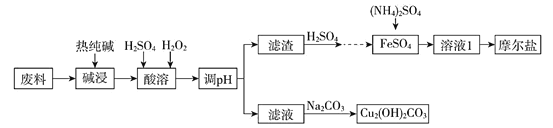
ΓΨ¥πΑΗΓΩ»Ξ≥ΐΖœΝœ±μΟφΒΡ”ΆΈέ ![]() AB 3~4.5 »ή“Κ±μΟφ≥ωœ÷ΨßΡΛ(Μρ»ή“Κ÷–≥ωœ÷ΨßΧε) ≥ΐ»ΞΨßΧε±μΟφΥ°Ζ÷ 2Cu2++3CO32-+2H2O=Cu2(OH)2CO3Γΐ+2HCO3-(Μρ2Cu2++2CO32-+H2O=Cu2(OH)2CO3Γΐ+CO2Γϋ) 6
AB 3~4.5 »ή“Κ±μΟφ≥ωœ÷ΨßΡΛ(Μρ»ή“Κ÷–≥ωœ÷ΨßΧε) ≥ΐ»ΞΨßΧε±μΟφΥ°Ζ÷ 2Cu2++3CO32-+2H2O=Cu2(OH)2CO3Γΐ+2HCO3-(Μρ2Cu2++2CO32-+H2O=Cu2(OH)2CO3Γΐ+CO2Γϋ) 6
ΓΨΫβΈωΓΩ
Φ”»κ»»ΒΡ¥ΩΦν“ΚΘ§Ϋπ τΖœΝœ(÷ς“ΣΚ§ΧζΓΔΆ≠ΚΆΥϋΟ«ΒΡ―θΜ·Έο)÷–ΒΡ÷ς“Σ≥…Ζ÷ΕΦ≤ΜΖΔ…ζΖ¥”ΠΘ§Υυ“‘»»ΒΡ¥ΩΦν“ΚΒΡΉς”Ο÷ΜΡή «»Ξ≥ΐ”ΆΈέΘΜΦ”»κH2SO4ΓΔH2O2Θ§ΧζΦΑ―θΜ·Έο»ήΫβ≤ΔΉΣΜ·ΈΣFe3+Θ§Ά≠ΦΑ―θΜ·Έο»ήΫβ…ζ≥…Cu2+ΘΜΒςpHΫΪFe3+ΉΣΜ·ΈΣFe(OH)3≥ΝΒμΘ§”ΟΝρΥα»ήΫβ…ζ≥…ΝρΥαΧζΘ§‘ΌΦ”»κΜΙ‘≠ΧζΖέΉΣΜ·ΈΣΝρΥα―«ΧζΘ§Φ”»κΝρΥαοßΉνΚσΒΟΡΠΕϊ―ΈΓΘ¬Υ“Κ÷–Κ§”–Cu2+Θ§Φ”»κNa2CO3»ή“ΚΖΔ…ζΥΪΥ°ΫβΖ¥”Π…ζ≥…Cu2(OH)2CO3ΓΘ
(1)”…“‘…œΖ÷ΈωΩ…÷ΣΘ§άϊ”Ο»»ΒΡ¥ΩΦν»ή“ΚΥ°Ϋβ Ι»ή“Κ≥ Ϋœ«ΩΒΡΦν–‘Θ§¥”Εχ¥οΒΫ»Ξ≥ΐ”ΆΈέΒΡΡΩΒΡΘ§ΤδΉς”Ο «»Ξ≥ΐΖœΝœ±μΟφΒΡ”ΆΈέΘ§H2O2ΈΣΙ≤ΦέΜ·ΚœΦέΘ§Φ»¥φ‘ΎO-HΙ≤ΦέΦϋΘ§”÷¥φ‘ΎO-OΙ≤ΦέΦϋΘ§ΤδΒγΉ” ΫΈΣ![]() ΓΘ¥πΑΗΈΣΘΚ»Ξ≥ΐΖœΝœ±μΟφΒΡ”ΆΈέΘΜ
ΓΘ¥πΑΗΈΣΘΚ»Ξ≥ΐΖœΝœ±μΟφΒΡ”ΆΈέΘΜ![]() ΘΜ
ΘΜ
(2)ΒςpHΒΡΡΩΒΡΘ§ «ΫΪFe3+ΉΣΜ·ΈΣFe(OH)3≥ΝΒμΘ§Ά§ ±≤Μ“ΐ»κ–¬ΒΡ‘”÷ Θ§Ω…―Γ‘ώCuOΓΔCu(OH)2Θ§Υυ“‘Ω…―Γ”ΟΒΡ ‘ΦΝΈΣABΓΘ¥πΑΗΈΣΘΚABΘΜ
(3) Ksp[Fe(OH)3]=1ΓΝ10-38Θ§c(Fe3+)=10-5mol/LΘ§c(OH-)=10-11mol/LΘ§pH=3ΘΜ»τΥυΒΟ»ή“Κ÷–c(Cu2+)=0.22molΓΛL-1Θ§άϊ”ΟKsp[Cu(OH)2]=2.2ΓΝ10-20Θ§Ω…«σΒΟc(OH-)=![]() =
=![]() mol/LȧpH=-lg(
mol/LΘ§pH=-lg(![]() ΓΝ10-5)=4.5Θ§‘ρ–η“ΣΒςΫΎΒΡpHΖΕΈß «3~4.5ΓΘ¥πΑΗΈΣΘΚ3~4.5ΘΜ
ΓΝ10-5)=4.5Θ§‘ρ–η“ΣΒςΫΎΒΡpHΖΕΈß «3~4.5ΓΘ¥πΑΗΈΣΘΚ3~4.5ΘΜ
(4)¥”»ή“Κ1÷–ΜώΒΟΡΠΕϊ―ΈΨßΧεΘ§–ηΨ≠ΙΐΦ”»»ΓΔ’τΖΔ÷Ν»ή“Κ±μΟφ≥ωœ÷ΨßΡΛ(Μρ»ή“Κ÷–≥ωœ÷ΨßΧε) ±ΘΜΉ‘»Μά以֥مΒΟΒΫΨßΧεΘ§»ΜΚσ≥ι¬ΥΘ§ΈΣΖάΚφΗ… ±ΨßΧε ß»ΞΫαΨßΥ°Θ§Υυ“‘≤ΜΡή≤…”ΟΚφΗ…ΒΡΖΫΖ®Θ§Εχ”Π”ΟΨΤΨΪœ¥Β”ΨßΧεΘ§ΨΤΨΪœ¥Β”ΒΡΡΩΒΡ «≥ΐ»ΞΨßΧε±μΟφΥ°Ζ÷ΓΘ¥πΑΗΈΣΘΚ»ή“Κ±μΟφ≥ωœ÷ΨßΡΛ(Μρ»ή“Κ÷–≥ωœ÷ΨßΧε)ΘΜ≥ΐ»ΞΨßΧε±μΟφΥ°Ζ÷ΘΜ
(5)ΗΟΝς≥Χ÷–Cu2+Θ§Φ”»κNa2CO3»ή“ΚΘ§άϊ”Ο≤ΩΖ÷άκΉ”ΖΔ…ζΥΪΥ°ΫβΖ¥”Π…ζ≥…Cu2(OH)2CO3Θ§άκΉ”ΖΫ≥Χ ΫΈΣ2Cu2++3CO32-+2H2O=Cu2(OH)2CO3Γΐ+2HCO3-(Μρ2Cu2++2CO32-+H2O=Cu2(OH)2CO3Γΐ+CO2Γϋ)ΓΘ¥πΑΗΈΣΘΚ2Cu2++3CO32-+2H2O=Cu2(OH)2CO3Γΐ+2HCO3-(Μρ2Cu2++2CO32-+H2O=Cu2(OH)2CO3Γΐ+CO2Γϋ)ΘΜ
(6)m[(NH4)2SO4ΓΛFeSO4]= 2.84gΘ§n[(NH4)2SO4ΓΛFeSO4]=![]() =0.01molΘ§m(H2O)= 3.92g-2.84g=1.08gΘ§n(H2O)=
=0.01molΘ§m(H2O)= 3.92g-2.84g=1.08gΘ§n(H2O)=![]() =0.06molΘ§‘ρΗΟΡΠΕϊ―ΈΫαΨßΥ°Ηω ΐx=
=0.06molΘ§‘ρΗΟΡΠΕϊ―ΈΫαΨßΥ°Ηω ΐx=![]() =6ΓΘ¥πΑΗΈΣΘΚ6ΓΘ
=6ΓΘ¥πΑΗΈΣΘΚ6ΓΘ


 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ –Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
–Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
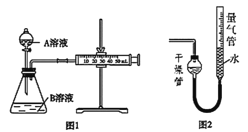
ΓΨΧβΡΩΓΩ Β―ι “”Ο≈®œθΥα―θΜ·C2H2÷Τ»ΓH2C2O4ΓΛ2H2OΒΡΉΑ÷Ο»γΆΦΥυ Ψ(Βγ ·÷ς“Σ≥…Ζ÷ΈΣCaC2Θ§Κ§…ΌΝΩCaS‘”÷ )Θ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
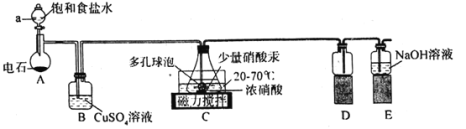
A.ΉΑ÷ΟAΩ…ΉςMnO2ΚΆ≈®―ΈΥαΖ¥”Π÷Τ±ΗCl2ΒΡΖΔ…ζΉΑ÷Ο
B.ΉΑ÷ΟBΒΡΉς”Ο «≥ΐ»ΞC2H2÷–ΒΡH2S
C.ΉΑ÷ΟDΒΡΉς”Ο « ’Φ·≤ίΥα
D.ΉΑ÷ΟE÷–ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ3NO2+2OH-=2NO3-+NO+H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΕκΟΦΫπΕΞ…ψ…μ―¬”÷≥Τ…α…μ―¬Θ§“ρ≥Θœ÷ΖπΙβΕχΒΟΟϊΓΘΓΑΖπΙβΓ±“ρ…ψ»κ…μ÷°”Αœώ”ΎΤδ÷–Θ§Υλ≥ΤΓΑ…ψ…μΙβΓ±Θ§ΈΣΕκΟΦ ΛΨΑ÷°“ΜΓΘ…ψ…ζ―¬œ¬ΆΝ»ά÷–ΗΜΚ§ΝΉΩσΘ§Υυ“‘‘ΎΈό‘¬ΒΡΚΎ“ΙΩ…ΦϊΒΫ―¬œ¬”ΪΙβΈό ΐΓΘ
Θ®1Θ©ΓΑ”ΪΙβΓ±÷ς“Σ≥…Ζ÷ « PH3Θ®λΔΘ©Θ§ΤδΫαΙΙ ΫΈΣ __________ Θ§œ¬Ν–”–ΙΊ PH3 ΒΡΥΒΖ®¥μΈσΒΡ «___________ ΓΘ
a.PH3 Ζ÷Ή” «ΦΪ–‘Ζ÷Ή”
b.PH3 Ζ÷Ή”Έ»Ε®–‘ΒΆ”Ύ NH3 Ζ÷Ή”Θ§“ρΈΣ N-H ΦϋΦϋΡήΗΏ
c.“ΜΗω PH3 Ζ÷Ή”÷–Θ§P ‘≠Ή”ΚΥΆβ”–“ΜΕ‘Ι¬ΒγΉ”Ε‘
d.PH3 Ζ–ΒψΒΆ”Ύ NH3 Ζ–ΒψΘ§“ρΈΣ P-H ΦϋΦϋΡήΒΆ
Θ®2Θ©PH3 ΒΡΖ–Βψ±» NH3______ΧνΓΑΗΏΓ±ΜρΓΑΒΆΓ±Θ© NH3 ΒΡΥ°»ή“ΚΦν–‘_____PH3 ΒΡΥ°»ή“ΚΦν–‘Θ®ΧνΓΑ¥σ”ΎΓ±ΜρΓΑ–Γ”ΎΓ±Θ©ΘΜ¬»Μ·γlΘ®PH4C1Θ©”κΦνΖ¥”Π…ζ≥…λΔΒΡάκΉ”ΖΫ≥Χ ΫΈΣ _______________________ ΓΘ
Θ®3Θ©PH3 «“Μ÷÷ΜΙ‘≠ΦΝΘ§ΤδΜΙ‘≠ΡήΝΠ±» NH3 «ΩΘ§Ά®≥Θ«ιΩωœ¬Ρή¥”Cu2+ΓΔAg+ΓΔHg2+Β»―Έ»ή“Κ÷–ΜΙ‘≠≥ωΫπ τΘ§ Εχ±Ψ…μ±Μ―θΜ·ΈΣΉνΗΏ―θΜ·Χ§ΓΘPH3 ”κ CuSO4 »ή“ΚΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ ______________ΓΘ
Θ®4Θ©ΓΑ”ΪΙβΓ±≤ζ…ζΒΡ‘≠άμ «Ca3P2 ‘Ύ≥± ΣΒΡΩ’Τχ÷–ΨγΝ“Ζ¥”ΠΘ§–¥≥ωΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ__________________ΓΘ
Θ®5Θ©PH3 ”–ΕΨΘ§ΑΉΝΉΙΛ≥ß≥Θ”Ο Cu2+ΓΔPd2+“ΚœύΆ―≥ΐ PH3ΘΚPH3+2O2![]() H3PO4Θ§ΤδΥϊΧθΦΰœύΆ§ ±Θ§ »ήΫβ‘Ύ»ή“Κ÷–O2 ΒΡΧεΜΐΖ÷ ΐ”κ PH3 ΒΡΨΜΜ·–߬ ”κ ±ΦδΒΡΙΊœΒ»γΆΦΥυ ΨΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
H3PO4Θ§ΤδΥϊΧθΦΰœύΆ§ ±Θ§ »ήΫβ‘Ύ»ή“Κ÷–O2 ΒΡΧεΜΐΖ÷ ΐ”κ PH3 ΒΡΨΜΜ·–߬ ”κ ±ΦδΒΡΙΊœΒ»γΆΦΥυ ΨΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ”…ΆΦΩ…÷ΣΘ§ΗΜ―θ”–άϊ”Ύ______Θ®―ΓΧνΓΑ―”≥ΛΓ±ΜρΓΑΥθΕΧΓ±Θ©¥ΏΜ·Ής”ΟΒΡ≥÷–χ ±ΦδΓΘ
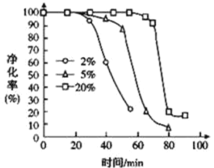
ΔΎΥφΉ≈Ζ¥”ΠΫχ––Θ§PH3 ΒΡΨΜΜ·–߬ Φ±ΨγΫΒΒΆΒΡ‘≠“ρΩ…ΡήΈΣ _________________ ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΒγΫβΖ®ΉΣΜ·CO2 Βœ÷CO2Ή ‘¥Μ·άϊ”ΟΓΘΒγΫβCO2÷ΤΦΉΥα―ΈΒΡΉΑ÷Ο»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®÷–’ΐ»ΖΒΡ «Θ® Θ©
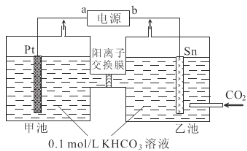
A.b «Βγ‘¥’ΐΦΪ
B.K+”…““≥ΊœρΦΉ≥Ί«®“Τ
C.ΦΉ≥Ί÷–KHCO3»ή“Κ≈®Ε»‘ω¥σΘ§““≥Ί÷–KHCO3»ή“Κ≈®Ε»ΫΒΒΆ
D.““≥ΊΒγΦΪΖ¥”Π ΫΈΣΘΚCO2+HCO3-+2e-=HCOO-+CO32-
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥ Β―ι–ΓΉι”ΟΝρΥαΥαΜ·ΒΡΗΏΟΧΥαΦΊ»ή“Κ”κ≤ίΥα»ή“ΚΖ¥”Π≤βΕ®ΒΞΈΜ ±ΦδΡΎ…ζ≥…CO2ΒΡΝΩά¥ΧΫΨΩ”ΑœλΖ¥”ΠΥΌ¬ ΒΡ“ρΥΊΓΘ…ηΦΤ Β―ιΖΫΑΗ»γ±μΘΚ
Β―ι–ρΚ≈ | A»ή“Κ | B»ή“Κ |
ΔΌ | 20mL0.1molΓΛL-1H2C2O4»ή“Κ | 30mL0.02molΓΛL-1Υα–‘KMnO4»ή“Κ |
ΔΎ | 20mL0.2molΓΛL-1H2C2O4»ή“Κ | 30mL0.02molΓΛL-1Υα–‘KMnO4»ή“Κ |
Θ®1Θ©ΆΦ1ΉΑ÷Ο÷– ΔΖ≈A»ή“ΚΒΡ“«ΤςΟϊ≥Τ «_____Θ§Φλ―ι»γΆΦ1ΉΑ÷ΟΤχΟή–‘ΒΡΖΫΖ®ΈΣ_____ΓΘ
Θ®2Θ©ΝρΥαΥαΜ·ΒΡΗΏΟΧΥαΦΊ»ή“Κ”κ≤ίΥα»ή“ΚΖ¥”ΠΒΡΜ·―ßΖ¥”ΠΖΫ≥Χ ΫΈΣ_____ΓΘ
Θ®3Θ©¥Υ Β―ιΧΫΨΩΒΡ «_____“ρΥΊΕ‘Μ·―ßΖ¥”ΠΥΌ¬ ΒΡ”ΑœλΘ§»τ Β―ιΔΎ‘Ύ40sΡ© ’Φ·ΝΥ22.4mLCO2(±ξΉΦΉ¥Ωωœ¬)Θ§‘ρ‘Ύ40sΡΎΘ§v(MnO4-)=_____(Κω¬‘»ή“ΚΜλΚœ«ΑΚσΧεΜΐΒΡ±δΜ·)ΓΘ
Θ®4Θ©–ΓΉιΆ§―ßΫΪΆΦ1ΒΡΤχΧε ’Φ·ΉΑ÷ΟΗΡΈΣΆΦ2Θ§ Β―ιΆξ±œά以ΚσΘ§ΕΝ ΐ ±ΖΔœ÷ΝΩΤχΙή“ΚΟφΗΏ”ΎΗ…‘οΙή“ΚΟφΘ§ΈΣΒΟΒΫΉΦ»Ζ ΐΨίΘ§≤…»ΓΒΡ≤ΌΉς «ΘΚ____ΓΘ
Θ®5Θ©≥ΐΝΥΆ®Ιΐ≤βΕ®ΒΞΈΜ ±ΦδΡΎ…ζ≥…CO2ΒΡΧεΜΐά¥±»ΫœΖ¥”ΠΥΌ¬ Θ§±Ψ Β―ιΜΙΩ…“‘Ά®Ιΐ≤βΕ®____ά¥±»ΫœΜ·―ßΖ¥”ΠΥΌ¬ ΓΘ
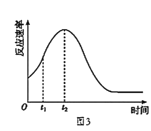
Θ®6Θ©Ά§―ßΟ«‘Ύ Β―ι÷–ΖΔœ÷Ζ¥”ΠΥΌ¬ Ήή «»γΆΦ3Υυ ΨΘ§ΧΫΨΩt1ΓΪt2 ±ΦδΡΎΥΌ¬ ±δΩλΒΡ÷ς“Σ‘≠“ρΩ…Ρή «ΘΚ____ΓΘ
A.ΗΟΖ¥”ΠΖ≈»» B.…ζ≥…ΒΡMn2+Τπ¥ΏΜ·Ής”Ο C.K2SO4≈®Ε»‘ω¥σ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩAΓΔBΓΔCΨυΈΣΕΧ÷ήΤΎ‘ΣΥΊΘ§ΥϋΟ«‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷Ο»γœ¬ΆΦΥυ ΨΓΘ“―÷ΣΘΚBΓΔCΝΫ‘ΣΥΊ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐ÷°ΚΆΒ»”ΎA‘ΣΥΊ‘≠Ή”ΉνΆβ≤ψΒγΉ” ΐΒΡ2±ΕΘΜB.CΝΫ‘ΣΥΊΒΡΚΥΒγΚ… ΐ÷°ΚΆ «A‘ΣΥΊ‘≠Ή”–ρ ΐΒΡ4±ΕΓΘœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «
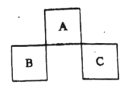
A.CΈΜ”Ύ‘ΣΥΊ÷ήΤΎ±μ÷–ΒΎ3÷ήΤΎΒΎVAΉε
B.BΒΡΖ«Ϋπ τ–‘±»A«Ω
C.CΒΡΤχΧ§«βΜ·ΈοΒΡΈ»Ε®–‘±»BΒΡ«Ω
D.‘≠Ή”ΑκΨΕΘΚr(B)<r(C)
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–”–ΙΊΥΒΖ®’ΐ»ΖΒΡ «
A.MgO(s)ΘΪC(s)=CO(g)ΘΪMg(g)ΗΏΈ¬œ¬ΡήΉ‘ΖΔΫχ––Θ§‘ρΗΟΖ¥”ΠΠΛHΘΨ0ΓΔΠΛSΘΨ0
B.≥ΘΈ¬œ¬Β»Έο÷ ΒΡΝΩ≈®Ε»ΒΡCH3COOH»ή“ΚΚΆHCl»ή“Κ÷–Θ§Υ°ΒΡΒγάκ≥ΧΕ»œύΆ§
C.0.1 molΓΛLΘ≠1 NH4Cl»ή“ΚΦ”Υ°œΓ ΆΘ§![]() ΒΡ÷Β‘ω¥σ
ΒΡ÷Β‘ω¥σ
D.Ε‘”ΎΖ¥”Π2SO2ΘΪO22SO3Θ§ Ι”Ο¥ΏΜ·ΦΝΡήΦ”ΩλΖ¥”ΠΥΌ¬ ≤ΔΧαΗΏSO2ΒΡΤΫΚβΉΣΜ·¬
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ≈πΧζΜλΚœΨΪΩσΚ§”–≈πΟΨ ·[MgBO2(OH)ΓΔ¥≈ΧζΩσ(Fe3O4)ΓΔ¥≈ΜΤΧζΩσ(FexS)ΓΔΤΖ÷ ”ΥΩσ(UO2)Β»Θ§“‘ΗΟΩσΈΣ‘≠Νœ÷Τ±ΗMgSO4ΓΛH2OΚΆ≈πΥα(H3BO3)ΒΡΙΛ“’Νς≥Χ»γœ¬ΘΚ
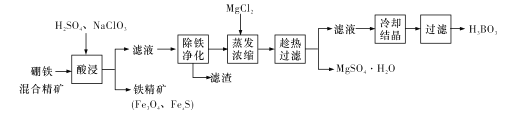
“―÷ΣΘΚ![]() ‘ΎpHΈΣ4ΓΪ5ΒΡ»ή“Κ÷–…ζ≥…UO2(OH)2≥ΝΒμΓΘ
‘ΎpHΈΣ4ΓΪ5ΒΡ»ή“Κ÷–…ζ≥…UO2(OH)2≥ΝΒμΓΘ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(l)ΓΑΥαΫΰΓ± ±Θ§ΈΣΝΥΧαΗΏΫΰ≥ω¬ Ω…≤…»ΓΒΡ¥κ ©”–ΘΚ________ (÷Ν…Ό¥πΝΫΗω¥κ ©)Θ§ΗΟ≤Ϋ÷η÷–NaC1O3Ω…ΫΪUO2ΉΣΜ·ΈΣ![]() Θ§‘ρΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_____ΓΘ
Θ§‘ρΗΟΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_____ΓΘ
(2)ΓΑ≥ΐΧζΨΜΜ·Γ±–η“ΣΦ”»κ____(ΧνΜ·―ß Ϋ)Α―»ή“ΚpHΒςΫΎ÷Ν4ΓΪ5Θ§¬Υ‘ϋΒΡ≥…Ζ÷ «_______ΓΘ
(3)ΓΑ’τΖΔ≈®ΥθΓ± ±Θ§Φ”»κΙΧΧεMgC12ΒΡΉς”Ο « ___ΓΘ
(4)ΧζΨΪΩσ(Fe3O4ΓΔFexS)Ψ≠Ιΐ“ΜœΒΝ–Φ”ΙΛΚσΘ§Ω…”Ο”Ύ÷Τ±Η«β―θΜ·ΧζΙΧΧεΓΘ“―÷ΣTΓφΘ§
![]() Θ§
Θ§![]() Θ§
Θ§![]() ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌ‘ΎTΓφΘ§ΦΌ…ηFe3+Υ°ΫβΒΡάκΉ”ΖΫ≥Χ Ϋ «ΘΚ![]() Θ§‘ρΗΟΧθΦΰœ¬Fe3+Υ°ΫβΖ¥”ΠΒΡΤΫΚβ≥Θ ΐK= __(”ΟΚ§“‘ΒΡΉ÷ΡΗ±μ Ψ)ΓΘ
Θ§‘ρΗΟΧθΦΰœ¬Fe3+Υ°ΫβΖ¥”ΠΒΡΤΫΚβ≥Θ ΐK= __(”ΟΚ§“‘ΒΡΉ÷ΡΗ±μ Ψ)ΓΘ
ΔΎ‘ΎTΓφœρ±ΞΚΆFe(OH)3ΓΔFe(OH)2ΒΡΜλΚœ»ή“Κ÷–Θ§Φ”»κ…ΌΝΩNaOHΙΧΧε(Κω¬‘»ή“ΚΧεΜΐ±δΜ·)Θ§‘ρ»ή“Κ÷–ΒΡc(Fe2+)Θ·c(Fe3+)Μα __(ΧνΓΑ±δ¥σΓ±ΓΑ±δ–ΓΓ±ΜρΓΑ≤Μ±δΓ±)Θ§«κΫαΚœœύΙΊ ΐΨίΆΤάμΥΒΟςΘΚ____ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΗυΨί‘≠Βγ≥ΊΒΡ÷Σ ΕΘ§œ¬Ν–Ζ¥”ΠΩ……ηΦΤ≥…‘≠Βγ≥ΊΒΡ «Θ® Θ©
A.CH3CH2OH+3O2![]() 2CO2+3H2O
2CO2+3H2O
B.Ba(OH)28H2O+2NH4Cl=BaCl2+2NH3Γϋ+10H2O
C.H2SO4+2NaOH=Na2SO4+2H2O
D.CaO+H2O=Ca(OH)2
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com