
【题目】已知某些共价键的键能如表所示,试回答下列问题:℃
共价键 | 键能 | 共价键 | 键能 |
| 436 |
| 467 |
| 243 |
| 945 |
| 413 |
| 431 |
(1)![]() 键的键能为什么比
键的键能为什么比![]() 键的键能大_______?
键的键能大_______?
(2)已知![]() 在
在![]() 时有
时有![]() 的分子分解,而
的分子分解,而![]() 在
在![]() 时可能完全分解为
时可能完全分解为![]() 和
和![]() ,试解释其中的原因_______。
,试解释其中的原因_______。
(3)试解释氮气能在空气中稳定存在的原因_______。
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
【题目】CO2是地球上取之不尽用之不竭的碳源,将CO2应用于生产中实现其综合利用是目前的研究热点。
(1)由CO2转化为羧酸是CO2资源化利用的重要方法。
I.在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。
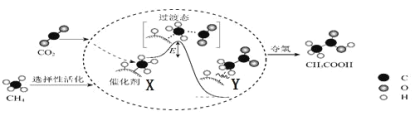
①在合成CH3COOH的反应历程中,下列有关说法正确的是_____。(填字母)
a.该催化剂使反应的平衡常数增大
b.CH4→CH3COOH过程中,有C—H键发生断裂
c.由X→Y过程中放出能量并形成了C—C键
②该条件下由CO2和CH4合成CH3COOH的化学方程式为_____。
II.电解法转化CO2制HCOOH的原理如图。

①写出阴极CO2还原为HCOO-的电极反应式:_____。
②电解一段时间后,阳极区的KHCO3溶液浓度降低,其原因是_____。
(2)由CO2合成甲醇是CO2资源化利用的重要方法。研究表明在催化剂作用下CO2和H2可发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH
①有利于提高合成CH3OH反应中CO2的平衡转化率的措施有_____。(填字母)
a.使用催化剂 b.加压 c.增大初始投料比![]()
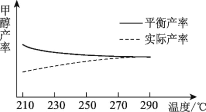
②研究温度对于甲醇产率的影响。在210℃~290℃保持原料气中CO2和H2的投料比不变,得到甲醇的实际产率、平衡产率与温度的关系如图所示。ΔH____0(填“>”或“<”),其依据是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素![]() 、
、![]() 、
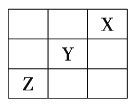
、![]() 在周期表中的相对位置如图所示。已知
在周期表中的相对位置如图所示。已知![]() 元素原子的外围电子排布式为
元素原子的外围电子排布式为![]() ,则下列说法不正确的是( )
,则下列说法不正确的是( )
A.![]() 元素原子的价电子排布式为
元素原子的价电子排布式为![]()
B.![]() 元素在元素周期表的第三周期第ⅥA族
元素在元素周期表的第三周期第ⅥA族
C.![]() 元素所在周期中所含非金属元素最多
元素所在周期中所含非金属元素最多
D.![]() 元素原子的核外电子排布式为
元素原子的核外电子排布式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 为直线形结构,
为直线形结构,![]() 为平面正三角形结构,
为平面正三角形结构,![]() 为三角锥形结构,请推测COS、
为三角锥形结构,请推测COS、![]() 、
、![]() 的空间构型:______________________________。
的空间构型:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.下表是从实验中测得的不同物质中氧氧键的键长和键能数据:
氧氧键 |
|
|
|
|
键长 | 149 | 128 | 121 | 112 |
键能 |
|
|
|
|
其中![]() 、
、![]() 的值尚未测定,但可根据规律推导
的值尚未测定,但可根据规律推导![]() 、
、![]() 、
、![]() 、
、![]() 的大小顺序是
的大小顺序是![]() ,该规律是( )
,该规律是( )
A.成键时,电子数越多,键能越大
B.键长越短,键能越大
C.成键所用电子数越少,键能越大
D.成键时电子对越偏移,键能越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有以下物质:①![]() 、②
、②![]() 、③
、③![]() 、④
、④![]() 、⑤
、⑤![]() 、⑥
、⑥![]() 、⑦
、⑦![]() 、⑧
、⑧![]() 和⑨
和⑨![]() 。
。
(1)只含有![]() 键的是__________(填序号,下同);
键的是__________(填序号,下同);
(2)既含有![]() 键又含有
键又含有![]() 键的是__________。
键的是__________。
(3)含有由两个原子的![]() 轨道重叠形成
轨道重叠形成![]() 键的是__________。
键的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。它是一种体心立方结构。实验测得金属钨的密度为19.30g·cm-3,钨的相对原子质量为183.9.假定金属钨为等直径的刚性球,请回答以下各题:
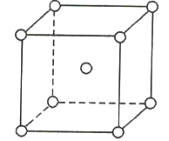
(1)每一个晶胞中分摊到__________个钨原子。
(2)计算晶胞的边长a。_____________
(3)计算钨的原子半径r(提示:只有体对角线上的各个球才是彼此接触的)。___________
(4)计算金属钨原子采取的体心立方密堆积的空间利用率。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为NaCl和CsCl的晶体结构,下列说法错误的是( )
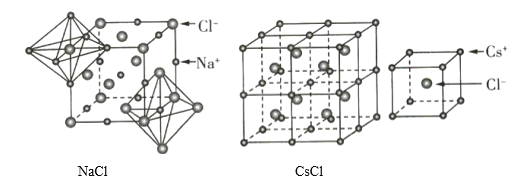
A.NaCl和CsCl都属于AB型的离子晶体
B.NaCl和CsC1晶体中阴、阳离子个数比相同,所以二者的阴、阳离子的配位数也相同
C.CsCl晶体中阴、阳离子的配位数均为8
D.NaCl和CsCl都属于AB型的离子晶体,但阴、阳离子的半径比不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含有Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol L-1的HC1溶液,测得溶液中某几种离子的物质的量的变化情况如图所示。下列说法不正确的是
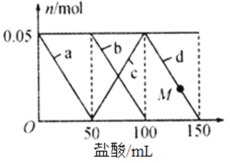
A.b和c曲线表示的离子反应均为CO32-+H+= HCO3-
B.结合H+的能力:AlO2>CO32> HCO3>Al(OH)3
C.原混合溶液中,CO32与AlO2的物质的量之比为2∶1
D.M点时A1(OH)3的质量等于3.9 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com