
右图为某种乙醇燃料电池示意图,工作时电子流方向如图所示,下列判断正确的是
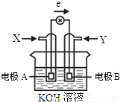
A.X为氧气
B.电极A反应式:CH3CH2OH-12e-+3H2O=2CO2+12H+
C.电极材料活泼性:A>B
D.B电极附近溶液pH增大
科目:高中化学 来源:2015-2016学年内蒙古巴彦淖尔一中高一上期中化学试卷(解析版) 题型:选择题
下列属于氧化还原反应的是
A.SO2+H2O=H2SO3
B.H2CO3=CO2↑+H2O
C.2NaOH+H2SO4=Na2SO4+2H2O
D.C+O2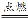 CO2
CO2
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三上学期1月月考理综化学试卷(解析版) 题型:实验题
某化学兴趣小组设计如下流程,从酸性工业废液(含H+、Al3+、Mg2+、Cr3+、SO42?)中提取铬.
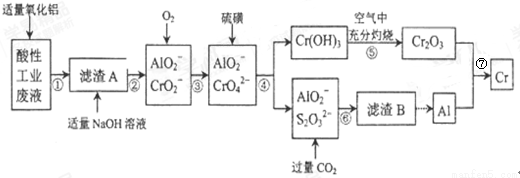
有关数据如表:
化合物 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
完全沉淀的PH | 10.5 | 4.3 | 5.3 |
开始溶解的pH | -- | 7.8 | 9.2 |
Ksp近似值 | 10-12 | 10-14 | 10-31 |
回答下列问题:
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是____。
(2)若酸性废液中c(Mg2+)=0.1mol/L,为达到步骤①的实验目的,则废液的pH应保持在_______范围(保留小数点后l位)。
(3)步骤②中生成NaCrO2 的离子方程式为_____________。
(4)步骤④中反应的离子方程式为________________。
(5)步骤⑤在空气中充分灼烧的目的是__________________,可选用的装置是________。(填序号)

(6)步骤⑦中发生的化学反应方程式为____________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016年海南省高一上第三次月考化学试卷(解析版) 题型:选择题
向下列各物质的水溶液中滴加稀硫酸或MgCl2溶液时,均有白色沉淀生成的是
A.BaCl2 B.KOH C.Na2CO3 D.Ba(OH)2
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:填空题
化学反应原理是中学化学学习的重要内容。请回答下列问题:
(1)下列判断正确的是______________。
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1 CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH2
则ΔH1﹤ΔH2
②H2(g)+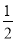 O2(g)===H2O(l) ΔH1 2H2(g)+O2(g)═2H2O(l) ΔH2
O2(g)===H2O(l) ΔH1 2H2(g)+O2(g)═2H2O(l) ΔH2
则ΔH1﹤ΔH2
③t ℃时,在一定条件下,将1 mol SO2和1 mol O2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时反应放出的热量分别为Q1和Q2
则Q1﹤Q2
④CaCO3(s)===CaO(s)+CO2(g) ΔH1 CaO(s)+H2O(l)===Ca(OH)2(s) ΔH2
则ΔH1﹤ΔH2
(2)依据氧化还原反应Zn(s)+Cu2+(aq)===Zn2+(aq)+Cu(s)
设计的原电池如图所示。
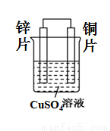
请回答下列问题:
①铜电极发生的电极反应为_____________________。
②溶液中Cu2+向________极移动。
(3)在一恒温、恒容密闭容器中充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g) + 3H2(g)  CH3OH (g) + H2O(g) △H=-49.0 kJ/mol
CH3OH (g) + H2O(g) △H=-49.0 kJ/mol
某种反应物和生成物的浓度随时间变化如图所示。
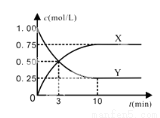
回答下列问题:
①Y的化学式是 。
②反应进行到3min时, v正 v逆(填“>”或“<”、“=”)。反应前3min,H2的平均反应速率,v(H2)= mol·L-1·min-1。
③能证明该反应达到化学平衡状态的依据是 。
A.容器内各气体的体积分数保持不变
B.混合气体密度不变
C.3v逆(CH3OH) =v正(H2)
D.混合气体的平均相对分子质量不变
E.CO2的转化率为70%
F.混合气体中CO2与H2的体积比为1﹕3
④上述温度下,反应CH3OH (g) + H2O(g)  CO2(g) + 3H2(g)的平衡常数K= (计算结果保留2位小数)。
CO2(g) + 3H2(g)的平衡常数K= (计算结果保留2位小数)。
⑤上述反应达到平衡后,往容器中同时加入0.1mol CO2和0.3mol H2O (g),此时平衡将 (填“向左”、“向右”或“不”)移动。
(4)室温时,向20 mL 0.1 mol/L的醋酸溶液中不断滴入0.1 mol/L的NaOH溶液,溶液的pH变化与所加NaOH溶液体积的关系如下图所示。下列有关溶液中离子、分子浓度大小关系的描述中正确的是____________。
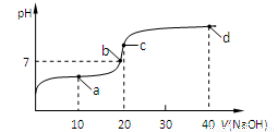
①.a点时:c(CH3COOH) >c(CH3COO-) > c(Na+) > c(H+) >c(OH-)
②.b点时:c(Na+)=c(CH3COO-) >c(H+) =c(OH-)
③.c点时:c(OH-)=c(CH3COOH)+c(H+)
④.d点时:c(Na+)> c(CH3COO-) > c(OH-) >c(H+)
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:填空题
某温度下,纯水中c(H+) = 2×10-7 mol•L-1,则此温度____________25°C(填“>”、“<”或“=”)。若温度不变,滴入稀盐酸,使c(H+) = 8×10-4 mol•L-1,则此时溶液中由水电离产生的c(H+) =_ _________ __。
查看答案和解析>>
科目:高中化学 来源:2015-2016年湖南湘潭、岳阳两校高二上第三次联考化学卷(解析版) 题型:选择题
下列有关平衡常数的说法正确的是
A. 温度越高,K值越大 B. K值越大,正反应速率越大
C. K值的大小与起始浓度有关 D. K值越大,反应物的转化率越大
查看答案和解析>>
科目:高中化学 来源:2015-2016年江西省高二上12月月考化学试卷(解析版) 题型:选择题
海水总量极大.金,铀等微量元素在海水中的总量自然也大,但从海水中获取这些微量元素的成本很高.其中成本最高的步骤在于
A.从海水中富集含微量元素的化合物 B.使含微量元素的离子沉淀
C.对含微量元素的混合物进行提纯 D.从化合物中冶炼这些单质
查看答案和解析>>
科目:高中化学 来源:2015-2016年山西省高一上12月月考化学试卷(解析版) 题型:选择题
在t℃时,将a gNH3完全溶于水,得到V mL溶液,设该溶液密度为ρg•cm﹣3,质量分数为ω,其中含NH4+的物质的量为b moL。下列叙述中正确的是
A.溶质的质量分数为ω=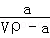 ×100%
×100%
B.溶质的物质的量浓度c=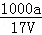 mol•L﹣1
mol•L﹣1
C.溶液中c (OH﹣)=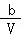 mol•L﹣1
mol•L﹣1
D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5ω
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com