
【题目】(1)某元素原子共有3个价电子,其中一个价电子位于第三能层![]() 能级,该能层有______个原子轨道,该元素基态原子的价电子排布图为______。
能级,该能层有______个原子轨道,该元素基态原子的价电子排布图为______。
(2)![]() 、
、![]() 均为短周期金属元素。依据下表数据,写出
均为短周期金属元素。依据下表数据,写出![]() 原子的核外电子排布式:______。
原子的核外电子排布式:______。
电离能/ |
|
|
|
|
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
科目:高中化学 来源: 题型:
【题目】在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时即产生N2和水蒸气,并放出大量热。已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256kJ的热量。
(1)写出该反应的热化学方程式____。
(2)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是__。
(3)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1
CH3OCH3(g)+H2O(g)===2CH3OH(g) ΔH2=+23.4kJ·mol-1
则2CO2(g)+6H2(g)===CH3OCH3(g)+3H2O(g) ΔH3=____kJ·mol-1
(4)用离子方程式表示碳酸钠溶液显碱性的原因:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据原子结构、元素周期表和元素周期律的知识回答下列问题:
①X是1~36号元素原子核外电子排布中未成对电子数最多的元素,X元素的名称是___,在元素周期表中的位置是___,位于周期表___区。。
②C、N、O、F四种元素第一电离能由大到小的顺序为___。
(2)早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
①基态铜原子的电子排布式为___。
②CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是___;Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___个铜原子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计能够成功的是( )
选项 | 实验目的 | 实验步骤及现象 |
A | 检验亚硫酸钠试样是否变质 | 试样 |
B | 检验某盐是否为铵盐 | 试样 |
C | 证明酸性条件下H2O2氧化性比I2强 | NaI溶液 |
D | 除去硝酸钾晶体中少量氯化钠 | 试样 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌-空气电池适宜用作城市电动车的动力电源。该电池放电时Zn转化为ZnO。该电池工作时,下列说法正确的是

A. 电池工作时溶液中的OH-向石墨电极移动
B. Zn电极发生了氧化还原反应
C. 电子经过溶液移向石墨电极
D. 锌电极的电极反应式:Zn + 2OH--2e- = ZnO + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配位化合物在生产生活中有重要应用,请根据要求回答下列问题:
(1)光谱证实单质铝与强碱性溶液反应有![]() 生成,则
生成,则![]() 中存在__________(填序号)
中存在__________(填序号)
a.共价键 b.非极性键 c.配位键 d.![]() 键 e.π键
键 e.π键
(2)![]() 可形成两种钴的配合物,已知
可形成两种钴的配合物,已知![]() 的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加
的配位数是6,为确定钴的配合物的结构,现对两种配合物进行了如下实验:在第一种配合物的溶液中加![]() 溶液时,产生白色沉淀,在第二种配合物的溶液中加
溶液时,产生白色沉淀,在第二种配合物的溶液中加![]() 溶液时,则无明显现象。则第一种配合物的结构可表示为____________________,第二种配合物的结构可表示为____________________。若在第二种配合物的溶液中滴加
溶液时,则无明显现象。则第一种配合物的结构可表示为____________________,第二种配合物的结构可表示为____________________。若在第二种配合物的溶液中滴加![]() 溶液,则产生的现象是____________________。(提示:
溶液,则产生的现象是____________________。(提示:![]() 这种配合物的结构可表示为
这种配合物的结构可表示为![]() 。)
。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学——选修3:物质结构与性质)
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均小于30)。A的基态原子2p能级有3个单电子;C的基态原子2p能级有1个单电子;E原子最外层有1个单电子,其次外层有3个能级且均排满电子;D与E同周期,价电子数为2。则:
(1)B元素的氢化物的沸点是同族元素氢化物中最高的,原因是__________________。
(2)A、B、C 三种元素的氢化物稳定性由强到弱的顺序为_________(用化学式表示)。
(3)A的最简单氢化物分子的空间构型为_______,其中A原子的杂化类型是________。
(4)A的单质中δ键的个数为_______________,π键的个数为_______________。
(5)写出基态E原子的价电子排布式:__________________________。
(6)C和D形成的化合物的晶胞结构如图所示,已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,求晶胞边长a =________cm。(用ρ、NA的计算式表示)
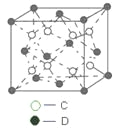
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中的有害气体主要有NO、碳氢化合物及CO,某校同学设计实验将模拟汽车尾气转化为无害气体。回答下列问题;

(1)为了配制模拟尾气,甲组同学用上图所示装置分别制备NO、乙烯及CO三袋气体。
①用装置A制取NO,分液漏斗中盛放的是___(填试剂名称)。
②用 (乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为______(磷转化为Na3 PO4)。
(乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为______(磷转化为Na3 PO4)。
③用H2 C2 O4与浓硫酸制取CO(化学方程式为H2C2O4 ![]() CO+CO2+H2O并提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为___→g(气流从左至右),其中装置D中盛放的药品是___
CO+CO2+H2O并提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为___→g(气流从左至右),其中装置D中盛放的药品是___
(2)乙组同学将甲组制得的气体与空气按适当比例混合形成模拟尾气(NO,CO,C2 H4及空气),按如图所示 装置进行尾气转化并检验。

①为检验催化反应后的气体中是否有CO2生成和乙烯的残留,G、H中盛放的试剂依次是_________(填标号)。
a. NaOH溶液 b.酸性KMnO4溶液
c.澄清石灰水 d. Br2/CCl4溶液
②通“模拟尾气”前,需先将催化剂加热到反应所需的温度,其目的是___;写出其中CO与NO完全转化为无害气体的化学方程式:___
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com