
科目:高中化学 来源:2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷(解析版) 题型:选择题
在下列变化过程中,被破坏的作用力正确的是()
A. 干冰升华——共价键 B. 氯化钠固体溶解——范德华力
C. 氢氧化钠熔融——离子键、共价键 D. 硫酸氢钠溶于水——离子键、共价键
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高二下学期第一次阶段性考试化学试卷(解析版) 题型:选择题
由两种气态烃组成的混和烃的总物质的量与该混和烃充分燃烧后,所得气体产物(二氧化碳和水蒸气)的物质的量的变化关系如图所示;以下对混和烃组成的判断中正确的是( )
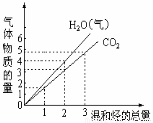
A. 一定有乙烯
B. 一定有乙烷
C. 一定有甲烷
D. 一定有丙烷
查看答案和解析>>
科目:高中化学 来源:2017届贵州省凯里市高三3月联考理综化学试卷(解析版) 题型:选择题
乙烯催化氧化成乙醛可设计成如图所示的燃料电池,其总反应为:2CH2=CH2+O2→2CH3CHO。下列有关说法正确的是

A.该装置能量转化形式是电能转化为化学能
B.负极反应式为:CH2=CH2-2e-+H2O=CH3CHO +2H+
C.每有0.1 mol O2反应,则向负极迁移的H+的物质的量为0.4 mol
D.电子移动方向:电极a→磷酸溶液→电极b
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省北校高一3月月考化学试卷(解析版) 题型:填空题
试分析下列各种情况下微粒间作用力的变化情况(填“离子键”“极性键”“非极性键”或“分子间作用力”):
(1)NaCl溶于水时破坏___________________________________;
(2)HCl溶于水时破坏____________________________________;
(3)SO2溶于水时破坏____________________________________;
(4)酒精溶于水时破坏____________________________________;
(5)NaOH和HCl反应时形成_______和_______;
(6)反应2H2+O2=2H2O中,被破坏的是________,形成的是________;
(7)CaCl2和Na2CO3反应时,被破坏的化学键有________,形成的化学键有________;
(8)Na2O熔化时被破坏的是________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省北校高一3月月考化学试卷(解析版) 题型:选择题
W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比是7:17;X与W同主族;Y的原子序数是W和X的原子序数之和的一半;含Z元素的物质焰色反应为黄色。下列判断正确的是( )
A. 金属性:Y>Z
B. 氢化物的沸点:X>W
C. 离子的还原性:X>W
D. 原子及离子的半径:Z>Y>X
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省北校高一3月月考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A. 非极性键只存在于双原子单质分子里
B. 由非金属元素组成的化合物不一定是共价化合物
C. 由于H-O键比H-S 键牢固,所以水的熔沸点比H2S高
D. 在由分子构成的物质中,分子间作用力越大,该物质越稳定
查看答案和解析>>
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(二)化学试卷(解析版) 题型:选择题
某有机物是一种医药中间体.其结构简式如图所示。下列有关该物质的说法正确的是( )

A. 该化合物分子中不含手性碳原子
B. 该化合物与NaHCO3溶液作用有CO2气体放出
C. 1 mol该化合物与足量溴水反应,消耗2 mol Br2
D. 在一定条件下,该化合物与HCHO能发生缩聚反应
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古包头市高三下学期第一次模拟考试理综化学试卷(解析版) 题型:简答题
利用锌锰干电池内的黑色固体水浸后的碳包滤渣(含MnO2、C、Hg2+等)制取MnSO4 • H2O 的实验流程如下:

已知:25℃时,几种硫化物的溶度积常数如下:
物质 | FeS | MnS | HgS |
溶度积 | 5.0×l0-18 | 4.6×l0-14 | 2.2×l0-54 |
25℃时,部分金属阳离子以氢氧化物形式沉淀时溶液的pH如下表所示:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
开始沉淀的pH | 2.7 | 7.6 | 8.3 |
完全沉淀的pH | 3.7 | 9.7 | 9.8 |
(1)上述流程中,蒸发实验操作时用到的硅酸盐材质的仪器有______________。
(2)在加热条件下“浸取”,其原因是__________________;浸取时生成MnSO4和Fe2(SO4)3的化学方程式为__________________________。
(3)滤渣I的成分为MnO2、C和____________(填化学式);若浸取反应在25℃时进行,FeS足量,则充分浸取后溶液中的c(Hg2+)/C(Fe2+)= ____________(填数值)。
(4)“氧化”时的离子方程式为____________;氧化时可用H2O2代替MnO2,H2O2的电子式为_______。
(5)中和时,应该调节溶液pH的范围到____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com