��2013?ͨ������ģ��̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��
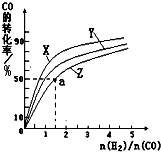
��1����CO
2�뽹̿��������CO��CO�����������ȣ�
����֪��Fe
2O
3��s��+3C��ʯī��=2Fe��s��+3CO��g����H
1=+489.0kJ/mol
C��ʯī��+CO
2��g��=2CO��g����H
2=+172.5kJ/mol
��CO��ԭFe
2O
3���Ȼ�ѧ����ʽΪ
Fe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H=-28.5kJ/mol
Fe2O3��s��+3CO��g��=2Fe��s��+3CO2��g����H=-28.5kJ/mol
��
���Ȼ��٣�PdCl
2����Һ����Ӧ���ڼ���������CO��PdCl
2����ԭ�ɵ��ʣ���Ӧ�Ļ�ѧ����ʽΪ
PdCl2+CO+H2O=Pd+CO2+2HCl
PdCl2+CO+H2O=Pd+CO2+2HCl
��
��2��������ʯī�缫����KOH��Һ�У��������ֱ�ͨ��C
3H
8��O
2���ɱ���ȼ�ϵ�أ�
�ٸ����缫��Ӧʽ�ǣ�
C3H8-20e-+26OH-=3CO32-+17H2O
C3H8-20e-+26OH-=3CO32-+17H2O
��
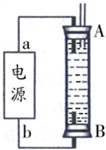
��ijͬѧ���ñ���ȼ�ϵ�������һ�ֵ�ⷨ��ȡFe��OH��
2��ʵ��װ�ã���ͼ��ʾ����ͨ�����Һ�в��������İ�ɫ�������ҽϳ�ʱ�䲻��ɫ������˵������ȷ����
ABD
ABD
������ţ�
A����Դ�е�aһ��Ϊ������bһ��Ϊ����
B��������NaCl��Һ��Ϊ���Һ
C��A��B���˶������������缫
D�����������ķ�Ӧ�ǣ�2H
++2e
-=H
2��
��3������ͬ����CO��g����H
2O��g���ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У����з�Ӧ��
CO��g��+H
2O��g��?CO
2��g��+H
2��g�����õ������������ݣ�
| ʵ���� |
�¶�/�� |
��ʼ��/mol |
ƽ����/mol |
�ﵽƽ������ʱ��/min |
| H2O |
CO |
CO2 |
| 1 |
650 |
2 |
4 |
1.6 |
5 |
| 2 |
900 |
1 |
2 |
0.4 |
3 |
| 3 |
900 |
1 |
2 |
0.4 |
1 |
�ٸ÷�Ӧ������ӦΪ
����
����
��������š����ȷ�Ӧ��
��ʵ��2�У�ƽ�ⳣ��K=
��
��ʵ��3��ʵ��2��ȣ��ı������������
ʹ���˴������Ӵ���ѹǿ
ʹ���˴������Ӵ���ѹǿ
����һ��������ɣ���
��4����2.4g̼������������ȼ�գ���������ͨ��100mL 3.0mol/L������������Һ�У���ȫ���պ���Һ���������ӵ����ʵ���Ũ���ɴ�С��˳��
c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+��
c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+��
��

 ̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��
̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��

 ��У����ϵ�д�
��У����ϵ�д�
 ��2013?ͨ������ģ��̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��
��2013?ͨ������ģ��̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��