
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
科目:高中化学 来源: 题型:
【题目】由 Al、CuO、Fe2O3 组成的混合物共 10.0g,放入 500mL 某浓度盐酸溶液中,混合物完全溶解,当再 加入 250mL 2.0mol/L 的 NaOH 溶液时,得到的沉淀最多。该盐酸的浓度为( )
A. 0.5 mol/L B. 3.0 mol/L C. 1.0 mol/L D. 2.0 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:
![]()
资料:TiCl4及所含杂质氯化物的性质
化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
熔点/℃ | 69 | 25 | 193 | 304 | 714 |
在TiCl4中的溶解性 | 互溶 | —— | 微溶 | 难溶 | |
(1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行。
已知:TiO2(s)+2 Cl2(g)= TiCl4(g)+ O2(g) ΔH1=+175.4 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH2=-220.9 kJ·mol-1
① 沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:____________________。
② 氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的ΔH_____0(填“>”“<”或“=”),判断依据:_______________。

③ 氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是__________________________。
④ 氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有_____________。
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4。示意图如下:

物质a是______________,T2应控制在_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.76克铜镁合金完全溶解于50mL、密度为1.400g/cm3、质量分数为63%的浓硝酸中,得到NO2气体1792mL(标准状况),向反应后的溶液中加入适量的1.0mol/LNaOH溶液,恰使溶液中的金属离子全部沉淀。下列说法不正确的是( )
A. 该浓硝酸中HNO3的物质的量浓度是14.0mol/L
B. 加入NaOH溶液的体积是50mL
C. 浓硝酸在与合金反应中起了酸性和氧化性的双重作用,且起氧化性的硝酸的物质的量为0.08 mol
D. 得到的金属氢氧化物的沉淀为3.12克
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应: MnO2 +4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O。将一定质量的二氧化锰溶解在过量的浓盐酸中,反应一段时间后生成标准状况下氯气4.48 L (假设反应前后溶液体积不变)。试回答下列问题:
MnCl2 + Cl2↑+ 2H2O。将一定质量的二氧化锰溶解在过量的浓盐酸中,反应一段时间后生成标准状况下氯气4.48 L (假设反应前后溶液体积不变)。试回答下列问题:
(1)用单线桥法标明该反应中电子转移的方向和数目:______
MnO2 +4HCl(浓) ![]() MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
(2)计算反应消耗的MnO2的质量______ ;
(3)计算被氧化的HCl物质的量______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。生产流程如图1:
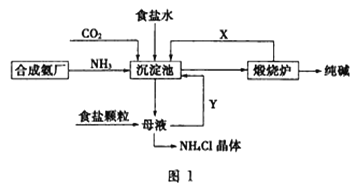
(1)完成有关反应的化学方程式
①沉淀池:NH3+CO2+H2O+NaCl=NaHCO3+NH4Cl
②煅烧炉:_______________。
(2)联合制碱法的优点表述中,不正确的是_______。
A.生产原料为:食盐、NH3、CO2
B.副产物氯化铵可做氮肥
C.生产过程中可循环利用的物质只有CO2
D.原料利用率高
某实验小组,利用下列装置图2模拟“联合制碱法”的第一步反应。
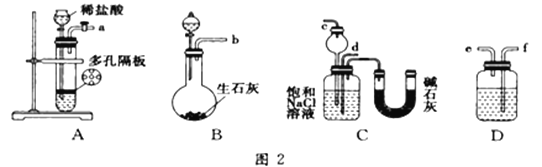
(3)上述装置中接口连接顺序为______。
A.a接c;b接f、e接d B.a接d;b接f、e接c
C.b接d;a接e、f接c D.b接c;a接f、e接d
(4)D中应选用的液体为______________。为测定产品纯碱的成分和含量,做如下实验,假设产品纯碱中只含NaCI、NaHCO3杂质。
(5)检验产品纯碱中是否含有NaCl,可取少量试样溶于水后,再滴加___________试剂。
(6)滴定法测定纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用cmol/L的HCI溶液滴定至溶液由红色变为无色(指示CO32-+H+=HCO3-反应的终点),所用HCI 溶液体积为V1mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄色变为橙色,所用HCI溶液总体积为V2mL,则纯碱样品中NaHCO3质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是()。
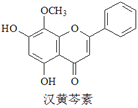
A. 汉黄芩素的分子式为C16H13O5
B. 该物质遇FeCl3溶液显色
C. 1 mol该物质与溴水反应,最多消耗1 mol Br2
D. 与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用16mol/L 浓硫酸配制100mL 2.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积②量取一定体积的浓硫酸③溶解 ④转移、洗涤 ⑤定容 ⑥摇匀。回答下列问题
(1)该实验所需的玻璃仪器:___________、玻璃棒、烧杯、胶头滴管、量筒。
(2)所需浓硫酸的体积是______,量取浓硫酸所用的量筒的规格是_______(规格从下列中选用 A.10mL B.20mL C.50mL D.100mL)
(3)第⑤步定容的具体实验操作是_______________________________________________。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏水洗涤后残留有少量的水__________。
B.转移溶液前未冷却至室温____________。
C.定容时仰视溶液的凹液面____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某铜和氧化铜的混合物中铜元素的质量分数,某同学设计了如图所示实验装置。

回答下列问题:
(1))装置A中盛装盐酸的仪器的名称为____________。
(2)实验时装置A中可观察到的现象________________________________________ ;发生反应的离子方程式为__________________________________________________。
(3)装置B的作用是_______________________________________________________。
(4)在加热装置D之前,应该进行的一步操作是________________________________,目的是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com