
ЁОЬтФПЁПвбжЊAЪЧвЛжжЕЛЦЩЋЙЬЬхЃЌПЩзіЙЉбѕМСЃЌCЮЊОпгаДХадЕФКкЩЋОЇЬхЃЌEЕФбцЩЋЗДгІЮЊЛЦЩЋЃЌFЮЊКьКжЩЋЙЬЬхЃЈВПЗжВњЮявбТдШЅЃЉЁЃ
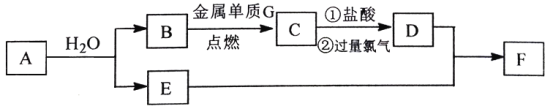
ЃЈ1ЃЉЮяжЪAЁЂFЕФЛЏбЇЪНЗжБ№ЪЧ_____________ЁЂ_____________ЁЃ
ЃЈ2ЃЉCЁњDЕФЙ§ГЬжаЕкЂкВНЗДгІЕФРызгЗНГЬЪНЪЧ____________________________________ЁЃ
ЃЈ3ЃЉШчКЮМьбщDжаЕФН№ЪєбєРызгЃЌЫЕУїОпЬхЕФВйзїКЭЪЕбщЯжЯѓ________________________ЁЃ
ЃЈ4ЃЉEШмвКгыЕиПЧжаКЌСПзюЖрЕФН№ЪєдЊЫиЕФЕЅжЪЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊ______________ЁЃ
ЃЈ5ЃЉGгыDШмвКвВФмЗЂЩњЗДгІЃЌЦфЗДгІЕФРраЭЮЊ___________________ЃЈЬюађКХЃЉЁЃ
a.ЛЏКЯЗДгІ b.жУЛЛЗДгІ c.ИДЗжНтЗДгІ d.бѕЛЏЛЙдЗДгІ
ЁОД№АИЁПNa2O2 Fe(OH)3 2Fe2+ЃЋCl2=2Fe3+ЃЋ2ClЃ ШЁЩйСПDШмвКгкЪдЙмжаЃЌЕЮМгKSCNШмвКЃЌШмвКЯдбЊКьЩЋЃЈЦфЫќКЯРэД№АИвВЕУЗж 2AlЃЋ2NaOHЃЋ2H2OЃН2NaAlO2ЃЋ3H2Ёќ ad
ЁОНтЮіЁП
вбжЊAЪЧвЛжжЕЛЦЩЋЙЬЬхЃЌПЩзіЙЉбѕМСЃЌгІЮЊNa2O2ЃЌCЮЊОпгаДХадЕФКкЩЋОЇЬхЃЌгІЮЊFe3O4ЃЌEЕФбцЩЋЗДгІЮЊЛЦЩЋЃЌдђгЩзЊЛЏЙиЯЕПЩжЊEЮЊNaOHЃЌBЮЊO2ЃЌDЮЊFeCl3ЃЌFЮЊКьКжЩЋЙЬЬхЃЌгІЮЊFe(OH)3ЃЌвдДЫНтД№ИУЬтЁЃ
ЃЈ1ЃЉгЩвдЩЯЗжЮіПЩжЊAЮЊNa2O2 ЃЌFЮЊFe(OH)3 ЃЌЙЪД№АИЮЊЃКNa2O2 ЃЛ Fe(OH)3 ЃЛ
ЃЈ2ЃЉCЁњDЕФЙ§ГЬжаЕкЂкВНЗДгІЕФРызгЗНГЬЪНЪЧ2Fe2++Cl2=2Fe3++2Cl-ЃЛ
ЃЈ3ЃЉDЮЊFeCl3ЃЌбєРызгЮЊЬњРызгЃЌМьбщЬњРызгЃЌПЩШЁЩйСПDШмвКгкЪдЙмжаЃЌЕЮМгKSCNШмвКЃЌПЩЙлВьЕНШмвКЯдбЊКьЩЋЃЌЙЪД№АИЮЊЃКШЁЩйСПDШмвКгкЪдЙмжаЃЌЕЮМгKSCNШмвКЃЌШмвКЯдбЊКьЩЋЃЛ
ЃЈ4ЃЉЕиПЧжаКЌСПзюЖрЕФН№ЪєЮЊТСЃЌгыЧтбѕЛЏФЦЗДгІЕФЗНГЬЪНЮЊ2Al+2NaOH+2H2O=2NaAlO2+3H2ЁќЃЛ
ЃЈ5ЃЉЬњгыТШЛЏЬњЗДгІЩњГЩТШЛЏбЧЬњЃЌЮЊЛЏКЯЗДгІКЭбѕЛЏЛЙдЗДгІЃЌЙЪД№АИЮЊЃКadЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгУжЪСПЗжЪ§ЮЊ36.5%ЕФХЈбЮЫс(УмЖШЮЊ1.16 gЁЄcmЃ3)ХфжЦГЩ1 molЁЄLЃ1ЕФЯЁбЮЫсЁЃЯжЪЕбщЪвНіашвЊетжжбЮЫс220 mLЃЌЪдЛиД№ЯТСаЮЪЬтЃК
(1)ХфжЦЯЁбЮЫсЪБЃЌгІбЁгУШнСПЮЊ________mLЕФШнСПЦПЁЃ
(2)дкСПШЁХЈбЮЫсЪБвЫбЁгУЯТСаСПЭВжаЕФ________ЁЃ
AЃЎ5 mL BЃЎ10 mL CЃЎ25 mL DЃЎ50 mL
(3)дкСПШЁХЈбЮЫсКѓЃЌНјааСЫЯТСаВйзїЃК(НЋВйзїВЙГфЭъећ)
ЂйЕШЯЁЪЭЕФбЮЫсЕФЮТЖШгыЪвЮТвЛжТКѓЃЌбиВЃСЇАєзЂШыШнСПЦПжаЁЃ
ЂкЭљШнСПЦПжааЁаФМгеєСѓЫЎжСвКУцРыШнСПЦППЬЖШЯп1ЁЋ2 cmЪБЃЌИФгУНКЭЗЕЮЙмМгеєСѓЫЎЃЌ____________________________________________ЁЃ
ЂлдкЪЂбЮЫсЕФЩеБжазЂШыеєСѓЫЎЃЌВЂгУВЃСЇАєНСЖЏЃЌЪЙЦфЛьКЯОљдШЁЃ
ЂмгУеєСѓЫЎЯДЕгЩеБКЭВЃСЇАє2ЁЋ3ДЮЃЌВЂНЋЯДЕгвКШЋВПзЂШыШнСПЦПЁЃ
ЩЯЪіВйзїжаЃЌе§ШЗЕФЫГађЪЧ(ЬюађКХ)________ЁЃ
(4)ШєгУ1mol/L HClШмвКШѓЯДШнСПЦПЃЌдйзЊвЦШмвКЃЌЫљХфжУЕФШмвКХЈЖШНЋ_________(ЬюЁАЦЋДѓЁБЁАЦЋаЁЁБЛђЁАЮогАЯьЁБ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯђHClЁЂAlCl3ЛьКЯШмвКжаж№ЕЮМгШыNaOHШмвКЃЌЩњГЩГСЕэЕФСПЫцNaOHШмвКМгШыСПЕФБфЛЏЙиЯЕШчЭМЫљЪОЃЌдђЯТСаРызгзщдкЖдгІЕФШмвКжавЛЖЈФмДѓСПЙВДцЕФЪЧЃЈ ЃЉ

A. MЕуЖдгІЕФШмвКжаЃКK+ЁЂFe2+ЁЂSO42-ЁЂNO3-
B. NЕуЖдгІЕФШмвКжаЃКK+ЁЂNH4+ЁЂCl-ЁЂCO32-
C. SЕуЖдгІЕФШмвКжаЃКNa+ЁЂSO42-ЁЂHCO3-ЁЂNO3-
D. RЕуЖдгІЕФШмвКжаЃКNa+ЁЂSO42-ЁЂCl-ЁЂNO3-
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаРызгЗНГЬЪНжаЃЌВЛе§ШЗЕФЪЧ
A.Й§СПCO2ЦјЬхЭЈШыNaOHШмвКжаЃКCO2+OHЃ=HCO3Ѓ
B.НЋТШЦјЭЈШыЫЎжаЃКCl2+H2O![]() ClЃ+ClOЃ+2HЃЋ
ClЃ+ClOЃ+2HЃЋ
C.ЯђSiO2ЗлФЉжаМгШызуСПЕФNaOHШмвКЃКSiO2+2OHЃ= SiO32Ѓ+ H2O
D.гУТШЛЏЬњШмвКИЏЪДЭЃЌжЦзїгЁЫЂЕчТЗАхЃК2Fe3ЃЋ+Cu=2Fe2ЃЋ+Cu2ЃЋ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПШчЭМ(EaБэЪОЛюЛЏФм)ЪЧCH4гыCl2ЩњГЩCH3ClЕФВПЗжЗДгІЙ§ГЬжаИїЮяжЪЮяжЪЕФФмСПБфЛЏЙиЯЕЭМЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧЃЈ ЃЉ
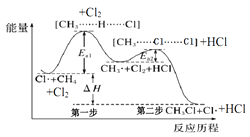
A.ClЁЄПЩгЩCl2дкИпЮТЬѕМўЯТЩњГЩЃЌЪЧCH4гыCl2ЗДгІЕФДпЛЏМС
B.Щ§ИпЮТЖШЃЌEa1ЁЂEa2ОљМѕаЁЃЌЗДгІЫйТЪМгПь
C.діДѓCl2ЕФХЈЖШЃЌПЩЬсИпЗДгІЫйТЪЃЌЕЋВЛгАЯьЁїHЕФДѓаЁ
D.ЕквЛВНЗДгІЕФЫйТЪДѓгкЕкЖўВНЗДгІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЪжЛњЕчГиВЩгУСЫЪЏФЋЯЉЕчГиЃЌПЩГфЕч5ЗжжгЃЌЭЈЛА2аЁЪБЁЃвЛжжЪЏФЋЯЉяЎСђЕчГи(2Li+S8=Li2S8)ЙЄзїдРэЪОвтЭМШчЭМЁЃЯТСагаЙиИУЕчГиЫЕЗЈе§ШЗЕФЪЧ
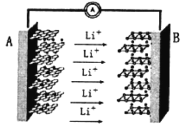
A.AЕчМЋЮЊИУЕчдДЕФИКМЋЃЌЕчМЋВФСЯжївЊЪЧН№ЪєяЎКЭЪЏФЋЯЉ
B.BЕчМЋЕФЗДгІЃК2Li++S8Љ2e=Li2S8
C.ГфЕчЪБЃЌЕчМЋAгыЕчдДИКМЋСЌНгЃЌзїЮЊвѕМЋ
D.ЮЊЬсИпЕчГиаЇТЪЃЌИУЕчГиПЩбЁгУЯЁСђЫсзїЮЊЕчНтжЪ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПжмЦкБэЧАЫФжмЦкЕФдЊЫи![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЁЂ
ЁЂ![]() ЃЌдзгађЪ§вРДЮдіДѓЃЌXдзгЛљЬЌЪБ
ЃЌдзгађЪ§вРДЮдіДѓЃЌXдзгЛљЬЌЪБ![]() Вужа
Вужа![]() ЙьЕРЕчзгЪ§гыsЙьЕРЕчзгЪ§ЯрЭЌЃЛ
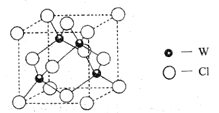
ЙьЕРЕчзгЪ§гыsЙьЕРЕчзгЪ§ЯрЭЌЃЛ![]() дзгЛљЬЌЪБ2pдзгЙьЕРЩЯга3ИіЮДГЩЖдЕФЕчзгЃЛZгаЖржжбѕЛЏЮяЃЌЦфжавЛжжКьзиЩЋбѕЛЏЮяПЩзїЭПСЯЃЛ
дзгЛљЬЌЪБ2pдзгЙьЕРЩЯга3ИіЮДГЩЖдЕФЕчзгЃЛZгаЖржжбѕЛЏЮяЃЌЦфжавЛжжКьзиЩЋбѕЛЏЮяПЩзїЭПСЯЃЛ![]() ЮЛгкЕкЫФжмЦкЃЌЦфдзгзюЭтВужЛга1ИіЕчзгЃЌЧвФкВуЖМДІгкШЋГфТњзДЬЌЁЃЛиД№ЯТСаЮЪЬтЃК
ЮЛгкЕкЫФжмЦкЃЌЦфдзгзюЭтВужЛга1ИіЕчзгЃЌЧвФкВуЖМДІгкШЋГфТњзДЬЌЁЃЛиД№ЯТСаЮЪЬтЃК
(1)XЮЛгкжмЦкБэЕФЕк_______жмЦкЃЌЕк______зхЁЃ
(2)дЊЫиЕФЕквЛЕчРыФмЃКX______Y(ЬюЁАЃОЁБЛђЁАЃМЁБЃЌЯТЭЌ)ЃЛдзгАыОЖЃКX______YЁЃ
(3)![]() ЕФзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяжаЫсИљРызгЕФПеМфЙЙаЭЪЧ_______(гУЮФзжУшЪі)ЁЃ
ЕФзюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяжаЫсИљРызгЕФПеМфЙЙаЭЪЧ_______(гУЮФзжУшЪі)ЁЃ
(4)![]() ЛљЬЌКЫЭтЕчзгХХВМЪНЮЊ_________ЃЌгУЬњЧшЛЏМиШмвКМьбщ
ЛљЬЌКЫЭтЕчзгХХВМЪНЮЊ_________ЃЌгУЬњЧшЛЏМиШмвКМьбщ![]() ЕФРызгЗНГЬЪНЮЊ___________ЁЃ
ЕФРызгЗНГЬЪНЮЊ___________ЁЃ
(5)дЊЫиWЕФвЛжжТШЛЏЮяОЇЬхЕФОЇАћНсЙЙШчЭМЫљЪОЃЌИУТШЛЏЮяЕФЛЏбЇЪНЪЧ_______ЃЌЫќПЩгыХЈбЮЫсЗЂЩњЗЧбѕЛЏЛЙдЗДгІЃЌЩњГЩХфКЯЮя![]() ЃЌЗДгІЕФЛЏбЇЗНГЬЪНЃК_________ЁЃ
ЃЌЗДгІЕФЛЏбЇЗНГЬЪНЃК_________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЛЏКЯЮяHЪЧвЛжжгаЛњЙтЕчВФСЯжаМфЬхЁЃЪЕбщЪвгЩЗМЯуЛЏКЯЮяAжЦБИHЕФвЛжжКЯГЩТЗЯпШчЯТЃК
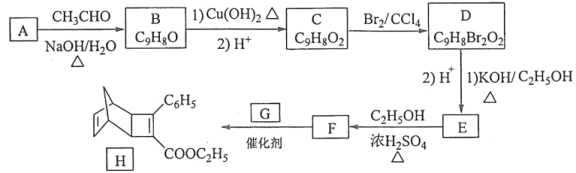
вбжЊЃК
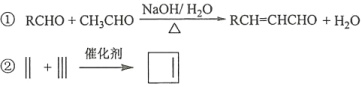
ЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉAЕФЛЏбЇУћГЦЪЧ__________ЁЃ
ЃЈ2ЃЉгЩCЩњГЩDКЭEЩњГЩFЕФЗДгІРраЭЗжБ№ЪЧ__________ЁЂ_________ЁЃ
ЃЈ3ЃЉEЕФНсЙЙМђЪНЮЊ____________ЁЃ
ЃЈ4ЃЉGЮЊМзБНЕФЭЌЗжвьЙЙЬхЃЌгЩFЩњГЩHЕФЛЏбЇЗНГЬЪНЮЊ___________ЁЃ
ЃЈ5ЃЉЗМЯуЛЏКЯЮяXЪЧFЕФЭЌЗжвьЙЙЬхЃЌXФмгыБЅКЭЬМЫсЧтФЦШмвКЗДгІЗХГіCO2ЃЌЦфКЫДХЙВеёЧтЦзЯдЪОга4жжВЛЭЌЛЏбЇЛЗОГЕФЧтЃЌЗхУцЛ§БШЮЊ6ЁУ2ЁУ1ЁУ1ЃЌаДГі2жжЗћКЯвЊЧѓЕФXЕФНсЙЙМђЪН____________ЁЃ
ЃЈ6ЃЉаДГігУЛЗЮьЭщКЭ2ЈCЖЁШВЮЊдСЯжЦБИЛЏКЯЮя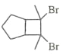 ЕФКЯГЩТЗЯп________ЃЈЦфЫћЪдМСШЮбЁЃЉЁЃ
ЕФКЯГЩТЗЯп________ЃЈЦфЫћЪдМСШЮбЁЃЉЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдквЛЖЈЮТЖШЯТЃЌЯђвЛИі2 LЕФецПеУмБеШнЦїжа(дЄЯШзАШыДпЛЏМС)ЭЈШы1 mol N2КЭ3 mol H2ЃЌОЙ§вЛЖЮЪБМфКѓЃЌВтЕУШнЦїФкбЙЧПЪЧЦ№ЪМЪБЕФ0.9БЖЁЃдкДЫЪБМфЖЮФкH2ЕФЦНОљЗДгІЫйТЪЮЊ0.1 molЁЄLЃ1ЁЄminЃ1ЃЌдђОЙ§ЪБМфЮЊ( ЁЁЁЁ)
A. 2 minB. 3 minC. 4 minD. 5 min
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com