
【题目】乙醇(C2H5OH)燃料电池是一种新型电池,其中采用质子(H+)溶剂,在200℃左右时供电,电池总反应为C2H5OH+3O2=2CO2+3H2O,该电池的工作原理如图所示。下列说法正确的是( )
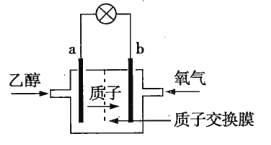
A.通入乙醇的a电极是正极
B..氧气在b电极上发生氧化反应
C.电池工作时,质子向电池的负极迁移
D.电池工作时,电流由b极沿导线流向a极
科目:高中化学 来源: 题型:
【题目】下列事实可以证明一水合氨是弱电解质的是
①室温下,![]() 的氨水可以使酚酞试液变红②室温下,
的氨水可以使酚酞试液变红②室温下,![]() 的氯化铵溶液的PH约为5
的氯化铵溶液的PH约为5
③在相同条件下,氨水溶液的导电性比强碱溶液弱④铵盐受热易分解
A. ①② B. ②③ C. ③④ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K时,将20mL3xmol·L-1Na3AsO3、20mL3xmol·L-1I2和20mLNaOH溶液混合,发生反应:AsO33-(aq)+I2(aq)+2OH-(aq)![]() AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43- 与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是
AsO43-(aq)+2I-(aq)+H2O(l),溶液中c(AsO43- 与反应时间(t)的关系如图所示。下列不能判断反应达到平衡的是

A. 溶液的pH不再变化
B. 2v正(I-)=v逆(AsO33-)
C. c(AsO43-)/c(AsO33-)不再变化
D. c(I-)=2ymol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25 ℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol·L-1 HF溶液中加入1 L 0.2 mol·L-1 CaCl2溶液,则下列说法中正确的是
A.25 ℃时,0.1 mol·L-1 HF溶液中pH=1B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中有CaF2沉淀产生D.该体系中,Ksp(CaF2)=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为相互串联的甲、乙两电解池,其中甲池为电解精炼铜的装置。

试回答下列问题:
(1)A是________极,材料是________,电极反应为_____________,B是________极,材料是________,主要电极反应为_________________,电解质溶液为________。
(2)乙池中若滴入少量酚酞溶液,电解一段时间后Fe极附近溶液呈________色。
(3)常温下,若甲池中阴极增重12.8 g,则乙池中阳极放出的气体在标准状况下的体积为________。若此时乙池剩余液体为400 mL,则电解后得到碱液的物质的量浓度为________,pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是(已知质子交换膜的作用是只允许H+通过)( )

A.该电池在高温下工作的速度更快
B.HS-在硫氧化菌作用下转化为SO42-的电极反应式为HS-+4H2O-8e-=SO42-+9H+
C.b电极是电池的负极
D.该电池工作时,H+向左通过质子交换膜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1887年,英国人赫勒森发明了最早的干电池,如今干电池已经发展成为一个庞大的家族,种类达100多种。应用广泛的是Zn—MnO2干电池,其电解质溶液是ZnCl2—NH4Cl混合溶液。电池工作一段时间后,电池内存在7种物质:NH3、Mn2O3、ZnCl2、MnO2、NH4Cl、Zn和H2O。请回答下列问题
(1)该电池的负极材料是__;电池工作时,电子流向__(填“正极”或“负极”,下同);放电时NH4+向___移动。
(2)该氧化还原反应的化学方程式为__,发生还原反应的物质是__,被氧化的元素是__。若有17.4g氧化剂参与反应,则电子转移数目为__NA(NA表示阿伏加德罗常数的值)。
(3)普通锌锰电池的缺点是电量小、放电电流弱。为增大放电电流,可把负极锌片改为锌粉,其理由是___。
(4)若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是__。欲除去Cu2+,最好选用下列试剂中的__(填序号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】杂志Joule中题为“Li—CO2 Electrochemistry:A New Strategy for CO2 Fixation and Energy Storage”的文章,阐述关于电化学技术固定CO2新的反应途径。下图是采用新能源储能器件将CO2转化为固体产物,实现CO2的固定和储能灵活应用的装置。储能器件使用的Li—CO2电池组成为钌电极/CO2—饱和LiClO4—DMSO电解液/锂片。下列说法错误的是
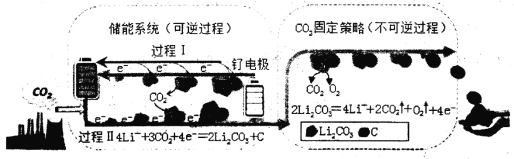
A.钌电极为负极,其电极反应式为:2Li2CO3+C—4e-=== 3CO2+4Li+
B.Li—CO2电池电解液由LiClO4—DMSO溶于水得到
C.这种电化学转化方式不仅减少CO2的排放,还可将CO2作为可再生能源载体
D.CO2的固定中,每生成1.5mol气体,可转移2mole-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】半胱氨酸是食品加工中最常用的“面团改良剂”,它可以促进面筋的形成。已知:α-氨基丙酸为![]() ;β-氨基丙酸为
;β-氨基丙酸为![]() 。回答下列问题:
。回答下列问题:
(1)半胱氨酸是一种含有一个硫氢基(—SH)的氨基酸,已知半胱氨酸分子中硫的质量分数为26.45%,其分子中硫氢基和氨基不在同一个碳原子上,硫氢基与半胱氨酸的β碳原子直接相连,则半胱氨酸的相对分子质量为__________,其结构简式为__________。
(2)半胱氨酸可以生成一种九肽,则这种九肽的分子式为__________。
(3)现有一种多肽的分子式为CxHyN12OmSn,将其完全水解只得到下面三种氨基酸:α-氨基丙酸、半胱氨酸、天门冬氨酸(![]() ),则将一个该多肽分子完全水解,得到的天门冬氨酸的数目为_________。
),则将一个该多肽分子完全水解,得到的天门冬氨酸的数目为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com