
用10.00ml 0.1mol/L的M(OH)y的碱溶液跟8.00ml0.25mol/LHxROn的酸溶液恰好完全中和,则x和y之比为
A.1∶1 B.1∶2 C.2∶1 D.3∶1
 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:阅读理解
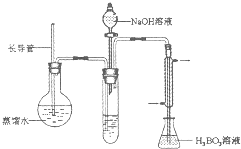
| 辅助试剂 |
| 加热 |
| NaOH溶液 |
| 吹出 |
| H3BO3 |
| 吸收 |
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积/mL |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 25.50 |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55 |
| 4 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 5 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 1.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
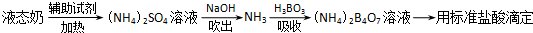
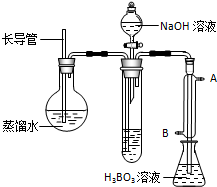
| 编号 | 样品和辅助试剂 | 消耗盐酸体积 |
| 1 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.45mL |
| 2 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.55mL |
| 3 | 10.00mL液态奶、0.2g催化剂、20mL浓硫酸 | 33.50mL |
| 4 | 10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸 | 1.50mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
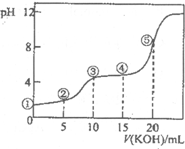 常温下,用0.10mol?L-1 KOH溶液滴定10.00ml 0.10mol?L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )
常温下,用0.10mol?L-1 KOH溶液滴定10.00ml 0.10mol?L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com