
将足量铁粉投入一定浓度的氯化铁和氯化铜的混合溶液中,充分反应后,溶液中剩余固体的质量与加人铁粉的质量相同,则原溶液中氯化铁和氯化铜的浓度之比为
A.2:7 B.3;4 C.4:7 D.2:3
科目:高中化学 来源:2016-2017学年宁夏省高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A. O2和O3互为同素异形体,性质相似
B. 常温下,PH=1的水溶液中,Na+、NO3-、HCO3-、Fe2+可以大量共存
C. 明矾和漂白粉用于自来水的净化和杀菌消毒,两者的作用原理相同
D. C(石墨,s)=C(金刚石,s);△H>0,所以石墨比金刚石稳定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省襄阳市高二3月月考化学试卷(解析版) 题型:选择题
下列装置(必要的夹持装置及石棉网已省略)或操作能达到实验目的的是( )
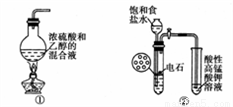
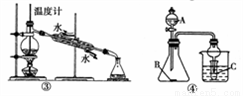
A. ①是实验室制乙烯
B. ②是实验室制乙炔并验证乙炔可以发生氧化反应
C. ③是实验室中分馏石油
D. ④中若A为稀硫酸,B为碳酸钠,C为硅酸钠溶液,验证硫酸、碳酸、硅酸酸性的强弱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一下学期第一次月考化学试卷(解析版) 题型:选择题
常温下, 下列各组物质中,Y既能与X反应又能与Z反应的是( )
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 稀盐酸 |
③ | O2 | N2 | H2 |
④ | FeCl3溶液 | Cu | 浓硝酸 |
A. ①③ B. ①④ C. ②④ D. ②③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一下学期第一次月考化学试卷(解析版) 题型:选择题
取x g铜镁合金完全溶于浓硝酸中,反应过程中硝酸被还原只产生8 960 mL的NO2气体和672 mL N2O4的气体(都已折算到标准状态),在反应后的溶液中加足量的氢氧化钠溶液,生成沉淀质量为17.02 g。则x等于( )
A.8.64 g B.9.20 g
C.9.00 g D.9.44 g
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省益阳市高一下学期3月月考化学试卷(解析版) 题型:计算题
把主族元素X的最高价氧化物X2O 4.7g溶于95.3g水中,得到溶质质量分数为5.6%的溶液,Y与X位于同一族,12gY的氢氧化物与400mL0.75
molL-1的盐酸完全中和,Z与Y同周期,标准状况下5.6L ZO2 为16g。则
(1)X的相对原子质量为__________________;
(2)Y的氧化物为_______化合物;
(3)Z的最高价氧化物的水化物化学式为____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省益阳市高一下学期3月月考化学试卷(解析版) 题型:选择题
57号镧元素(La)是一种活泼性比铁还强的金属元素,La的氧化物的化学式为La2O3,La(OH)3是不溶于水的碱,La的氯化物、硝酸盐均易溶于水,下列各组物质中不能直接反应得到LaCl3的是
A. La2O3+HCl B. La+Cl2 C. La (OH)3+HCl D. La(NO3)3+HCl
查看答案和解析>>
科目:高中化学 来源:2017届宁夏银川市高三下学期第一次模拟考试理综化学试卷(解析版) 题型:简答题
(1)甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g) + 2H2(g) CH3OH(g),在体积为1L的恒容密闭容器中,充人2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g),在体积为1L的恒容密闭容器中,充人2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到5min,用一氧化碳表示的平均反应速率v(CO)=______________
②下列说法正确的是___________(填字母序号)。
A.达到平衡时,H2的转化率为65%
B.5min后容器中混合气体的平均相对分子质量不再改变
C.达到平衡后,再充人氩气,反应速率减小
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)一定温度下,将NO2与SO2以体积比1:2置于密闭容器中发生反应NO2(g)+SO2(g) SO3(g)+NO(g) , 达到平衡时SO3的体积分数为25%。该反应的平衡常数K = _________。
SO3(g)+NO(g) , 达到平衡时SO3的体积分数为25%。该反应的平衡常数K = _________。
(3)碳与水蒸气反应制取H2的相关反应如下:
Ⅰ:C(s)+H2O(g)=CO(g)+H2(g) △H= +131.0kJ/molZiyuanku.com
Ⅱ:CO(g)+H2O(g)=CO2(g)+H2(g) △H= -43kJ/mol
Ⅲ:CaO(s)+CO2(g)=CaCO3(S) △H= -178.3kJ/mol
计算①反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g)的△H=_________kJ/mol;
CaCO3(s)+2H2(g)的△H=_________kJ/mol;
②对于可逆反应C(s)+2H2O(g)+CaO(s) CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是_________。(填字母)
CaCO3(s)+2H2(g),采取以下措施可以提高H2产率的是_________。(填字母)
A.降低体系的温度 B.压缩容器的体积
C.增加CaO的量 D.选用适当的催化剂
(4)甲醇作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。该电池的负极反应式为_________________。
(5)若往20 mL0.01mol/L的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如下图所示,下列有关说法正确的是________(填标号)
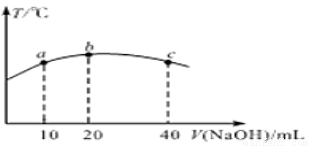
①该烧碱溶液的浓度为0.02mol/L
②该烧碱溶液的浓度为0.01mol/L
③HNO2的电离平衡常数:b点>a点
④从b点到c点,混合溶液中一直存在:c(Na+)>c(NO2-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一下学期3月月考化学试卷(解析版) 题型:选择题
下列物质呈固态时必定属于分子晶体的是( )
A.非金属氧化物 B.金属氧化物
C.非金属单质 D.常温下呈气态的物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com