
| +3 |
| Fe |
| +3 |
| Fe |


科目:高中化学 来源: 题型:
| A、Fe+2HCl═H2+FeCl2 |
| B、2FeCl2+Cl2═2FeCl3 |
| C、CaO+H2O═Ca(OH)2 |
| D、2Fe(OH)3═Fe2O3+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1molSO2的质量为64g/mol |
| B、CH4的摩尔质量为16g |
| C、SO2的摩尔质量等于SO2的相对分子质量 |
| D、NA个SO2的质量以克为单位与SO2的相对分子质量在数值上相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲醇不完全燃烧生成CO和液态水的热化学方程式:CH3OH(l)+O2 (g)═CO(g)+2H2O(l)△H1=-1009.5kJ?mol-1 |
| B、已知:S(s)+O2(g)=SO2(g)△H1;S(g)+O2(g)=SO2(g)△H2;则△H1>△H2 |
| C、2H2O(g)═2H2(g)+O2(g)△H1=+571.6 kJ?mol-1 |
| D、△H>0的化学反应在高温条件下才能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水和冰的混合物,澄清石灰水 |
| B、净化后的空气,氧化镁 |
| C、生锈的铁钉,高锰酸钾充分加热后的剩余固体 |
| D、氯化钾,液氧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
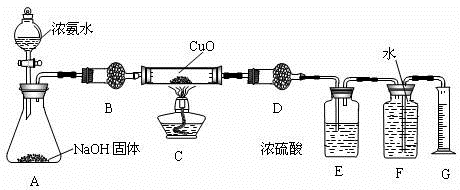
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.查看答案和解析>>
科目:高中化学 来源: 题型:
 现有易溶强电解质的混合溶液10L,其中可能含有K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示:请回答下列问题:
现有易溶强电解质的混合溶液10L,其中可能含有K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如图所示:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com