
科目:高中化学 来源:2015-2016学年福建省高一上第二次月考化学试卷(解析版) 题型:填空题
工业上,从海水中提取溴常用如下方法:
(1)将海水浓缩后,向其中通入氯气,将溴化物氧化,以溴化钠为例,用化学方程式表示该反应 ,该反应属于四种基本反应类型中的 反应,也属于
反应_______(选填“氧化还原反应”或“非氧化还原反应” )。
(2)向上述混合液中吹入热空气,将生成的溴吹出,是根据溴的沸点比水的沸点 (选填“低”或“高” )的性质,吹出的溴用碳酸钠溶液吸收,这一过程的化学方程式为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑,生成物中溴元素的化合价分别为 价。 这一类型的化学反应称为歧化反应。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省宝安第一外国语学校高二上期中考试化学试卷(解析版) 题型:选择题
已知:298K时,2SO2(g) + O2(g)  2SO3(g) △H = —Q1 KJ/mol,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q2KJ,则下列关系式正确的是( )
2SO3(g) △H = —Q1 KJ/mol,在相同温度下,向密闭容器中通入2molSO2和1molO2,达到平衡时放出热量Q2KJ,则下列关系式正确的是( )
A.Q1>Q2 B.Q1<Q2 C.Q1=Q2 D.无法比较
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省宝安第一外国语学校高一上期中考试化学试卷(解析版) 题型:选择题
同温同压下,下列气体的密度最大的是( )
A.氢气 B.二氧化硫 C.氧气 D.二氧化碳
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列分离、提纯、鉴别物质的方法正确的是( )
A.用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液
B.用溶解、过滤的方法提纯含有少量BaSO4的BaCO3
C.用过滤的方法除去蔗糖溶液中含有的少量淀粉胶体
D.用加热、过滤、蒸发的方法可以除去粗盐中的泥沙、CaCl2、MgCl2等杂质
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上学期12月月考化学试卷(解析版) 题型:选择题
a g Fe2O3和Al2O3组成的混合物全部溶于20 mL、物质的量浓度为0.05 mol/L的硫酸中,反应后向所得溶液中加入10 mL NaOH溶液,恰好使Fe3+、Al3+完全沉淀,则氢氧化钠溶液的物质的量浓度为( )
A.0.1 mol/L B.0.2 mol/L C.0.4 mol/L D.0.8 mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高一上学期12月月考化学试卷(解析版) 题型:填空题
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,实验小组利用A制备Al(OH)3的操作流程如下:
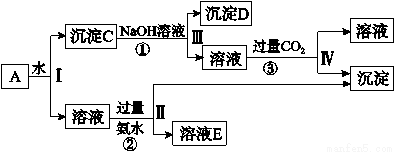
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀所采取的操作名称是______,该实验操作所用到的玻璃仪器有____ _。
(2)根据上述流程,写出D、E所含物质的化学式:沉淀D________;溶液E________、_______。
(3)写出②、③反应的离子方程式:
②__________ __ _;③________ _____。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上学期第三次月考化学试卷(解析版) 题型:选择题
某氨水的pH=X,某盐酸的pH=Y,已知X+Y=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是
A. c( NH4+ )>c(Cl-)>c(OH-)>c(H+) B. c( NH4+)>c(Cl-)>c(H+)>c(OH-)
C. c(Cl-)>c(NH4+)>c(H+)>c(OH-) D. c( NH4+)>c(H+)>c(Cl-) >c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南京市六校高三上学期12月联考化学试卷(解析版) 题型:实验题
氯酸钠(NaClO3)是无机盐工业的重要产品之一。
(1)工业上制取氯酸钠采用在热的石灰乳中通入氯气,然后结晶除去氯化钙后,再加入适量的 (填试剂化学式),过滤后即可得到。
(2)实验室制取氯酸钠可通过如下反应3C12+6NaOH 5NaC1+NaC1O3+3H2O
5NaC1+NaC1O3+3H2O
先往-5℃的NaOH溶液中通入适量C12,然后将溶液加热,溶液中主要阴离子浓度随温度的变化如右图所示,图中C表示的离子是 。

(3)某企业采用无隔膜电解饱和食盐水法生产氯酸钠。则反应化学方程式为: 。
(4)样品中C1O3-的含量可用滴定法进行测定,步骤如下:
步骤1:准确称取样品ag(约2.20g),经溶解、定容等步骤准确配制1000mL溶液。
步骤2:从上述容量瓶中取出10.00mL溶液于锥形瓶中,准确加入25mL 1.000mol/L (NH4)2Fe(SO4)2溶液(过量),再加入75mL硫酸和磷酸配成的混酸,静置10min。
步骤3:再在锥形瓶中加入100mL蒸馏水及某种指示剂,用0.0200mol/L K2Cr2O7标准溶液滴定至终点,消耗体积15.62mL。
步骤4: 。
步骤5:数据处理与计算。
①步骤2中反应的离子方程式为 ;静置10min的目的是 。
②步骤3中K2Cr2O7标准溶液应盛放在 (填仪器名称)中。
③为精确测定样品中C1O3-的质量分数,步骤4操作为 。
(5)在上述操作无误的情况下,所测定的结果偏高,其可能的原因的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com