
科目:高中化学 来源:2016-2017学年新疆兵团第二师华山中学高二下学期学前考试化学试卷(解析版) 题型:选择题
少量铁粉与100 mL 0.01 mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③滴入几滴浓盐酸 ④加CH3COONa固体 ⑤加NaCl固体 ⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发) ⑧改用10 mL 0.1 mol/L盐酸
A. ①⑥⑦ B. ③⑤⑦⑧ C. ③⑦⑧ D. ③⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省台州市高二上学期期末质量评估考试化学试卷(解析版) 题型:选择题
下列各组中的两种有机物,其最简式相同但不是同系物的是( )
A. 甲酸与硬脂酸 B. 甲醇与甘油 C. 苯酚与苯甲醇 D. 苯与苯乙烯
查看答案和解析>>
科目:高中化学 来源:2017届天津市红桥区高三上学期期末考试(下学期开学考试)化学试卷(解析版) 题型:选择题
用下图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是
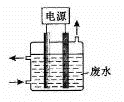
A. 用石墨作阳极,铁作阴极
B. 阳极的电极反应式为:Cl- + 2OH--2e-= ClO- + H2O
C. 阴极的电极反应式为:2H2O + 2e- = H2↑ + 2OH-
D. 除去CN-的反应:2CN-+ 5ClO- + 2H+ = N2↑ + 2CO2↑ +5Cl-+ H2O
查看答案和解析>>
科目:高中化学 来源:2017届天津市红桥区高三上学期期末考试(下学期开学考试)化学试卷(解析版) 题型:选择题
下图是部分短周期元素的原子序号与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是
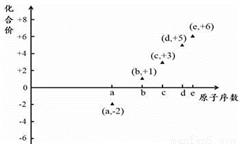
A. 31d和33d属于同种核素 B. 气态氢化物的稳定性:a>d>e
C. 工业上常用电解法制备单质b和c D. a和b形成的化合物不可能含共价键
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宿州市高一上学期期末教学质量检测(a卷)化学试卷(解析版) 题型:填空题
现有八种物质:①HCl ②Na2SO4晶体 ③浓硝酸 ④铜 ⑤烧碱 ⑥蔗糖 ⑦C12 ⑧SO2
(1)上述物质中可导电的是_______(填序号);
(2)上述物质中属于非电解质的是_______(填序号);
(3)写出②溶于水的电离方程式_______________;
(4)写出⑧与足量的⑤在溶液中反应的离子方程式_______________;
(5)在③与④的反应中,还原产物为_______________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宿州市高一上学期期末教学质量检测(a卷)化学试卷(解析版) 题型:选择题
对于某盐溶液的检验,其结论一定正确的是
A. 加入稀盐酸产生无色气体,该气体可使澄清石灰水变浑浊,则一定含有CO32-
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则一定含有SO42-
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则一定含有NH4+
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,则一定含有Ba2+
查看答案和解析>>
科目:高中化学 来源:2017届江苏省联盟大联考高三2月联考化学试卷(解析版) 题型:填空题
工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3)。其工业流程如下:
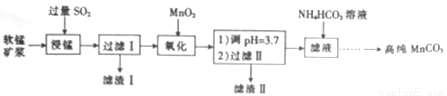
(1)过滤Ⅰ所得滤液中主要存在的两种金属阳离子为____和_____(填离子符号)。
(2)写出氧化过程中MnO2与SO2反应的化学方程式:____________。
(3)“浸锰”反应中往往有副产物MnS2O6生成,温度对“浸锰”反应的影响如图所示,为减少MnS2O6的生成,“浸锰”的适宜温度是___________。

(4)向过滤Ⅱ所得的滤液中加入NH4HCO3溶液时温度控制在30-35℃,温度不宜太高的原因是___。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同时还有气体生成,写出反应的离子方程式:_______。
(6)生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高二上学期期末考试化学试卷(解析版) 题型:计算题
常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。试回答下列问题:
(1)混合溶液pH=8的原因是______________(用离子方程式表示)
(2)混合溶液中由水电离出的c(OH-)___________(填“大于”、“等于”或“小于”)0.1mol/LNaOH溶液中由水电离出的c(OH-)
(3)求出混合溶液中下列算式的精确计算结果(填具体数字):
c(Na+)- c(A-)=____________mol/L, c(OH-)- c(HA)=____________mol/L
常温下,将PH=2的酸HA溶液与PH=12的NaOH溶液等体积混合后,所得溶液PH_________7 (填“大于”、“等于”或“小于”)
(5)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的PH___________7(填“大于”、“等于”或“小于”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com