
��֪25��ʱ��AgC1��AgBr��Agl��Ksp�ֱ�Ϊ1��8��l0-l0��5��O��10��13��8��3��10��17����AgNO3����Һ�ζ�±�����ӵĹ��̣��Ե���AgNO3��Һ�����Ϊ�����꣬pXΪ�����꣺[pX= -lgc��X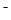 ��]���Ϳɻ�õζ����ߡ�����0��1 mol��L-l AgNO3��Һ�ֱ�ζ�20��00 mL 0��1 mol��L-lCl
��]���Ϳɻ�õζ����ߡ�����0��1 mol��L-l AgNO3��Һ�ֱ�ζ�20��00 mL 0��1 mol��L-lCl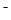 ��Br
��Br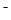 ��I
��I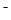 ��õζ�������ͼ�������й�˵������ȷ����
��õζ�������ͼ�������й�˵������ȷ����
A��a��b��c�ֱ��ʾCl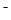 ��Br ��Br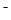 ��I ��I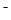 |
B��a��b��c�ֱ��ʾI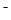 ��Br ��Br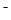 ��Cl ��Cl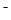 |
C��a��b��c�ֱ��ʾBr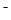 ��I ��I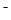 ��Cl ��Cl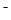 |
D�����������ζ����ⶨ������c��Cl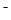 ��������KI��ָʾ�� ��������KI��ָʾ�� |
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
+ 2 |
- 6 |
+ 2 |
- 6 |
+ 4 |
| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ���ݸ���ѧ2012������������¿���ѧ���� ���ͣ�013
|
��֪25��ʱ��AgC1��AgBr��Agl��Ksp�ֱ�Ϊ1.8��10��10��5.0��10��13��8.3��10��17����AgNO3����Һ�ζ�±�����ӵĹ��̣��Ե���AgNO3��Һ�����Ϊ�����꣬pXΪ�����꣺[pX����lgc(X��)]���Ϳɻ�õζ����ߣ�����0.1 mol��L��1��AgNO3��Һ�ֱ�ζ�20.00 mL��0.1 mol��L��1��Cl����Br����I����õζ�������ͼ�������й�˵������ȷ����
| |
| [����] | |
A�� |
a��b��c�ֱ��ʾCl����Br����I�� |
B�� |
a��b��c�ֱ��ʾI����Br����Cl�� |
C�� |
a��b��c�ֱ��ʾBr����I����Cl�� |
D�� |
���������ζ����ⶨ������c(Cl��)������KI��ָʾ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com