
氯气是一种重要的化工原料,在工农 业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
业生产、生活中有着重要的应用。请你根据所学知识回答下列问题:
Ⅰ.把氯气通入紫色石蕊溶液中,可以观察到的现象是:
请你解释其中的原因 。
Ⅱ.某化学兴趣小组计划用氯气和氢氧化钠制取简易消毒液。
(1)其反应原理为: (用化学方程式表示)
(2)实验室配制好4.0 mol·L-1的NaOH溶液,这种溶液 L才能与2.24 L氯气(标准状况)恰好完全反应。
(3)配制500 mL 4.0 mol·L-1 NaOH溶液的实验步骤:
a.计算需要氢氧化钠固体的质量。
b.称量氢氧化钠固体。
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶。
d.用适量蒸馏水溶解称量好的氢氧化钠固体,冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1 cm~2 cm时,改用胶头滴管加蒸馏水至凹液面与刻度线相切。
①所需称量的氢氧化钠固体的质量是
②上述步骤的正确操作顺序是
③上述实验需要的仪器有
 ④某同学观察液面的情况如图所示,对所配溶液的物质的量浓度有何影响? (填“偏高”、“偏低”或“无影响”);
④某同学观察液面的情况如图所示,对所配溶液的物质的量浓度有何影响? (填“偏高”、“偏低”或“无影响”);

⑤在配制溶液的过程中,下列操作能造成结果偏低的是 。
A.容量瓶不干燥,含有少量蒸馏水
B.溶解所用烧杯未洗涤
C.NaOH溶解后,未冷却即进行实验
D.定容后摇匀,发现液面低于刻度线,然后又加水至刻度线。
科目:高中化学 来源:2016-2017学年江西省高二上第二次月考化学试卷(解析版) 题型:选择题
下列有关化学实验的叙述中,不正确的是( )
A.用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率
B.制肥皂时,在皂化液里加入饱和食盐水,能够促进高级脂肪酸钠的析出
C.制备乙酸乙酯时,为除去乙酸乙酯中的乙酸,用饱和碳酸钠溶液收集产物
D.制乙烯时,用量程为100℃的温度计代替量程为300℃的温度计,测反应液的温度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期中化学试卷(解析版) 题型:选择题
在密闭容器中,一定条件下进行如下反应:NO(g) +CO(g) 

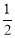 N2(g) +CO2(g);△H=-373.2kJ·mol-1 ,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g) +CO2(g);△H=-373.2kJ·mol-1 ,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上9月月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是 ( )
A.铁与稀HNO3 反应:Fe+2H+==Fe2++H2↑
B.大理石溶于醋酸中:CaCO3+2CH3COOH==Ca2++2CH3COO-+CO2↑+H2O
C.氯化钙与碳酸氢钾溶液混合:Ca2++CO ==CaCO3↓
==CaCO3↓
D.向小苏打溶液中加入过量的澄清石灰水:2HCO +Ca2++2OH-==CaCO3↓+2H2O+CO
+Ca2++2OH-==CaCO3↓+2H2O+CO
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上9月月考化学试卷(解析版) 题型:选择题
短周期元素R、T、Q、W在元素周期表中的相对位置如下图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是 ( )

A. 最简单气态氢化物的热稳定性:R>Q
B. 最高价氧化物对应水化物的酸性:Q<W
C. 原子半径:T>Q>R
D. 含T的盐溶液一定能与碱反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省青岛市高一上月考一化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.1.00mol NaClO中含有6.02×1023个Cl-
B. 1.00mol NaCl中,所有Na+的最外层电子总数约为8×6.02×1023
C.欲配置1.00L ,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中
D.电解58.5g 熔融的NaCl,能产生22.4L氯气(标准状况)、23.0g金属钠
{2NaCl(熔融) = 2Na + Cl2↑(通电电解),制取金属钠和氯气。}
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省青岛市高一上月考一化学试卷(解析版) 题型:选择题
在标准状况下 ,100mL 某气体的质量为0.125g,则该气体可能是下列中的
,100mL 某气体的质量为0.125g,则该气体可能是下列中的
A. 氨气 B. 氮气 C. 二氧化碳 D. 氢气
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省济南市高二上第一次质检化学卷(解析版) 题型:选择题
可用于电动汽车的铝﹣空气燃料电池,通常以NaCl溶液或NaOH溶液为电解液,铝合金为负极,空气电极为正极.下列说法正确的是( )
A.以NaCl溶液或NaOH溶液为电解液时,正极反应都为:O2+2H2O+4e﹣=4OH﹣
B.以NaOH溶液为电解液时,负极反应为:Al+3OH﹣﹣3e﹣=Al(OH)3↓
C .以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
.以NaOH溶液为电解液时,电池在工作过程中电解液的pH保持不变
D.电池工作时,电子通过外电路从正极流向负极
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一上月考一化学卷(解析版) 题型:选择题
固体单质A和气体单质B在容积一定的密闭容器中完全反应生成气体C,相同温度下测得容器内压强不变,若产物气体C的密度是原气体密度的4倍,则判断正确的是( )
A.两种单质A、B的摩尔质量之比是1∶4
B.反应前后的气体质量之比一定是1∶4
C.在生成物C中,A的质量分数为50%
D.C中A、B两元素的原子个数比为3∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com