
(20分)
Ⅰ 以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。

① 若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);若装置D中装的是V2O5(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为 。
②SO2通入B中,溶液颜色退去,则该反应的离子方程式为 。
(2) 某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母) ,仍然无法观察到沉淀产生。
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.硫化钠溶液
(3)若由元素S和O组成–2价酸根离子X,X中S和O的质量比为4∶3;当Cl2与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。

(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如上图,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为_________极,其电极反应式为 ;电池的总反应式
Ⅱ 实验是化学研究的基础,关于下列各装置图的叙述正确的是
(填序号)
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正扳,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
D.装置④能用于测量气体体积
Ⅲ 用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。下列说法中正确的是 (填序号)

A.铅蓄电池负极的反应式为:Pb—2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
科目:高中化学 来源: 题型:
2- 4 |
2- 4 |
| 化学式 | CaCO3 | CaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 2.8×10-9 | 9.1×10-6 | 1.0×10-4 | 6.8×10-6 | 1.8×10-11 |
查看答案和解析>>
科目:高中化学 来源:黑龙江省哈师大附中2011-2012学年高一上学期期中考试化学试题 题型:022
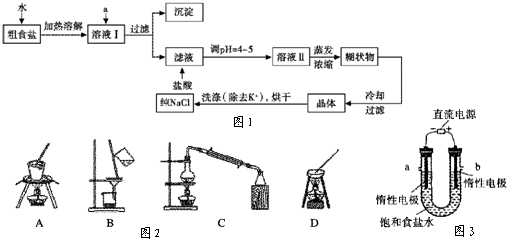
人类与食盐关系密切,食盐在老百姓生活和现代社会的工农业生产中均有重要作用.粗盐中含有Ca2+、Mg2+、SO![]() 以及泥沙等杂质,请回答粗盐提纯的有关问题:
以及泥沙等杂质,请回答粗盐提纯的有关问题:
(1)为了除去粗盐中的泥沙,可采取的提纯实验操作方法的名称是________.
(2)为了除去可溶性杂质,可以按以下实验步骤进行提纯:①加过量BaCl2溶液;②加过量NaOH溶液;③加过量Na2CO3溶液;④过滤;⑤________.请补全实验步骤,并回答步骤③的目的是________.
(3)2010年7月26日,卫生部公布了《食用盐碘含量》的征求意见稿,面向社会征求意见.对于食用盐中碘含量平均水平的规定有所降低.食盐中添加的是KIO3.可用下列反应来检验食盐中是否含KIO3:
KIO3+KI+H2SO4-I2+K2SO4+H2O(
未配平).请配平该反应并表示出电子转移的方向和数目________;为了获取反应后溶液中的I2,可采取的实验操作方法的名称是________.查看答案和解析>>
科目:高中化学 来源:福建省四地六校2011-2012学年高二上学期第二次月考化学试题 题型:058
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过如图所示装置研究反应速率的有关问题.

(1)取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内足量的稀盐酸中.足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图所示.
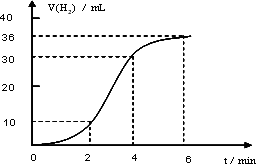
①请根据实验中现象并结合上图中数据回答0到6分钟内哪一段速率最快________.
A:0-2分钟
B:2-4分钟
C:4-6分钟
②并请简述速率出现这种情况的其原因:________
(2)某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快.他决定对其原因进行探究.填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO![]() 对反应没有影响;
对反应没有影响;
原因Ⅱ:Cl-对反应没有影响,而SO![]() 对反应具有阻碍作用;
对反应具有阻碍作用;
原因Ⅲ:________;
原因Ⅳ:Cl-、SO![]() 均对反应具有促进作用,但Cl-影响更大;
均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:________.
②该同学设计并进行了两组实验,即得出了正确结论.他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化.
若观察到实验a中________,实验b中________,则说明原因Ⅰ是正确的.依次类推.该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用.
查看答案和解析>>
科目:高中化学 来源:浙江省温州市楠江中学2009-2010学年高二下学期期中化学试题 题型:058
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法通过下图所示装置研究反应速率的有关问题.

(1)取一段镁条,用砂纸擦去表面的氧化膜,使镁条浸入锥形瓶内足量的稀盐酸中.足量镁条与一定量盐酸反应生成H2的量与反应时间的关系曲线如图所示.

①请在下图的方框中画出上述反应的速率与时间的关系曲线.

②在前4 min内,镁条与盐酸的反应速率逐渐加快,请简述其原因:________________;在4 min之后,反应速率逐渐减慢,请简述其原因:________________.
(2)某同学发现,纯度、质量、表面积都相同的两铝片与H+浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝和盐酸反应速率更快.他决定对其原因进行探究.填写下列空白:
①该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl-对反应具有促进作用,而SO![]() 对反应没有影响;
对反应没有影响;
原因Ⅱ:________________;
原因Ⅲ:Cl-对反应具有促进作用,而SO![]() 对反应具有阻碍作用;
对反应具有阻碍作用;
原因Ⅳ:Cl-、SO![]() 均对反应具有促进作用,但Cl-影响更大;
均对反应具有促进作用,但Cl-影响更大;
原因Ⅴ:________________.
②该同学设计并进行了两组实验,即得出了正确结论.他取了两片等质量、外形和组成相同、表面经过砂纸充分打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
a.在盛有硫酸的试管中加入少量NaCl或KCl固体,观察反应速率是否变化;
b.在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否变化.
若观察到实验a中________________,实验b中________________,则说明原因Ⅲ是正确的.依次类推.该同学通过分析实验现象,得出了结论:Cl-对反应具有加速作用.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com