
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4—(绿色)、Cr2O72—(橙红色)、CrO42—(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答:
(1)Cr3+与Al3+的化学性质相似,往Cr2(SO4)3溶液中滴入NaOH溶液直至过量,可观察到的现象是 。
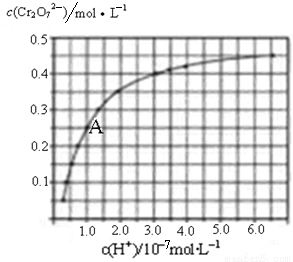
(2)CrO42—和Cr2O72—在溶液中可相互转化。室温下,初始浓度为1.0mol•L﹣1的Na2CrO4溶液中c(Cr2O72—)随c(H+)的变化如图所示。
 ①用离子方程式表示Na2CrO4溶液中的转化反应 。
①用离子方程式表示Na2CrO4溶液中的转化反应 。
②由图可知,溶液酸性增强,CrO42﹣的平衡转化率 (填“增大“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为 。
(3)用K2CrO4为指示剂,以AgNO3标准液滴定溶液中的Cl﹣,Ag+与CrO42﹣生成砖红色沉淀时到达滴定终点。当溶液中Cl﹣恰好完全沉淀(浓度等于1.0×10﹣5mol•L﹣1)时,溶液中c (Ag+)为 mol•L﹣1,此时溶液中c(CrO42﹣)等于 mol•L﹣1。(Ksp(Ag2CrO4)=2.0×10﹣12、Ksp(AgCl)=2.0×10﹣10)。
(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72﹣还原成Cr3+,反应的离子方程式为 。
科目:高中化学 来源:2017届宁夏高三上期中化学试卷(解析版) 题型:填空题
在下图所示装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹,夹在被Na2SO4溶液浸湿的滤纸条上,滤纸条的中部滴有KMnO4液滴;电源有a、b两极。若在A、B中充满KOH溶液后倒立于KOH溶液的水槽中,断开K1,闭合K2、K3,通直流电,实验现象如图所示。
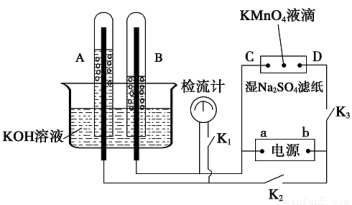
则:①标出电源的正、负极:a为________极,b为______极。
②在湿的Na2SO4滤纸条中部的KMnO4液滴处有什么现象发生?__________________
③写出电极反应式:C中______________,D中______________。
④若电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,则检流计的指针是否移动?___________(填“是”或“否”),其理由________________。写出电极反应式:A中 ,B中__ _。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三上期中化学试卷(解析版) 题型:选择题
下列实验操作、现象和结论均正确的是( )
选项 | 实验操作 | 现象 | 结论 |
A | SO2通入溴水中 | 溶液褪色 | SO2有漂白性 |
B | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已氧化变质 |
C | 将新制氯水和KI溶液在试管中混合后,加入CCl4,振荡、静置 | 溶液分层,下层呈紫色 | 氧化性:Cl2<I2 |
D | 分别向0.1 mol·L-1醋酸和饱和硼酸溶液中滴加0.1 mol·L-1 Na2CO3溶液 | 醋酸中有气泡产生,硼酸中没有气泡产生 | 酸性:醋酸>碳酸>硼酸 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上月考二化学试卷(解析版) 题型:选择题
已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示已知A、B、D、E均为中学化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是

A、若A是铁,则E可能为稀硝酸
B、若A是CuO,E是碳,则B为CO
C、若A是AlCl3溶液,E可能是氨水
D、若A是NaOH溶液,E是CO2,则B为NaHCO3
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上月考二化学试卷(解析版) 题型:选择题
下列说法不正确的是①将BaSO4放入水中不能导电,所以硫酸钡是非电解质;
②氨溶于水得到的溶液氨水能导电,所以氨水是电解质;
③固态共价化合物不导电,熔融态的共价化合物可以导电
④固态的离子化合物不导电,熔融态的离子化合物可以导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
A.①④ B.①④⑤ C.①②③④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江牡丹江高级中学高三上期中化学卷(解析版) 题型:选择题
反应:MgSO4(s) + CO(g) MgO(s)+CO2(g)+SO2(g) ΔH>0。在恒
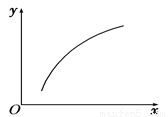
MgO(s)+CO2(g)+SO2(g) ΔH>0。在恒 容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,y随x变化趋势合理的是
容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,y随x变化趋势合理的是
选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江牡丹江高级中学高三上期中化学卷(解析版) 题型:选择题
对室温下10 mL pH=3的醋酸溶液作如下改变时,说法正确的是
A.加水稀释到原体积的10倍, 溶液的pH=4
B.加水稀释,溶液中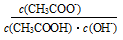 不变,n(OH-)增大
不变,n(OH-)增大
C.加入10 mL pH=11的NaOH溶液,所得混合液的pH=7
D.加入少量醋酸钠固体, 则平衡CH3COOH CH3COO-+ H+逆向移动,K变小
CH3COO-+ H+逆向移动,K变小
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期月考二化学试卷(解析版) 题型:实验题
某实验小组用 0.50 mol/L NaOH 溶液和 0.50 mol/L H2SO4 溶液进行中和热的测定。
Ⅰ.配制 0.50 mol/L NaOH 溶液
(1)实验中大约要使用 245 mL NaOH 溶液,则至少需要称量 NaOH 固体 g。
(2)从表中选择称量 NaOH 固体所需要的仪器 (填序号)。

Ⅱ.测定中和热的实验装置如图所示。
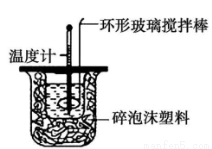
(3)写出稀硫酸和稀 NaOH 溶液反应表示中和热的热化学方程式 (中和热为 57.3 kJ/mol)。

①温度差的平均值为__________。
②使硫酸与 NaOH 溶液混合均匀的正确操作是 (填字母)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
③近似认为 0.50 mol/L NaOH 溶液和 0.50 mol/L 硫酸的密度都是 1g/cm3,中和后生成溶液的比热容 c = 4.18 J/(g·℃),则中和热 Δ H= ________(结果保留小数点后一位)。
④上述实验结果与 57.3 kJ/mol 有偏差,产生偏差的原因可能是__________(填字母)。
A.实验装置保温、隔热效果差
B.量取 NaOH 溶液的体积时仰视读数
C.分多次把 NaOH 溶液倒入盛有硫酸的小烧杯中
D.用温度计测定 NaOH 溶液起始温度后直接测量 H2SO4 溶液的温度
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三上学期11月月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以HClO4的氧化性强
B.已知①Fe+Cu2+=Fe2++Cu②2Fe3++Cu=2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+
C.已知还原性:B->C->D-,反应2C-+D2=2D-+C2和反应2C-+B2=2B-+C2都能发生
D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com