
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源:2017届广东省惠州市高三上学期调研模拟二化学试卷(解析版) 题型:实验题
钛合金烤瓷牙是目前国内使用最为普遍的一种烤瓷牙,TiCl4是生产金属钛的原料。
(1)工业上主要用TiO2氯化的方法来制取TiCl4
① 有人拟用以下氯化反应来制取TiCl4:TiO2(s)+2Cl2(g) TiCl4(l)+O2(g) ,写出实验室用二氧化锰与浓盐酸反应制取Cl2的离子方程式 。
TiCl4(l)+O2(g) ,写出实验室用二氧化锰与浓盐酸反应制取Cl2的离子方程式 。
② 工业上通常往TiO2和Cl2反应体系中加入碳单质,在一定条件下制取TiCl4,从化学平衡的角度解释此方法能顺利制取TiCl4的原因 。
(2)某化学实验小组以TiO2和足量 CCl4为原料制取TiCl4,装置图如下:
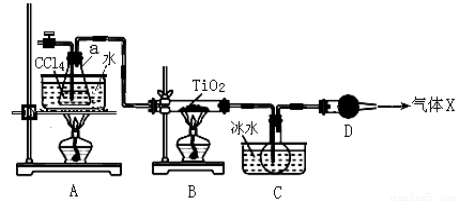
下表是有关物质的性质:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | ﹣23 | 76.8 | 与TiCl4互溶 |
TiCl4 | ﹣25 | 136 | 遇潮湿空气产生白雾 |
① 实验开始时先点燃A处的酒精灯,待C中烧瓶里有液滴出现时再点燃B处的酒精灯,其主要目的是 。
② 本实验中仪器a采用题给的加热方式的突出优点是 。
③ B中CCl4与TiO2发生反应的化学方程式是 。
④ 欲分离C装置中的TiCl4,应采用的实验操作为 (填操作名称)。
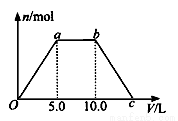
⑤ 若将反应过程中生成的气体X(足 量)缓缓通入Ba( OH)2和NaOH的混合稀溶液中,生成沉淀的物质的量(n)和 通入气体X的体积(V)的关系如图所示,若混合溶液中Ba( OH)2和2NaOH的物质的量之比为1:1,则b点溶液中溶质主要成分的化学式为 , 从b点到c点,沉淀减少过程中发生反应的离子方程式为 。
量)缓缓通入Ba( OH)2和NaOH的混合稀溶液中,生成沉淀的物质的量(n)和 通入气体X的体积(V)的关系如图所示,若混合溶液中Ba( OH)2和2NaOH的物质的量之比为1:1,则b点溶液中溶质主要成分的化学式为 , 从b点到c点,沉淀减少过程中发生反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三上学期期中化学试卷(解析版) 题型:选择题
下列解释实验事实的方程式正确的是
A.用氢氧化钠溶液去除铝条表面的氧化膜:Al2O3+2OH—=2AlO2—+H2O
B.铜片溶于稀硝酸产生无色气体:Cu+4H++2NO3—=Cu2++2NO2↑+2H2O
C.氢氧化亚铁在空气中变质:2Fe(OH)2+O2+2H2O=2Fe(OH)3
D.碳酸钠溶液呈碱性:CO32—+2H2O H2CO3+2OH—
H2CO3+2OH—
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市高一10月月考化学卷(解析版) 题型:选择题
N2与O2 的混合气体的密度对氢气的相对密度为14.5,则N2在混合气体中的质量分数为
A.72.4% B.75% C.50% D.80.5%
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市高一10月月考化学卷(解析版) 题型:选择题
不用其他试剂,用最简单的方法鉴别下列物质:( )
①NaOH溶液,②Mg(NO3)2溶液,③CuSO4溶液,④KCl溶液,正确的鉴别顺序是
A.①②③④ B.③④②①
C.④①②③ D.③①②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市高一10月月考化学卷(解析版) 题型:选择题
已知1.505×1023个X气体分子的质量为8 g,则X气体的摩尔质量是( )
A.16 g B.32 g
C.64 g/mol D.32 g/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二10月月考化学卷(解析版) 题型:填空题
密闭容器中发生如下反应:A(g)+3B(g) 2C(g) ΔH<0,根据下列速率-时间图像,回答下列问题:
2C(g) ΔH<0,根据下列速率-时间图像,回答下列问题:

(1)下列时刻所改变的外界条件是:t1___________;t3___________;t4___________;
(2)产物C的体积分数最大的时间段是_______________;A的物质的量最大的时间段是
(3)反应速率最大的时间段是___________;
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二10月月考化学卷(解析版) 题型:选择题
在一定条件下,对于A2(g)+3B2(g) 2AB3(g)反应来说,以下化学反应速率的表示中,化学反应速率最快的是
2AB3(g)反应来说,以下化学反应速率的表示中,化学反应速率最快的是
A.v(A2)=0.8 mol·L-1·s-1 B.v(A2)=30 mol·L-1·min-1
C.v(AB3)=1.0 mol·L-1·s-1 D.v(B2)=1.2 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:填空题
I.某温度下,Kw = 10-12。
(1)若保持温度不变,向少量水中加入_________g的NaOH固体,并加水至1 L,才能使溶液中水电离产生的H+、OH-的浓度乘积即:c(H+)·c(OH-) = 10-22
(2)若保持温度不变,某溶液中c(H+)为1×10-7 mol/L,则该溶液显________性(选填“酸”、“碱”或“中”)。
II.(3)实验室中常用NaOH进行洗气和提纯,当600 mL 1 mol/L NaOH溶液吸收标准状况下8.96 L CO2气体时所得溶液中各离子浓度由大到小的顺序是 。
(4)已知常温下Kw[Fe(OH)3] = 4.0×10-38,在FeCl3溶液中加入NaHCO3溶液,发生反应的离子方程式为_____________。若所得悬浊液的pH调整为4,则溶液中Fe3+的浓度为__________mol/L。
(5)试利用平衡移动原理解释下列事实:FeS不溶于水,但能溶于稀盐酸中_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com