
下列各组物质的性质比较中,正确的是( )
A. 氢化物的沸点:HI>HBr>HCl>HF B. 稳定性:HF>HCl>HBr>HI
C. 离子的还原性:Cl—>Br—>I— D. 单质的熔点:Li<Na<K<Rb
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年江西省南昌市高一下学期第一次月考化学试卷(解析版) 题型:选择题
取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4∶1)的混合气体;然后分别做溶解于水的喷泉实验。实验结束后三个烧瓶中所得溶液的物质的量浓度之比为( )
A.2∶1∶2 B.1∶1∶1
C.5∶5∶4 D.7∶7∶4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二3月月考化学试卷(解析版) 题型:选择题
根据等电子原理判断,下列说法中错误的是
A.B3N3H6分子中所有原子均在同一平面上
B.B3N3H6分子中存在双键,可发生加成反应
C.H3O+和NH3是等电子体,均为三角锥形
D.CH4和NH4+是等电子体,均为正四面体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷(解析版) 题型:实验题
某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。
(Ⅰ)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
①甲同学设计实验的目的是____________________
②反应最剧烈的烧杯是_______(填字母);
③写出b烧杯里发生反应的离子方程式_________________
(Ⅱ)乙同学设计了下图装置来探究碳、硅元素的非金属性强弱,根据要求完成下列各小题
(1)实验装置:

填写所示仪器名称A___________B___________
(2)实验步骤: 连接仪器、________、加药品后,打开a、然后滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是______________,装置E中足量酸性KMnO4溶液的作用是_______________。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是_________________;
③试管D中发生反应的离子方程式是_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷(解析版) 题型:选择题
W、X、Y、Z是4种短周期元素,在元素周期表中的位置如下图所示,其中Z位于ⅦA族。下列判断错误的是( )
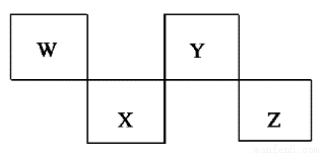
A. 常压下四种元素的单质中,W单质的熔点最高 B. Z的阴离子电子层结构与氩原子的相同
C. W的氢化物的沸点比Y的氢化物的沸点高 D. Y元素的非金属性比X元素的非金属性强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷(解析版) 题型:选择题
下列有关元素周期表中元素性质的叙述不正确的是( )
A. 同主族元素从上到下,非金属性逐渐减弱
B. 元素的最高正化合价在数值上均等于原子的最外层电子数
C. 同周期元素的原子半径从左到右逐渐减小(稀有气体除外)
D. 元素的非金属性越强,它的最高价氧化物的水化物的酸性越强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师范大学附属中学高一下学期第一次阶段性测试化学试卷(解析版) 题型:填空题
有1H、D、T三种原子:
(1)在标准状况下。它们的单质的密度之比是__ ;
(2)1mol各种单质中,它们的质子数比是_______;
(3)各lmol的H2O,D2O,T2O,它们的中子数之比是_____。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省南昌市高二下学期第一次阶段性考试化学试卷(解析版) 题型:实验题
已知使用林德拉催化剂(Pd/PbO、CaCO3)可使炔烃的氢化停留在生成烯烃的阶段,而不再进一步氢化。现有一课外活动兴趣小组利用上述原理设计了一套由如下图所示的仪器组装而成的实验装置(铁架台未画出),由乙炔制得乙烯,并测定在氢化反应中乙炔的转化率。若用含0.020 mol CaC2的电石和含1.30 g锌的锌粒(杂质不与酸反应)分别与足量的饱和食盐水和稀硫酸反应,当反应完全后,假定在标准状况下测得G中收集到的水的体积为V mL(忽略乙炔在水中溶解的部分)。试回答下列问题:

(1)各装置的连接顺序为
a→______→______→______→_____→______→______→h。
(2)分别写出A中和C中所发生反应的化学方程式:
A:______________________。
C:______________________。
(3)装置A中产生气体的反应速率往往太快,为了减慢反应速率,操作时还应采取的措施是__________________________。
(4)G所选用的量筒的容积较合理的是____________(填写选项字母)。
A.500 mL B.1000 mL C.2000 mL
(5)若V=672(导管内气体体积忽略不计),则乙炔的转化率为__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省北校高一3月月考化学试卷(解析版) 题型:选择题
现有下列短周期元素性质的数据:下列关于表中11种元素的说法正确的是
元素 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ |
原子半径 (10-10m) | - | 0.37 | 0.74 | 0.75 | 0.77 | 0.82 | 0.99 | 1.10 | 1.52 | 1.60 | 1.86 |
最高或最低化合价 | 0 | +1 | +5 | +4 | +3 | +7 | +5 | +1 | +2 | +1 | |
-2 | -3 | -4 | -1 | -3 |
A. 上表中11种元素中形成的非金属单质都有非极性共价键
B. ②⑨处于同一周期,④⑧处于同一主族
C. 上表中11种元素中最高价氧化物对应的水化物中⑦号酸性最强
D. ⑥原子结构示意图为:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com