
某化学科研小组研宄在其他条件不变时,改变某一条件对A2(g) +3B2 (g)  AB3 (g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度, n表示物质的景),根据如图可得出的判断结论正确的是( )
AB3 (g)化学平衡状态的影响,得到如右图所示的变化规律(图中T表示温度, n表示物质的景),根据如图可得出的判断结论正确的是( )
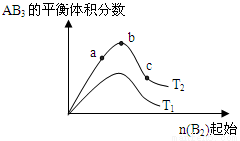
A.反应速率a>b>c
B.若T2>T1,则正反应一定是吸热反应
C.达到平衡时,AB3的物质的量大小为:b>c>a
D.达到平衡时A2的转化率大小为:b>a>c
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源:2016-2017学年黑龙江牡丹江中学高二上期中理化学卷(解析版) 题型:选择题
下列判断正确的是( )
A. pH=6的溶液一定呈酸性
B. c(H+)水电离产生 = c(OH-)水电离产生的溶液一定呈中性
C. 使石蕊试液显红色的溶液一定呈酸性
D. 强酸和强碱等物质的量混合后溶液一定呈中性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高一上期中化学卷(解析版) 题型:选择题
质量为8.02g的铁片,放进1.0 L 0.90 mol/L的CuSO4溶液中,过一段时间取出洗净、干燥称量,质量变为8.66g 。假设溶液的体积没有变化,则Cu2+的浓度变为
A.0.89 mol/L B.0.82 mol/L C.0.78 mol/L D.0.6 mol/L
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:填空题
汽车尾气和燃煤造成空气污染。
(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径.目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)△H=+QkJ/mol
CH3OCH3(g)+3H2O(g)△H=+QkJ/mol
①反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 0.4 | 0.6 | 1.0 | 1.1 | 1.7 |
写出该反应平衡常数表达式:K=__________。
向一个10L的密闭容器中充入10mol CO2和7molH2,830℃时测得H2为lmol,此时V (正)________V (逆):(选填“>”、“<”)
②判断该反应在一定温度下,体积恒定的密闭容器中达到化学平衡状态的依据是__________。
A. 容器中密度不变
B. 容器内压强保持不变
C.平均摩尔质量保持不变
D.v(CO2) :v(H2) =1:3
E.单位时间内消耗2 mol CO2,同时消耗1 mol二甲醚
F.△H不变
(2)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。
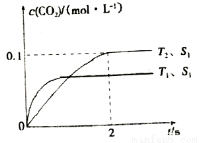
①在T2温度下,0~2 s内的平均反应速率v(N2)=__________;
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1〉S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化趋势曲线。
(3)工业上用CO和H2合成 CH3OH:CO (g) +2H2 (g)  CH3OH (g)
CH3OH (g)
①现在容积均为1 L的a、b、c三个密闭容器中分别充入1 mol CO和2 mol H2的混合气体,控制温度进行反应,测得相关数据的关系如图所示。下列说法正确的是____________

A.正反应的△H>0
B.反应进行到5 min时,b容器中v正=v逆
C.减压可使甲醇的含量由b点变成c点
D.达到平衡时,a、b、c中CO的转化率为b>a>c
②某温度下,在体积固定的4L密闭容器中将1molCO和2molH2混合,测得不同时刻的反应前后压强关系如下:
时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
压强比(p后/p前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
达到平衡时CO的转化率为__________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
下列各表述与示意图—致的是( )

A.图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液, 溶液的pH随加入酸体积的变化
B.图②中表示常温下,两份少量等浓度的盐酸与过量锌粉反应时,其中一份滴加了少量硫酸铜溶液
C.图③表示10 mL 0.01 mol/LKMnO4酸性溶液与过量的0.1 mol/L H2C2O4溶液混合时(Mn2+是该反应的催化剂),n (Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) +H2(g) →CH3CH3 (g)△H < 0,使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反 应mX(g)  nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
nY(g)+pZ(s) △H = Q kJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确的是( )
气体体积/L c(Y)/mol•L-1 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
A.m>n+p
B.Q<0
C.温度不变,压强增大,Y的体积分数减少
D.体积不变,温度升高,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
如图表示的是某离子X的水解过程示意图,则离子X可能是( )

A.CO32- B.HCO3- C.Na+ D.NH4+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上期中化学试卷(解析版) 题型:选择题
25℃时,某溶液中由水电离出的c(OH﹣)=1×10﹣13mol/L,该溶液中一定不能大量共存的离子组是
A.NH4+、Fe3+、SO42﹣、Cl﹣ B.CO32﹣、PO43﹣、K+、Na+
C.Na+、SO42﹣、NO3﹣、Cl﹣ D.HCO3﹣、Na+、HSO3﹣、K+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:选择题
普伐他汀是一种调节血脂的药物,其结构如图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述正确的是( )

A.不能通过反应形成高分子化合物 B.不能使酸性KMnO4溶液褪色
C.能发生加成、取代、消去反应 D.1 mol该物质最多可与1 mol NaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com