
【题目】下列关于物质结构的命题中,错误的项数有( )
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于p区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2、NaHSO4晶体中的阴、阳离子个数比均为1 :2
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为: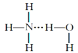
⑦HF沸点高于HCl,是因为 HCl共价键键能小于HF
⑧可燃冰中甲烷分子与水分子之间存在氢键
A.4项B.5项C.6项D.7项
【答案】B
【解析】
①甲基中,碳原子价层电子对个数=σ键个数+孤电子对个数=4+0=4,所以为sp3杂化,-COOH中,碳原子价层电子对个数=3+0=3,形成3个σ键,无孤对电子,采取sp2杂化,①正确;
②Ge位于第四周期ⅣA族,Ge为32号元素,原子核外电子排布式为[Ar]3d104s24p2,属于p区元素,②错误;
③H2O2结构不对称,属于极性分子,③错误;
④Na2O每有2个Na+,就有1个O2-,阴阳离子个数比为1:2,Na2O2每有2个Na+,就有1个![]() ,阴阳离子个数比为1:2,NaHSO4晶体中为Na+和
,阴阳离子个数比为1:2,NaHSO4晶体中为Na+和![]() ,阴阳离子个数比为1:1,④错误;
,阴阳离子个数比为1:1,④错误;
⑤Cu(OH)2属于碱能溶于硝酸,但Cu(OH)2能溶于氨水,是因为Cu(OH)2和氨水反应生成络合离子,属于络合反应,Cu(OH)2无两性,⑤错误;
⑥氢键应形成于X![]() H-Y形式中,X、Y必须是N、O、F元素之一,这样NH3·H2O的结构式有两种可能:H3N
H-Y形式中,X、Y必须是N、O、F元素之一,这样NH3·H2O的结构式有两种可能:H3N![]() H-O-H、H2N-H
H-O-H、H2N-H![]() OH2,由于NH3·H2O可电离出
OH2,由于NH3·H2O可电离出![]() 和OH-,前者合理,⑥正确;
和OH-,前者合理,⑥正确;
⑦HF和HCl属于分子晶体,由于HF中存在H—F![]() H这样的相互作用,即氢键,使得HF沸点高于HCl,⑦错误;
H这样的相互作用,即氢键,使得HF沸点高于HCl,⑦错误;
⑧O可以形成氢键,因此可燃冰中甲烷分子与水分子之间存在氢键,⑧正确;
综上所述,共5项错误,答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】二草酸合铜(Ⅱ)酸钾晶体{K2[Cu(C2O4)2]2H2O}(摩尔质量为354gmol-1),是一种工业用化工原料。微溶于冷水和酒精,虽可溶于热水但会慢慢分解,干燥时较为稳定,温度高于260℃易分解。实验室以胆矾和草酸为原料制备二草酸合铜(Ⅱ)酸钾晶体的流程如下,请根据相关流程回答:(已知:H2C2O4![]() CO↑+CO2↑+H2O)
CO↑+CO2↑+H2O)
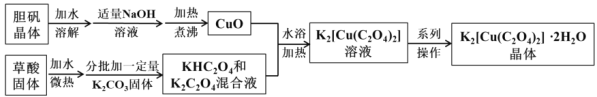
(1)抽滤CuO时若发现滤液中有较多浑浊,应采取的措施是_________。
(2)如图装置,经过一系列操作完成CuO的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整(洗涤操作只需考虑一次):开抽气泵→a→b→d→________→c→关抽气泵。
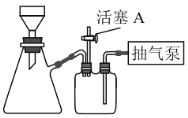
a.转移固液混合物; b.关活塞A; c.开活塞A; d.确认抽干; e.加洗涤剂洗涤
(3)KHC2O4和K2C2O4混合溶液制备时K2CO3固体需分批加入的原因是________。
(4)下列说法正确的是________。
A.从K2[Cu(C2O4)2]溶液中结晶时应采用水浴蒸发浓缩、冷却结晶
B.洗涤CuO沉淀和K2[Cu(C2O4)2]2H2O晶体时可分别用热水和冷水
C.为充分利用滤纸上的CuO,可将滤纸剪碎后加入到热的KHC2O4和K2C2O4混合溶液中,待充分反应后趁热过滤
D.在500℃下烘干K2[Cu(C2O4)2]2H2O晶体比200℃的效果更好
(5)产品纯度的测定:准确称取制得的晶体试样ag溶于氨水中,并加水定容至250mL,取试样溶液25.00mL,再加入10mL的稀硫酸,用bmolL-1的KMnO4标准液滴定,消耗KMnO4标准液V mL。
已知:![]()
①滴定过程中若不慎将标准液滴在锥形瓶内壁上,用少量蒸馏水冲洗锥形瓶内壁后再继续滴定至终点,实验结果会________。(填“偏大”“偏小”或“无影响”)
②该产品的纯度为________________。(用含字母的最简式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.凡是放热反应均能自发进行
B.N2(g)+3H2(g)![]() 2NH3(g) Δ H<0,当升高温度,该反应的 v(正)减小、v(逆)增大
2NH3(g) Δ H<0,当升高温度,该反应的 v(正)减小、v(逆)增大
C.钠投入水中,熔化成小球,说明钠和水的反应,反应物的总能量大于生成物的总能量
D.中和热测定时环形玻璃搅拌棒要不断顺时针搅拌,目的是为了混合均匀,充分反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家,磷酸铁锂锂离子电池充电时阳极反应式为,![]() ,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是
,电池放电时,锂离子从石墨晶体中脱嵌出来,通过隔膜迁移到磷酸铁锂晶体表面,然后重新嵌入到磷酸铁锂的晶格内,放电工作示意图如图。下列叙述不正确的是

A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铝箔沿导线流向铜箔
C.放电时正极反应为:![]()
D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从冬青中提取出的有机物A可用于合成抗结肠炎药物Y及其他化学品,合成路线如下图:

提示:
根据上述信息回答:
(1)请写出Y中含氧官能团的名称:__________________。
(2)写出反应③的反应类型:_________________。
(3)写出下列反应的化学方程式:
②______________。
⑤_______________。
(4)A的同分异构体I和J是重要的医学中间体,在浓硫酸的作用下I和J分别生成![]() 和
和 ,鉴别I和J的试剂为_________________。
,鉴别I和J的试剂为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】β-氮化碳的硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知该氮化碳的二维晶体结构如图所示。下列说法不正确的是( )
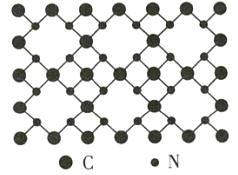
A.该晶体中的碳、氮原子都满足8电子稳定结构
B.该晶体中碳显+4价,氮显-3价
C.该晶体中每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连
D.该晶体的分子式为C3N4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)可用作高级耐火材料、新型陶瓷材料、LED基质材料等。已知:Si的电负性比H的小,利用硅烷(SiH4)制备氮化硅的反应为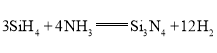 。下列有关说法正确的是( )
。下列有关说法正确的是( )
A.硅烷中Si的化合价为-4价B.NH3在该反应中作还原剂
C.H2既是氧化产物,也是还原产物D.转移1.2mol电子时,生成26.88 L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在抗击新冠病毒肺炎中瑞德西韦是主要药物之一。瑞德西韦的结构如图所示,下列说法正确的是

A.瑞德西韦中N、O、P元素的电负性:N>O>P
B.瑞德西韦中的O—H键的键能大于N—H键的键能
C.瑞德西韦中所有N都为sp3杂化
D.瑞德西韦结构中存在σ键、π键和大π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室为探究铜与浓硫酸(足量)的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法错误的是( )

A.装置B、C的目的分别是验证二氧化硫的还原性、氧化性
B.实验结束后可向装置A的溶液中加水,以验证是否有蓝色溶液生成
C.装置D的目的是验证SO2的漂白性及漂白的不稳定性
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com