
����Ŀ������ʽ��������������Na2SO4��ˮ��ԭ����ͼ��ʾ�����ö��Ե缫��ab��cd��Ϊ���ӽ���Ĥ����ֱ���糡�������£���Ĥ�м��Na+��SO42-��ͨ�����ӽ���Ĥ�������˸��������ӱ��赲���ܽ����м���ҡ�����������ȷ����
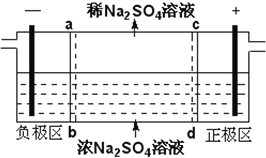
A. ͨ����м���ҵ�SO42-����������Ǩ�ƣ���������ҺpH����
B. �÷��ڴ�����Na2SO4��ˮʱ���Եõ�NaOH��H2SO4��Ʒ
C. ������ӦΪ2H2O�C4e�C=O2+4H+����������ҺpH����
D. ����·��ͨ��1mol���ӵĵ���ʱ������0.5mol��O2����
���𰸡�B
�������� A������ͬ�ֵ����ų⣬���ֵ���������ԭ���ڵ����������ӻ�������ɽ϶�������������ƶ������ͨ����м���ҵ�SO42������������Ǩ�ƣ���������������ɵ�OH��ʧȥ���ӣ�����������Ӧ���ŵ磬�����ƻ��˸�����ˮ�ĵ���ƽ�⣬ʹ��Һ��c(H��)>c(OH��)��������������Һ������ǿ����Һ��pH��С����A����B���������������ŵ磬��Һ�в������ᣬ�����������ӻ�õ��ӣ�������ԭ��Ӧ���ŵ磬�ƻ��˸�����ˮ�ĵ���ƽ�⣬ʹ��Һ��c(OH��)>c(H��)�����Բ����������ƣ���˸÷��ڴ�����Na2SO4��ˮʱ���Եõ�NaOH��H2SO4��Ʒ����B��ȷ��C�������������ӵõ����ӣ�ʹ��Һ��c(H��)�������Ը�������ҺpH���ߣ���C����D������·��ͨ��1mol���ӵĵ���ʱ�����������պϻ�·�е���ת����Ŀ��ȿ�֪��Ӧ�������������ʵ�����n(O2)=1mol��4=0.25mol����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ1��ʾø�ʹ����ı仯ѧ��Ӧ���ʵ�ԭ��,ͼ2��ʾ�������Ƽ�����ʼ��Ӧ���ʵ�Ӱ�졣ø�����Ƽ�����ø��ϲ�����ø���Եķ��ӡ����������Ƽ�����ᄎ��ø�Ļ��Բ�λ,�Ǿ��������Ƽ���ø���Բ�λ���������λ����,�Ӷ�����ø�Ļ��ԡ���ش��������⡣
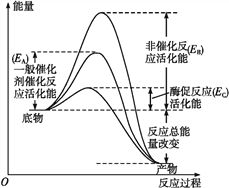 ͼ1
ͼ1 ͼ2
ͼ2
(1)��ͼ1��֪,��ø���͵Ļ����______(��ͼ����ĸ��ʾ),�����������______________________,�����Ч�ʸ��ߡ�
(2)��ϸ������ø�ij�����________,��Ҫ��ԭ����________��
(3)ͼ2�ж�������____���ߵĽ��,����bΪ����_____���Ƽ�������,�ж�������_________________������ͼ2�л��������ø�ļ���������ߡ�________________
(4)�ź��ļ�˵��Ϊ,������ڵ���mRNA�ڷ���ʱ���Ⱥϳɵ���Nĩ�˴�����ˮ������л����ź���,����������Ĥ�ϵ�����ʶ����֮���ϡ��ź��ľ���Ĥ�е������γɵĿ�������������ǻ,��������ת���߶�����ӹ�ʱȴû���˸��ź������С��ݴ����ǿ����ƶ��������п��ܴ��ڵ�ø��������_______________��
(5)�ܵĺ�ϸ���ϳ�ø����Ҫ��ATP��Ҫ��_______(����)������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ��Һ�е���������������ֽ���������еķ�ɢ�����Ӳ�������ֽ�����Կ�������ֽ��������Һ�ͽ���
B. �л�ѧ�����ѻ�ѧ���γɵĹ��̶��ǻ�ѧ�仯
C. ��ɫ��Ӧ�������ȷ�Ӧ
D. ʳ����Һ�ܵ��磬��ʳ����Һ���ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��������A��B��C��D��E��X���ɶ�����Ԫ����ɣ��Ҵ�����ͼת����ϵ�����ַ�Ӧ�������ͷ�Ӧ������ȥ���������ƶϲ���ȷ���ǣ� �� 
A.��DΪ��ɫ����������A��Ħ��������ȣ���Xһ��������
B.��A�ǵ��ʣ�B��D�ķ�Ӧ��OH��+HCO3���TH2O+CO32�� �� ��Eһ���ܻ�ԭCuO
C.��B��X��Ϊ���ʣ�DΪCO��C�ܺ�E��Ӧ����EΪNaOH
D.��X��Na2SO3 �� C����ʹƷ����Һ��ɫ�����壬��A��������������D��E����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������G��һ�ֿ���������������ҩ�ʵ�����ɷ�����A�Ʊ�G�ĺϳ�·�����£�
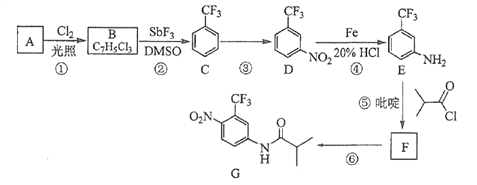
�ش��������⣺
��1��A�Ľṹ��ʽΪ____________��C�Ļ�ѧ������______________��
��2���۵ķ�Ӧ�Լ��ͷ�Ӧ�����ֱ���____________________���÷�Ӧ��������__________��
��3���ݵķ�Ӧ����ʽΪ_______________�������һ���л����������____________��
��4��G�ķ���ʽΪ______________��
��5��H��G��ͬ���칹�壬�䱽���ϵ�ȡ������G����ͬ��λ�ò�ͬ����H���ܵĽṹ��______�֡�
��6��4-����������������![]() ������Ҫ�ľ�ϸ�����м��壬д���ɱ����ѣ�
������Ҫ�ľ�ϸ�����м��壬д���ɱ����ѣ�![]() ���Ʊ�4-���������������ĺϳ�·��___________�������Լ���ѡ����
���Ʊ�4-���������������ĺϳ�·��___________�������Լ���ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�ؼס��ҡ����������졢�����������ڱ��е����λ����ͼ���ײ�һ���ڶ������������ϣ����졢���ֱ��ǿ������ؿ��к�������Ԫ�ء������ж���ȷ����
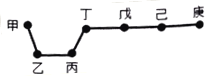
A. ��һ���ǽ���Ԫ��
B. ��̬�⻯����ȶ��ԣ���>��>��
C. �ҡ������������������ˮ������������Ӧ
D. �������������ˮ����������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ������ˮ��Һ��ֻ���ܺ������������е������֣�K+��NH4+��Cl����Mg2+��Ba2+��CO32����SO42�� �� ��ȡ����100mL��Һ��������ʵ�飺 �ٵ�һ�ݼ���AgNO3��Һ�г�������
�ڵڶ��ݼ�����NaOH��Һ���Ⱥ��ռ�������0.04mol
�۵����ݼ�����BaCl2��Һ�ø������6.27g������������ϴ�ӡ������������Ϊ2.33g����������ʵ�飬�����Ʋ���ȷ���ǣ� ��
A.K+��һ������
B.100 mL��Һ�к�0.01 mol CO32��
C.Cl�����ܴ���
D.Ba2+һ�������ڣ�Mg2+���ܴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���а��ֶ���������Ԫ��x��y��z��d��e��f�� g��h������x��y��d��f����ԭ�������ĵ�������ԭ�Ӱ뾶����Դ�С��������ۻ�����۵ı仯��ͼ1��ʾ��z��e��g��h������������Ӧˮ������Һ��Ũ�Ⱦ�Ϊ0.01 mol/L����pH��ԭ�������Ĺ�ϵ��ͼ2��ʾ��
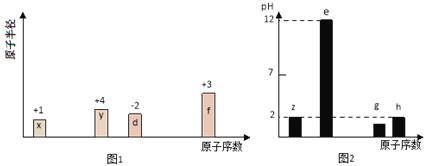
����������Ϣ�����жϣ����ش��������⣺
��1��g��Ԫ�����ڱ��е�λ����____________________��
��2���Ƚ�d��e��f�ļ����Ӱ뾶��СΪ______��______��______�������ӷ��ű�ʾ����y��h ������������Ӧˮ�������Խ�ǿ����__________���û�ѧʽ��ʾ����
��3�����п���Ϊ�Ƚ�e��f������ǿ����������________��
A�����Ũ����Ӧ�Ȼ���ˮ��Һ��pH
B��������Ԫ�ص��ʵ�Ӳ�Ⱥ��ۡ��е�
C���Ƚϵ�������ԭ��ʱʧȥ�ĵ�����Ŀ�Ķ���
D���Ƚ�����Ԫ���ڻ������л��ϼ۵ĸߵ�
E���Ƚϵ�����ͬŨ�����ᷴӦ�ľ��ҳ̶�
��4���ݱ���������������ѧ�һ���˼����о���ֵ��z4������ӽṹ������ӣ�P4������������ṹ���ơ���֪����1 mol z��z������167 kJ����������1 mol Z��Z���ų�942 kJ��������д��z4������һ������������z2���巴Ӧ���Ȼ�ѧ����ʽ___________________��
��5��������Ԫ���е�y��z��e��ɵ�ij�綾������eyz����й¶ʱ��������Աͨ��������������������Һ�ķ�ʽ�������Լ�����Ⱦ����Ӧ����һ����ʽ�κ�һ�����壬��������ˮ���ʼ��ԣ��÷�Ӧ�Ļ�ѧ����ʽΪ___________________________________________����֪eyz����z2���������ƵĻ�ѧ����д��������eyz�ĵ���ʽ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȡ�ͷ�Һʵ����,���в��������п϶�����Ҫ����(����)
A.��Һ©��B.������
C.�ձ�D.�¶ȼ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com