
下列说法正确的是( )
A.吸热反应不加热就不会发生
B.需要加热才能发生的反应一定是吸热反应
C.反应是放热还是吸热必须看反应物和生成物所具有的总能量的相对大小
D.放热的反应在常温下一定很容易发生
考点:反应热和焓变.
专题:化学反应中的能量变化.
分析:A、有的吸热反应不加热也会发生;
B、有的放热反应也需要反应条件;
C、反应物和生成物所具有的总能量的相对大小决定△H的正负;
D、有的放热反应也需要加热.
解答: 解:A、有的吸热反应不加热也会发生,如碳酸氢铵的分解,故A错误;
B、有的放热反应也需要反应条件,如碳的燃烧,故B错误;
C、反应物和生成物所具有的总能量的相对大小决定△H的正负,反应物的总能量大于生成物所具有的总能量为放热反应,反之为吸热反应,故C正确;
D、有的放热反应也需要加热,常温下不容易发生,碳与氧气的反应,故D错误;
故选C.
点评:本题考查了反应过程中的能量变化,注意吸热反应、放热反应的判断及与反应条件无关,题目较简单.


科目:高中化学 来源: 题型:
某澄清、透明的浅黄色溶液中,可能含有下列八种离子:Na+、NH4+、Fe3+、Ba2+、Al3+、SO42﹣、HCO3﹣、I﹣,在设计检验方案前的初步分析中,可确定该溶液中能大量存在的离子最多有( )
A. 4种 B. 5种 C. 6种 D. 7种
查看答案和解析>>
科目:高中化学 来源: 题型:
合理使用药物有利身心健康.下列有关说法错误的是( )
A.氢氧化铝用于治疗胃酸过多
B.维生素C可用于治疗感冒
C.非处方药都无毒副作用,可长期大量服用
D.阿司匹林用于解热镇痛
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在恒容密闭容器中,发生化学反应X(g)+2Y(g)⇌2Z(g).下列说法中:
①X、Y、Z的物质的量之比1:2:2;
②X、Y、Z的浓度不再发生变化;
③容器中的压强不再发生变化;
④单位时间内生成n molZ,同时生成2n mol Y,
一定达到化学平衡状态的是( )
A.②③ B.①④ C.①② D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出了杰出贡献,荣获2010年度国家最高科学技术奖.
①合金是生活中常见的材料.某合金具有密度小、强度高的优良性能,常用于制造门窗框架.该合金中含量最高的金属为 (填元素符号).
②铁锈的主要成分是 (填化学式),它是钢铁在潮湿的空气中发生吸氧腐蚀的结果.
③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有CaCO3、 和 (填化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列描述中,不符合生产实际的是( )
A.电解熔融的氧化铝制取金属铝,用铁作阳极
B.电解法精炼粗铜,用纯铜作阴极
C.电解饱和食盐水制烧碱,用石墨作阳极
D.在镀件上电镀锌,用锌作阳极
查看答案和解析>>
科目:高中化学 来源: 题型:
据环保部门测定,我国一些大城市的酸雨pH约为3.5.在酸雨季节铁制品极易腐蚀,下列说法正确的是( )
A.腐蚀中正极反应为:2H++2e﹣=H2↑
B.腐蚀中负极反应为:Fe﹣3e﹣=Fe3+
C.钢铁设备上连接铜块可以防止腐蚀
D.钢铁与外加直流电源的正极相连可以防止腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇的研究成为当代社会的热点.
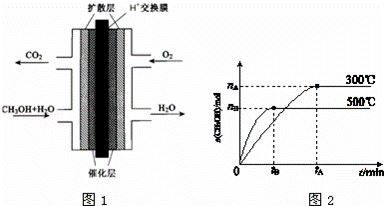
Ⅰ.甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源.
(1)101kP a时,1mol CH3OH完全燃烧生成稳定的氧化物放出热量726.51kJ/mol,则甲醇燃烧的热化学方程式为 .
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H1=+49.0kJ•mol﹣1
②CH3OH(g)+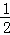 O2(g)=CO2(g)+2H2(g)△H2
O2(g)=CO2(g)+2H2(g)△H2
已知H2(g)+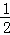 O2(g)=H2O(g)△H=﹣241.8kJ•mol﹣1
O2(g)=H2O(g)△H=﹣241.8kJ•mol﹣1
则反应②的△H2= kJ•mol﹣1.
(3)甲醇燃料电池的结构示意图如图1.甲醇进入 极(填“正”或“负”),正极发生的电极反应为 .负极发生的电极反应为 .
Ⅱ.一定条件下,在体积为3L的密闭容器中反应CO(g)+2H2(g)⇌CH3OH(g)达到化学平衡状态.
(1)该反应的平衡常数表达式K= ;根据图2,升高温度,K值将 (填“增大”、“减小”或“不变”).
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是 mol•L﹣1•min﹣1(用nB、tB表示).
(3)判断该可逆反应达到化学平衡状态的标志是 (填字母).
a.v生成(CH3OH)=v消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的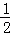 ,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).
,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).
a.c(H2)减少 b.正反应速率加快,逆反应速率减慢
c.CH3OH 的物质的量增加 d.重新平衡时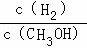 减小.
减小.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是( )
|
| A. | FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ |
|
| B. | NO2与水的反应:3NO2+H2O═2NO3﹣+NO+2H+ |
|
| C. | 醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
|
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2﹣+CO2+3H2O═2Al(OH)3↓+CO32﹣ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com