
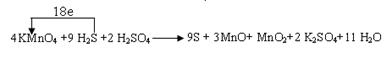 (4分)
(4分) 。根据原子守恒可知,KMnO4系数为4,H2S系数为9,K2SO4的系数为2,H2SO4的系数为2,H2O的系数为11,因此配平后方程式为:4KMnO4+9H2S+2H2SO4=9S+3MnO+MnO2+2K2SO4+11H2O,则反应中转移电子数目为9×[0-(-2)]=18,所以标出电子转移方向与数目为
。根据原子守恒可知,KMnO4系数为4,H2S系数为9,K2SO4的系数为2,H2SO4的系数为2,H2O的系数为11,因此配平后方程式为:4KMnO4+9H2S+2H2SO4=9S+3MnO+MnO2+2K2SO4+11H2O,则反应中转移电子数目为9×[0-(-2)]=18,所以标出电子转移方向与数目为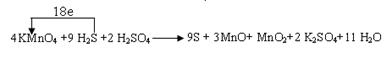 。
。

 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源:不详 题型:填空题
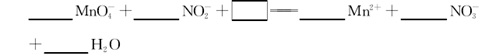
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在该反应中NaIO3作还原剂 |
| B.碱性条件下,氯气氧化性强于Na2H3IO6 |
| C.反应中生成1mol Na2H3IO6,转移2mol电子 |
| D.反应中氧化产物与还原产物的物质的量比为2:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 xOH-+ N2+4H2O。下列有关说法正确的是
xOH-+ N2+4H2O。下列有关说法正确的是| A.该反应为置换反应 |
| B.每生成1mol N2,反应转移5mole- |
| C.x=2 |
| D.反应过程中溶液pH减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 AlN+3HCl反应中,该方法比前者在生产上更具优势。下列说法中,正确的是 。
AlN+3HCl反应中,该方法比前者在生产上更具优势。下列说法中,正确的是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是 。
HNO3。写出OH与NO反应的化学方程式:_____________,该反应中被氧化的元素是 。
 SO32-+____N2+____
SO32-+____N2+____

 SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为 。
SO42-+4H+,阴极生成的吸收液每吸收标准状况下7.84 L的气体,阳极区新生成质量分数为49%的硫酸100 g,则被吸收气体中NO2和NO的物质的量之比为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.胶体:组成物质的直径是否在1nm~100nm之间 |
| B.氧化还原反应:反应前后元素的化合价是否发生了变化 |
| C.共价化合物:组成化合物的元素是否全部都是非金属元素 |
| D.化学变化:是否有热效应、颜色变化、气体或沉淀生成等四种实验现象 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只表现氧化性 | B.只表现还原性 |
| C.既表现氧化性又表现酸性的是 | D.既表现氧化性又表现还原性的是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com