
����A��B��C��D��E��F��G��H��M�������ʣ�����AΪ����ɫ��ĩ��GΪ����ɫ���嵥�ʣ�EΪ��ɫ���嵥�ʣ�F��ˮ��Һ��ʯ��ˮ��Ͽɵ�D����Һ������֮����ת����ϵ��ͼ��ʾ�����������ص������������ȥ��
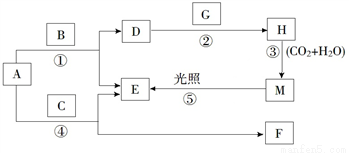
��ش��������⣺
��1��д��G��H�Ļ�ѧʽ��G__________��H__________��
F��������_________________��A����Ҫ��;��________________��
��2��д����Ӧ�٢ڵ����ӷ���ʽ��
��____________________��
��____________________��
��3����֪CN��(�������))��Cl��������֮���������(CN)2��������Cl2������������֮�����ҳ��³�ѹ�������塣��д��MnO2��HCN��Һ���ȷ�Ӧ�Ļ�ѧ����ʽ��_______________��
��4��������ͼװ�ý���ʵ�飬֤��������ǿ����KMnO4>Cl2>Br2��
��ѡ�Լ���KBr��Һ��KMnO4��Ũ���ᡢŨ���ᡣ
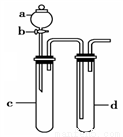
��֪��2KMnO4+16HCl(Ũ)=2KCl+ 2MnCl2+5Cl2��+8H2O
��ش��������⣺
��װ��a ��d��ʢ�ŵ��Լ��ֱ���__________��__________��
��ʵ���й۲쵽������Ϊ_____________________��
�۴�ʵ��װ�õIJ���֮����_____________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����������������ѧ���״κϳɵ�117��Ԫ�أ���������ʱ�����ܿ���ѡΪ����ʮ���ѧ���֡������117��Ԫ�ط�����ʱ��ΪUp�����й��� ��
�� ˵������ȷ���ǣ�������
˵������ȷ���ǣ�������
A.  ��
�� ������Ԫ�� B.
������Ԫ�� B.  ��
�� ��Ϊͬλ��
��Ϊͬλ��
C.  ��
�� ��������ͬ����������ͬ D.
��������ͬ����������ͬ D.  ��
�� ��������ͬ����������ͬ
��������ͬ����������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ��ͨ�и����߿�ȫ��ģ�⣨�壩��ѧ �Ծ��������棩 ���ͣ��ƶ���
G��һ���������ϵ���Ҫ�ɷ�֮һ����ṹ�к���������Ԫ����G�ĺϳ�·�����£����ֲ���Ͳ��ַ�Ӧ������ȥ����
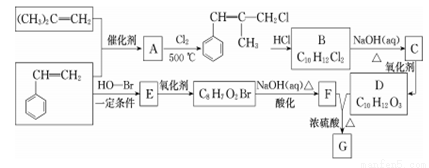
��֪���� RCH=CH2+CH2=CHR?----CH2=CH2+RCH=CHR?��
�� B�ĺ˴Ź�������ͼ��ʾ��������6 �ֲ�ͬ��������ԭ�ӣ�
��D��F��Ϊͬϵ�
��1��(CH3)2C=CH2����������ͬһƽ���ڵ�ԭ�������Ϊ_____��D�����к��еĺ���������������________��
��2��A��B��Ӧ�������漰�ķ�Ӧ��������Ϊ______��_______��
��3��E�Ľṹ��ʽΪ_______��G�Ľṹ��ʽΪ________��
��4��B��C�Ļ�ѧ����ʽΪ___________________��
��5��д��ͬʱ��������������F��һ��ͬ���칹��Ľṹ��ʽ__________��
������FeCl3��Һ������ɫ��Ӧ���� ������������ȡ�������ܷ���ˮ�ⷴӦ��
����˴Ź�������ͼ����4 ��塣
��6��ģ���ɱ���ϩ�ϳ�F�ķ�����д���ɱ�ϩ��ȡ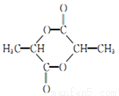 �ĺϳ�·�ߣ�_______��
�ĺϳ�·�ߣ�_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������к�����2017�����һģ��ѧ�Ծ� ���ͣ������
MgH2��Mg2Cu������������ϣ�MgO������¯���������������Լ���
��1��MgH2��һ�����ӻ���������ʽΪ_______________��
��2��Mg2Cu�ڼ�ѹ�����´���ʱ����MgH2��MgCu2,�÷�Ӧ�Ļ�ѧ����ʽΪ_____________��
��3����֪MgH2���й��Ȼ�ѧ����ʽ���£�
MgH2(s) =Mg(s)+H2(g) ��H1=+74.4kJ • mol-1��
H2(g)+l/2O2(g)=H2O(g) ��H2=-241.8 kJ • mol-1��
Mg(s)+l/2O2(g)=MgO(s) ��H3=-141.6 KJ • mol-1��
���⻯þȼ����������þ��ˮ�������Ȼ�ѧ����ʽΪ______________��
��MgH2���������ʱ����λ��������ͷų�������������ʱ��ı仯��ͼ����ʾ�������¶�T1��T2��T3��С�����˳��Ϊ__________________��

��4��¯�����ѳ� SO2��NO ��ӦΪ2MgO(s)+2SO2(g)+2NO(g) 2MgSO4(s)+N2(g) ��H =akJ/ mol����ƽ�ⳣ�����¶ȵĹ�ϵ��ͼ����ʾ��
2MgSO4(s)+N2(g) ��H =akJ/ mol����ƽ�ⳣ�����¶ȵĹ�ϵ��ͼ����ʾ��
��������Ӧ��ƽ�ⳣ������ʽΪK=_________��
��a_________0(�>����,<��)��
��5��ȫ��̬����ӵ�صĽṹ��ͼ����ʾ���ŵ�ʱ��ط�ӦΪ2Li+MgH2=Mg+2LiH���ŵ�ʱ��X���ĵ缫��ӦʽΪ_________�����ʱ��Y���ĵ缫��ӦʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������к�����2017�����һģ��ѧ�Ծ� ���ͣ�ѡ����
����ʵ���У���ѡװ�ò���������

A. �����ᴿ��ѡ�ٺ͢�
B. ��CCl4��ȡ��ˮ�еĵ⣬ѡ��
C. ����Na2CO3��Һ��CH3COOC2H5��ѡ��
D. ��NaOH��Һ��������Cl2ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ���ݰ�һ�С�Ȫ��ʵ����ѧ��һ��ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ˮ���˺��Ժ��п����Ե� ��
�� ��
�� �����ʣ�ͨ�����¼���ʵ�鲽����Գ�ȥ��Щ���ʡ�
�����ʣ�ͨ�����¼���ʵ�鲽����Գ�ȥ��Щ���ʡ� �����Թ�����
�����Թ����� ��Һ��
��Һ�� �����Թ�����
�����Թ����� ��Һ��
��Һ�� �����Թ�����
�����Թ����� ��Һ��
��Һ�� ���ˣ�
���ˣ� ����ϡ�����������ݲ�������ȷ�IJ���˳���ǣ� ��
����ϡ�����������ݲ�������ȷ�IJ���˳���ǣ� ��
A. �٢ۢڢܢ� B. �ۢڢ٢ܢ� C. �ڢۢ٢ݢ� D. �ۢܢڢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ���ݰ�һ�С�Ȫ��ʵ����ѧ��һ��ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���������Һ��ͨ��������CO2�����Ա仯���ǣ� ��
A. NaOHϡ��Һ B. NaAlO2��Һ C. ����NaHCO3��Һ D. CaCl2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ��һ��ѧ�ڵ�һ�Σ�3�£��μ�⻯ѧ�Ծ��������棩 ���ͣ������
һ����̼���㷺Ӧ����ұ��ҵ�͵��ӹ�ҵ��
��1����֪CO��ȼ����Ϊ283kJ/mol����д������COȼ���ȵ��Ȼ�ѧ����ʽ___________��
��2����¯��������Ϊ�ձ��������������ط�Ӧ���Ȼ�ѧ����ʽ���£�
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s)��H=akJ/mol
CO(g)+Fe2O3(s)= CO2(g)+2Fe3O4(s)��H=bkJ/mol
��д��COֱ�ӽ�Fe2O3��ԭΪFe���Ȼ�ѧ����ʽ��____________���ú�a,b�Ĵ���ʽ��ʾ��H����ֵ����
��3��ʹ�õ绯ѧһ����̼���崫����������������CO��������ṹ����ͼ��ʾ�����ִ���������ȼ�ϵ��ԭ������õ�صĸ�����ӦʽΪ_________��
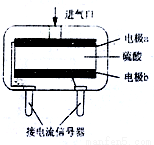
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶���ѧ�ʼ죨3�£���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���У���ȷ���ǣ� ��
A. �������м��백ˮ�����ԣ���Һ��c��NH4+��/ c��C l�� ��=1
B. 25��ʱ��Mg��OH��2������20 mL 0.01mol•L��1��ˮ�е�Ksp����20mL0.01mol•L��1 NH4Cl��Һ�е�KspС
C. pH��ֽ���������ˮ��pHΪ4.5
D. FeCl3��Һ��Fe2��SO4��3��Һ�������ɡ����ն��õ�Fe2O3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com