
(12分)在不同温度下,反应CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数K如下表:
CO(g)+H2O(g)的平衡常数K如下表:
|
温度/℃ |
700 |
800 |
850 |
1000 |
1200 |
|
平衡常数K |
2.6 |
1.7 |
1 |
0.9 |
0.6 |
(1)该反应的△H 0。(填“>”、“=”或“<”)。若到达平衡后升高温度,则CO2的转化率将 ,正反应速率 (填“增大”、“减小”或“不变”)。
(2)850℃时发生上述反应,CO2的转化率随时间变化如图所示。其他条件相同时,请在下图中画出700℃时CO2的转化率随时间变化的示意图(注明必要的标示)。
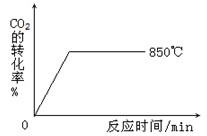
(3)在850℃时发生上述反应,以下表中的物质的量投入恒容反应器,其中向正方向移动的组是 (填代号),平衡后与C中各物质的百分含量相等的组有__________(填代号 )
|
|
A |
B |
C |
D |
E |
|
n(CO2)[ |
3 |
1 |
0 |
1 |
1 |
|
n(H2) |
2 |
1 |
0 |
1 |
2 |
|
n(CO) |
1 |
2 |
3 |
0.5 |
3 |
|
n(H2O) |
5 |
2 |
3 |
0.5 |
1 |
(4) 850℃时,在1L的密闭容器中分别充入2mol的CO2和H2,计算反应到达平衡时CO的物质的量浓度。(写出计算过程)
(1)<,减小,增大(各1分)
(2)如下图(2分)(标注及拐点要明确)

(3)AD BD(每空2分)
(4) (5分) 解: 设平衡时CO的浓度为x
CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
起始浓度(mol·L-1) 2 2 0 0
转化浓度(mol·L-1) x x x x
平衡浓度(mol·L-1)(2-x)(2-x) x x (2分)
则:K= (1分)
(1分)
解得:x =1 即平衡时c(CO) =1 mol·L-1(2分)
【解析】(1)反应CO2(g)+H2(g) CO(g)+H2O(g)的平衡常数K=
CO(g)+H2O(g)的平衡常数K= ,随温度升高而减小,说明平衡左移,正反应是放热反应,该反应的△H<0。若到达平衡后升高温度,则CO2的转化率将减小,正逆反应速率均增大。
,随温度升高而减小,说明平衡左移,正反应是放热反应,该反应的△H<0。若到达平衡后升高温度,则CO2的转化率将减小,正逆反应速率均增大。
(2)注意两点:一是温度越高,反应速率越大,越先达到平衡;再有降低温度,则CO2的转化率将增大。
(3)850℃时K=1,所以 <1时,AD符合题意。
<1时,AD符合题意。
CO2(g)+H2(g) CO(g)+H2O(g)属于两边气体系数相等的可逆反应,依据等效平衡的判断标准可知,只需按照系数比转换为半边,反应物的物质的量比例相同即可,故答案为BD
CO(g)+H2O(g)属于两边气体系数相等的可逆反应,依据等效平衡的判断标准可知,只需按照系数比转换为半边,反应物的物质的量比例相同即可,故答案为BD
(4)见答案


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 一定条件下,在体积为V L的密闭容器中,一氧化碳和氢气反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图表示该反应在不同温度下的反应过程.关于该反应,下列说法正确的是( )
一定条件下,在体积为V L的密闭容器中,一氧化碳和氢气反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图表示该反应在不同温度下的反应过程.关于该反应,下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
 (2010?广东)硼酸(H3BO3)在食品、医药领域应用广泛.
(2010?广东)硼酸(H3BO3)在食品、医药领域应用广泛. B(OCH3)3+3H2O中,H3BO3的转化率(a)在不同温度下随反应时间(t)的变化见图,由此图可得出:
B(OCH3)3+3H2O中,H3BO3的转化率(a)在不同温度下随反应时间(t)的变化见图,由此图可得出: [B(OH)4]-( aq)+H+(aq)已知0.70mol?L-1 H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0×10-5mol?L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)
[B(OH)4]-( aq)+H+(aq)已知0.70mol?L-1 H3BO3溶液中,上述反应于298K达到平衡时,c平衡(H+)=2.0×10-5mol?L-1,c平衡(H3BO3)≈c起始(H3BO3),水的电离可忽略不计,求此温度下该反应的平衡常数K(H2O的平衡浓度不列入K的表达式中,计算结果保留两位有效数字)查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
| c(CO) |
| c(CO2) |
| c(CO) |
| c(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知可逆反应:X(g)+Y(g)?E(g),现将X和Y按一定比例混合,其他条件不变时,在不同温度下,反应混合物中X体积分数的变化曲线如图所示.请分析图象并回答下列问题:
已知可逆反应:X(g)+Y(g)?E(g),现将X和Y按一定比例混合,其他条件不变时,在不同温度下,反应混合物中X体积分数的变化曲线如图所示.请分析图象并回答下列问题:查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省菏泽市高三3月模拟(一模)考试理综化学试卷(解析版) 题型:填空题
工业制硫酸的过程中利用反应2SO2(g)+O2(g) 2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
(1)一定条件下,向一带活塞的密闭容器中充入2 mol SO2和1mol O2发生反应,则下列说法正确的是??????????????????? 。
A.若反应速率v (SO2) ﹦v (SO3),则可以说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,充入2 mol N2,化学反应速率加快
C.平衡后仅增大反应物浓度,则平衡一定右移,各反应物的转化率一定都增大
D.平衡后移动活塞压缩气体,平衡时SO2、O2的百分含量减小,SO3的百分含量增大
E.平衡后升高温度,平衡常数K增大
F.保持温度和容器体积不变,平衡后再充入2molSO3,再次平衡时各组分浓度均比原平衡时的浓度大
(2)将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | |||
1 | T1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | 4 | 2 | 0.4 | y | 9 |
①实验1从开始到反应达到化学平衡时,v(SO2)表示的反应速率为??????? ,? 表中y? ﹦?????? 。
②T1????????????????? T2 ,(选填“>”、“<”或“=”), 实验2中达平衡时 O2的转化率为???????????????? 。
(3)尾气SO2用NaOH溶液吸收后会生成Na2SO3。现有常温下0.1 mol/L Na2SO3溶液,实验测定其pH约为8,完成下列问题:
① 该溶液中c(Na+)与 c(OH-) 之比为???????????????????????????????????????? 。
② 该溶液中c(OH-) = c(H+)+ ???????????? + ????????????? (用溶液中所含微粒的浓度表示)。
③ 当向该溶液中加入少量NaOH固体时,c(SO32-)???????????????? , 水的离子积Kw? ??? ??????????????? 。(选填“增大”、“减小”或“不变”)
(4)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是 ????????????????????????????????????????????? 。
A. Na2CO3???????? ?? B. Ba(NO3)2 ??????????? C.Na2S???????? D.酸性KMnO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com