
【题目】某活动小组利用废铁屑(含少量S等元素)为原料制备硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O],设计如图所示装置(夹持仪器略去)。

称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50~60°C热水浴中加热.充分反应。待锥形瓶中溶液冷却至室温后加入氨水,使其反应完全,制得浅绿色悬浊液。
(1)在实验中选择50~60° C热水浴的原因是___________
(2)装置B的作用是______________;KMnO4溶液的作用是______________。
(3)若要确保获得浅绿色悬浊液,下列不符合实验要求的是_________(填字母)。
a.保持铁屑过量 b. 控制溶液呈强碱性 c.将稀硫酸改为浓硫酸
(4)检验制得的(NH4)2SO4·FeSO4·6H2O中是否含有Fe3+的方法:将硫酸亚铁铵晶体用加热煮沸过的蒸馏水溶解,然后滴加_______(填化学式)。
(5)产品中杂质Fe3+的定量
①配制Fe3+浓度为0.1 mg/mL的标准溶液100 mL。称取______ (精确到0.1)mg高纯度的硫酸铁铵[(NH4)Fe(SO4)2·12H2O],加入20.00 mL经处理的去离子水。振荡溶解后,加入2 mol·L-1HBr溶液1mL和1mol·L-1KSCN溶液0.5mL,加水配成100mL溶液。
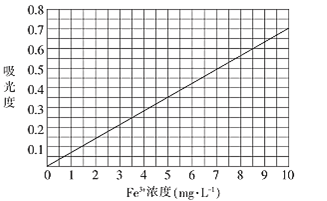
②将上述溶液稀释成浓度分别为0.2、1.0、3.0、5.0、7.0、10.0(单位:mg·L-1)的溶液。分别测定不同浓度溶液对光的吸收程度(吸光度),并将测定结果绘制成如图所示曲线。取硫酸亚铁铵产品,按步骤①配得产品硫酸亚铁铵溶液10mL,稀释至100mL,然后测定稀释后溶液的吸光度,两次测得的吸光度分别为0.590、0.610,则该兴趣小组所配产品硫酸亚铁铵溶液中所含Fe3+浓度为_______mg·L-1。
(6)称取mg产品,将产品用加热煮沸的蒸馏水溶解,配成250mL溶液,取出100mL放入锥形瓶中,用cmol·L-1KMnO4溶液滴定,消耗KMnO4溶液VmL,则硫酸亚铁铵晶体的纯度为_____ (用含c、V 、m的代数式表示)。
【答案】使受热均匀,加快反应速率,防止温度过高,氨水挥发过多,原料利用率低 防止液体倒吸进入锥形瓶 吸收氨气、硫化氢等杂质气体,防止污染空气 bc KSCN 86.1 85 ![]()
【解析】
A中稀硫酸与废铁屑反应生成硫酸亚铁、氢气,还有少量的硫化氢气体,滴加氨水,可生成硫酸亚铁铵,B导管短进短出为安全瓶,避免倒吸,C用于吸收硫化氢等气体,避免污染环境,气囊可以吸收氢气。
(1)水浴加热的目的是控制温度,加快反应的速率,同时防止温度过高,氨水挥发过多,原料利用率低,故答案为:使受热均匀,加快反应速率,防止温度过高,氨水挥发过多,原料利用率低;
(2)B装置短进短出为安全瓶,可以防止液体倒吸进入锥形瓶;由于铁屑中含有S元素,因此会产生H2S,同时氨水易挥发,因此高锰酸钾溶液(具有强氧化性)吸收这些气体,防止污染空气,吸收氨气、硫化氢等杂质气体,防止污染空气,故答案为:防止液体倒吸进入锥形瓶;吸收氨气、硫化氢等杂质气体,防止污染空气;
(3)由于Fe2+易被氧化,所以为防止其被氧化,铁屑应过量,同时为抑制Fe2+的水解,所以溶液要保持强酸性,浓硫酸常温下会钝化铁,故答案为:bc;
(4)检验铁离子常用KSCN溶液,故答案为:KSCN;
(5)①在Fe3+浓度为1.0mg/mL的标准溶液100mL中,m(Fe3+)=0.1mg/mL×100mL=10.0mg,依据关系式Fe3+~(NH4)Fe(SO4)212H2O得:m[(NH4)Fe(SO4)212H2O]=10.0mg×![]() =86.1mg,故答案为:86.1;
=86.1mg,故答案为:86.1;
②两次测定所得的吸光度分别为0.590、0.610,取其平均值为0.600,从吸光度可以得出浓度为8.5 mg/L,又因配得产品溶液10mL,稀释至100 mL,故原产品硫酸亚铁铵溶液中所含Fe3+浓度为:8.5mg/L×![]() =85mg/L,故答案为:85;
=85mg/L,故答案为:85;
(6)滴定过程中Fe2+被氧化成Fe3+,化合价升高1价,KMnO4被还原生成Mn2+,所以有数量关系5 Fe2+~ KMnO4,所以n[(NH4)2SO4·FeSO4·6H2O]=V×10-3L×cmol·L-1×5×![]() =12.5Vc10-3mol,则硫酸亚铁铵晶体的纯度为
=12.5Vc10-3mol,则硫酸亚铁铵晶体的纯度为![]() ×100%=
×100%=![]() ;故答案为:
;故答案为:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
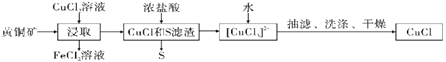
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)(无色溶液),下列叙述错误的是( )
[CuCl3]2-(aq)(无色溶液),下列叙述错误的是( )
A.浸取阶段,参加反应的CuFeS2和CuCl2的物质的量之比为3:l
B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板
C.加水有利于CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)平衡逆向移动,析出CuCl
[CuCl3]2-(aq)平衡逆向移动,析出CuCl
D.为提高产率和纯度,可采用乙醇洗涤、真空干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烷基取代苯![]() 可以被KMnO4的酸性溶液氧化生成
可以被KMnO4的酸性溶液氧化生成![]() ,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到![]() 。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为
。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为![]() 的异构体共有7种,其中的3种是
的异构体共有7种,其中的3种是![]() 、
、![]() 、
、![]() 。请写出其他4种的结构简式:_________________、________________、_________________、___________________。
。请写出其他4种的结构简式:_________________、________________、_________________、___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知钴酸锂电池的总反应方程式为Li1-xCoO2+LixC6=LiCoO2+6C。用该电池作电源按如图所示装置进行电解。通电后,电极a上一直有气泡产生,电极d附近先出现白色沉淀(CuCl),t min后白色沉淀全部转变成橙黄色沉淀(CuOH)。下列有关叙述不正确的是

A.钴酸锂电池放电时的正极反应为Li1-xCoO2 +xe- +xLi+=LiCoO2
B.当电极a处产生标准状况下气体2. 24 L时。钴酸锂电池负极质量减少1.4g
C.电极d为阳极,电解开始时电极d的反应式为Cu+C1-- e- =CuCl
D.电解tmin后.装置II中电解质溶液的pH显著增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含苯酚的工业废水的处理流程如图所示。
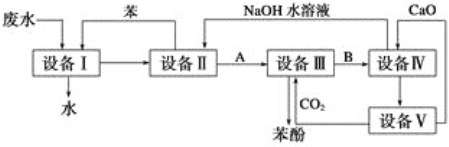
(1)①流程图设备Ⅰ中进行的是操作________(填写操作名称)。实验室里这一步操作可以用_______(填仪器名称)进行。
②由设备Ⅱ进入设备Ⅲ的物质A是______________(填化学式,下同)。由设备Ⅲ进入设备Ⅳ的物质B是___________。
③在设备Ⅲ中发生反应的化学方程式为_____________________。
④在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和______。通过 _________________(填操作名称)操作,可以使产物相互分离。
⑤图中,能循环使用的物质是_______、_____________C6H6和CaO。
(2)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是____________。
从废水中回收苯酚的方法是①用有机溶剂萃取废液中的苯酚;②加入某种药品的水溶液使苯酚与有机溶剂脱离;③加入某物质又析出苯酚。试写出②、③两步的反应方程式:_________________________。
(3)为测定废水中苯酚的含量,取此废水100 mL,向其中加入浓溴水至不再产生沉淀为止,得到沉淀0.331 g,求此废水中苯酚的含量____________(mg·L-1)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏伽德罗常量的值,最早由奥地利化学及物理学家JohannJosefLoschmidt测得,有时候用L代替NA表示阿伏伽德罗常量的值,下来说法错误的是
A.1.1g的11B中,含有0.6L个中子
B.pH=1的H3PO4溶液中,含有0.1L个H+
C.标准状态下的33.6L氯气与27g铝充分反应,转移电子数为3L
D.1L1mol/LNaCl溶液和1L1mol/LNaF溶液中离子总数:前者大于后者
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机物合成中的重要试剂,为红褐色液体或黄色气体,具有刺鼻恶臭味,遇水反应生成一种烈化物和两种氧化物。某学习小组在实验用C12和NO制备NOCl并测定其纯度,相关实验(装置略去)如下。请回答:
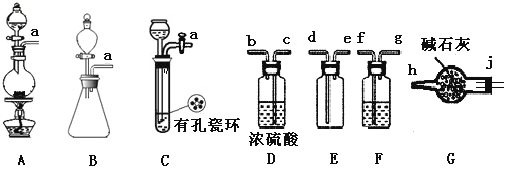
(1)制备Cl2发生装置可______ (填大写字母),反应的离子方程式为_______。
(2)欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→________(按气流方向,用小写字母表示),若用到F,其盛装药品为_________。
(3)实验室可用下图装置制备亚硝酰氯(NOCl)
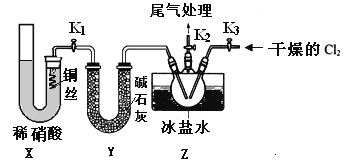
①实验室也可用B装置制备NO,上图X装置的优点为__________(至少写出两点)
②检验装置气密性并装入药品,打开k2,然后再打开____(填“k1”或“k3”),通入一段时间气体,其目的为________,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装肖Y,则Z中NOCl可能发生反应的化学方程式为_________
(4)取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol/LAgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL.已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12,则亚硝酰氯(NOC1)的质量分数为____(用代数式表示,不必化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
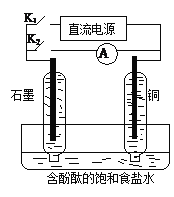
A. 断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl—![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl—
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K=c(CO)c(H2O)/c(CO2)c(H2),恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应的ΔH>0
B.恒温恒容条件下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应的化学方程式为CO+H2O![]() CO2+H2
CO2+H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com