
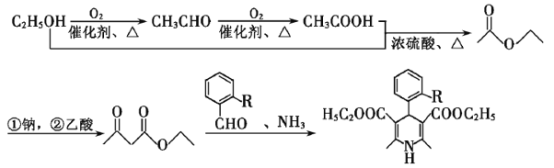
【题目】硝苯地平H是一种治疗高血压的药物;其一种合成路线如下:

已知:酯分子中的a-碳原子上的氢比较活泼,使酯与酯之间能发生缩合反应。
![]()
回答下列问题:
(1)B的化学名称为________.
(2)②的反应类型是________.
(3)D的结构简式为________.
(4)H的分子式为________.
(5)反应①的化学方程式为________.
(6)已知M与G互为同分异构体,M在一定条体下能发生银镜反应,核磁共振氢谱显示有4组峰,峰面积之比为1:1:2:4,写出M的一种可能的结构简式________.
(7)拉西地平 也是一种治疗高血压药物,设以乙醇和
也是一种治疗高血压药物,设以乙醇和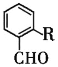 为原料制备拉西地平的合成路线(无机试剂任选)。________________________
为原料制备拉西地平的合成路线(无机试剂任选)。________________________
【答案】邻硝基甲苯 取代反应 ![]() C17H18N2O6
C17H18N2O6 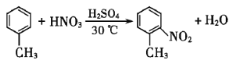
![]()
【解析】
A→B为取代反应,引入硝基,B→C引入酯基结构,C中酯基在酸性条件下水解得到D(![]() ),D中取代结构被高锰酸钾氧化为E中醛基,由题目已知两分子F发生缩合反应得到G。
),D中取代结构被高锰酸钾氧化为E中醛基,由题目已知两分子F发生缩合反应得到G。
(1)硝基和甲基为邻位关系,故B的化学名称为邻硝基甲苯;
(2)对比B、C结构,可知②的反应类型为取代反应;
(3)由分析知D为![]() ;
;
(4)H分子式为C17H18N2O6;
(5)反应①取代反应引入硝基: ;
;
(6)M在一定条体下能发生银镜反应,则考虑其中包含醛基或甲酸酯的结构,故M可能为![]() ;
;
(7)参考题干酯与酯之间能发生缩合反应,以及E、G和NH3生成H的原理,可知合成路线为: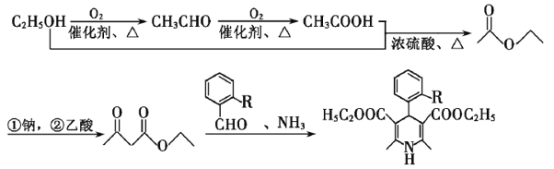 。
。


科目:高中化学 来源: 题型:
【题目】短周期主族元素 W、X、Y、Z的原子序数依次增大,W 在大气中有两种同素异形体且均能支持燃烧,X 的原子半径是所有短周期主族元素中最大的,非金属元素 Y 的原 子序数是 Z 的最外层电子数的 2 倍。下列叙述不正确的是
A.Y、Z的氢化物稳定性 Y> Z
B.Y单质的熔点高于X 单质
C.X、W、Z 能形成具有强氧化性的 XZW
D.YZ4分子中 Y 和 Z 都 满足8 电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】十九大报告提出要对环境问题进行全面、系统的可持续治理。绿色能源是实施可持续发展 的重要途径,利用生物乙醇来制取绿色能源氢气的部分反应过程如图所示:
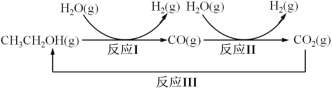
(1)已知:CO(g)+H2O(g) ![]() CO2(g)+H2(g) △H1= - 41 kJ/mol
CO2(g)+H2(g) △H1= - 41 kJ/mol
CH3CH2OH(g)+3H2O(g) ![]() 2CO2(g)+6H2(g) △H2=+174.1 kJ/mol
2CO2(g)+6H2(g) △H2=+174.1 kJ/mol
请写出反应 I 的热化学方程式____________。
(2)反应 II,在进气比[n(CO) : n(H2O)]不同时,测得相应的 CO 平衡转化率见图(各点对应的反应温度可能相同,也可能不同;各点对应的其他反应条件都相同)。

①经分析,A、E 和 G 三点对应的反应温度相同,其原因是 KA=KE=KG=____________(填数值)。在该温度下:要提高 CO平衡转化率,除了改变进气比之外,还可采取的措施是____________。
② 对比分析 B、E、F 三点,可得出对应的进气比和反应温度的变化趋势之间的关系是____________。
③ 比较 A、B 两点对应的反应速率大小:VA____________VB(填“<” “=”或“>”)。已知反应速率 v=v 正v 逆= k正X(CO)X(H2O)-k逆X(CO2)X(H2),k 正、k 逆分别为正、逆向反应速率常数,X为物质的量分数计算在达到平衡状态为D点的反应过程中,当CO转化率刚好达到20%时,![]() =_____________(计算结果保留1位小数)。
=_____________(计算结果保留1位小数)。
(3)反应 III 利用碳酸钾溶液吸收 CO2 得到饱和 KHCO3 电解液,电解活化的 CO2 来制备乙醇。
①已知碳酸的电离常数 Ka1=10-a mol·L1,Ka2=10-b mol·L1,吸收足量 CO2 所得饱和 KHCO3 溶液的 pH=c,则该溶液中lg![]() =________________
=________________
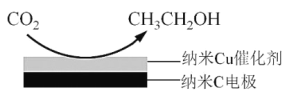
②在饱和 KHCO3 电解液中电解 CO2 来制备乙醇的原理如图所示。则阴极的电极反应式是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 分子的结构是由键角决定的
B. H2O分子中的两个O—H键的键角为180°
C. CF4、CCl4、CBr4、CI4中C—X键的键长、键角均相等
D. 共价键的键能越大,共价键越牢固,由该键形成的分子越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种短周期元素的原子序数依次增大,A 的一种核素在考古时常用来鉴定一些文物的年代,B的气态氢化物的水溶液呈碱性;C为金属元素且有两种常见含氧化合物(都含两种元素);若往D单质的水溶液中滴加少量紫色石蕊溶液,可观察到先变红后褪色。下列说法中正确的是( )
A.C的两种含氧化合物中阴、阳离子个数比都为1∶2
B.最高价氧化物对应的水化物的酸性:B>D
C.B的氢化物的沸点一定高于A的氢化物
D.电负性:D>B>A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备(NH4)2Fe(SO4)2·6H2O 的实验中,需对过滤出产品的母液(pH<1)进行处理。室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是
A.通入过量Cl2:Fe2+、H+、![]() 、Cl、
、Cl、![]()
B.加入少量NaClO溶液:![]() 、Fe2+、H+、
、Fe2+、H+、![]() 、ClO
、ClO
C.加入过量NaOH 溶液:Na+、Fe2+、![]() 、
、![]() 、OH
、OH
D.加入过量NaClO和NaOH的混合溶液:Na+、![]() 、Cl、ClO、OH
、Cl、ClO、OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
A.方案①用于分离I2和NH4I固体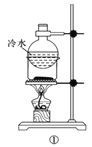
B.方案②用于比较CuSO4和MnO2的催化活性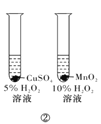
C.方案③用于测定中和热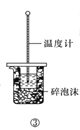
D.方案④用于比较醋酸和硼酸的酸性强弱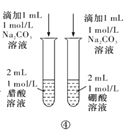
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的太阳能电池有单晶硅或多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。请回答下列问题:
(1)基态硒原子的价电子排布式为___;H2O的沸点高于H2Se的沸点(-42℃),其原因是___。
(2)已知GaCl3晶体熔点为77.9℃,沸点为201.3℃,GaCl3品体类型为____。
(3)Na3AsO4中阴离子的空间构型为_____,As原子采取_____杂化。
(4)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因:_____。
(5)锌与铜位于同一周期。硫化锌的晶胞结构如图所示,S2-周围等距离且最近的Zn2+个数为____;若晶胞边长为dpm,则硫化锌的密度为____g·cm-3(不必简化)。
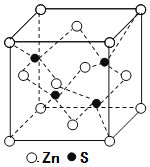
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。有关该电池的说法正确的是( )
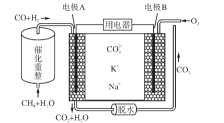
A. 反应CH4+H2O![]() 3H2+CO,每消耗1 molCH4转移12 mol电子
3H2+CO,每消耗1 molCH4转移12 mol电子
B. 电极B上发生的电极反应:O2+2CO2+4e-=2CO32-
C. 电池工作时,CO32-向电极B移动
D. 电极A上H2参与的电极反应:H2+2OH--2e-=2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com