
等电子体之间具有相似的结构和化学键类型。根据等电子原理,由短周期元素组成的粒子,只要其原子总数和原子最外层电子总数相同,均可互称为等电子体.下列各组粒子不能互称为等电子体的是
A.CO32-和NO3- B.O3和SO2
C.CO2和NO2- D.SCN-和N3-
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:2016-2017学年浙江省温州市十校联合体高二上期末化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.O2,O3都是氧元素所形成的单质,互为同素异形体
B.乙酸(CH3COOH)和乙二酸(HOOC-COOH)互为同系物
C.CH3CH2CH2CH2CH3和CH3CH2CH(CH3)CH3互为同分异构体
D.CH3CH(CH3)CH3的名称是异丁烷
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省等名校高二上期末化学卷(解析版) 题型:填空题
一种甲醇燃料电池以稀硫酸为电解液,其中一个电极上加入甲醇(CH3OH),同时另一个电极通入空气:
(1)此电池的负极反应式是__________;
(2)正极电极反应式是___________;
(3)电解液中的H+向___________极移动。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高二上学期期末化学试卷(解析版) 题型:计算题
现有反应:CO(g)+ H2O(g)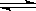 CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
CO2(g)+ H2(g) △H﹤0,在850℃时,平衡常数K=1。现在850℃时,向2L的密闭容器中充入CO、H2O(g)各4mol,试回答下列问题(写出具体的计算过程):
(1)达平衡时,CO转化率为多少?
(2)H2的体积分数为多少?
(3)若温度仍为850℃,初始时CO浓度为2mol/L,H2O(g)为6mol/L,则平衡时CO转化率为多少?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高二上学期期末化学试卷(解析版) 题型:选择题
下列关于平衡常数K的说法中,正确的是
A.在任何条件下,化学平衡常数是一个恒定值
B.改变反应物浓度或生成物浓度都会改变平衡常数K
C.平衡常数K只与温度有关,与反应浓度、压强无关
D.从平衡常数K的大小不能推断一个反应进行的程度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高二上学期期末化学试卷(解析版) 题型:选择题
下列晶体中,化学键种类相同,晶体类型也相同的是
A.SO2与SiO2 B.CO2与H2O C.NaCl与HCl D.CCl4与KCl
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省简阳市高二上学期期末化学试卷(解析版) 题型:填空题
今年入冬以来,简阳的雾霾较为严重,NO是引起原因之一。综合治理空气污染是环境化学当前主要研究的内容。
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可转化为N2(g)和CO2(g)得到净化。
①已知 2NO(g)+2CO(g) N2(g)+2CO2(g)反应能自发进行,则该为___________反应(填“吸热”或“放热”)。
N2(g)+2CO2(g)反应能自发进行,则该为___________反应(填“吸热”或“放热”)。
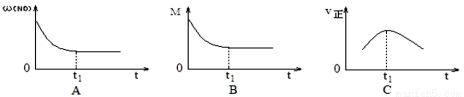
②上述反应在绝热、恒容密闭容器中进行,并在 t1时可达到平衡(图中 ω、M、v 正分别表示质量分数、混合气体平均相对分子质量和正反应速率),则下列示意图中符合题意的是___________(填选项序号)。
(2)在25℃、101kPa下,将2 mol NO、2.4 mol CO通入固定容积为2 L的密闭容器中,反应过程中部分物质的浓度变化如图所示。

①NO的转化率为 ,0~15min 内,v(NO) = 。
②20min 时若改变反应条件,导致CO浓度下降,则改变的条件可能是 (填选项序号)。
a.升高温度 b.增加CO的量 c.降低温度 d.扩大容器体积
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省简阳市高二上学期期末化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A. 增大反应物浓度可以增大活化分子百分数,从而使反应速率增大
B. Li、Be、B三种元素的第一电离能(I1)差别不大,而I2差别很大,则三种原子中最难失去第二个电子的是Be
C. 液氯溶于水后能导电,因此液氯是电解质
D. 固体NH5的所有原子的最外层均满足2个或8个电子的稳定结构,它与水反应的化学方程式为NH5+H2O═NH3•H2O+H2↑
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上摸底考试四化学卷(解析版) 题型:填空题
我国铜矿资源分布广泛,已探明储量居世界第三位。铜元素常见价态为+1,+2。大多数+1价铜的化合物是难溶物,如:CuCl、Cu2O等。+1价铜在酸性条件下易发生反应:2Cu+= Cu2++Cu。
(1)CuCl通常用作催化剂、杀菌剂、媒染剂、脱色剂。某实验兴趣小组模拟制备CuCl。
方法一:在CuCl2溶液中逐滴加入KI溶液可能发生:2Cu2++2Cl-+2I-=2CuCl↓(白色)+I2,为顺利观察到白色沉淀可以加入的最佳试剂是 。
A.SO2 B.苯 C.NaOH溶液 D.乙醇
方法二:将Na2SO3溶液逐滴加入CuCl2溶液中再加入少量的浓盐酸混匀,倾出清液,过滤出沉淀,沉淀用无水乙醇多次洗涤,得白色粉末状固体。
①沉淀的过滤和洗涤均用到的玻璃仪器有 ;
②洗涤CuCl沉淀的操作为 。
(2)纳米级Cu2O具有特殊的光学、电学及光电化学性质,研究制备纳米氧化亚铜的方法成为当前的研究热点之一。
方法一:在新制Cu(OH)2浊液中滴入N2H4•H2O水溶液,蓝色沉淀逐渐转化为砖红色,同时产生无色无味的气体。写出上述制备过程中的化学反应方程式 ;
方法二:以铜作阳极,石墨作阴极,电解含有NaOH的NaCl水溶液。
已知:该电解过程中阳极先生成难溶物CuCl,再与NaOH反应转化为Cu2O。
①写出阳极的电极反应式 ;
②电解后溶液中c(OH-)会 (填“变大”、“变小”或“不变”);
③若电解电路中通过0.2 mol电子,理论上生成Cu2O的质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com