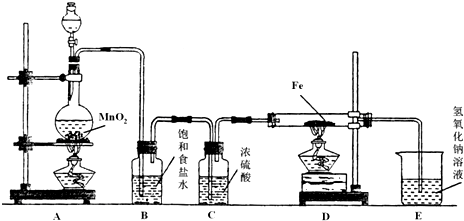
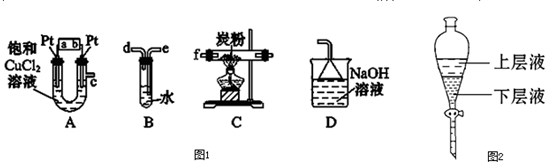
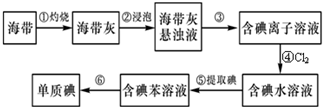
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素碳与硅的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润的红色试纸.已知常温下浓盐酸与高锰酸钾能反应生成氯气.
根据图1回答:
(1)写出选用物质的名称:A
硝酸
硝酸
,B
碳酸钙
碳酸钙
C
硅酸钠溶液
硅酸钠溶液
;
(2)烧瓶中反应的离子方程式为
CaCO3+2H+=Ca2++CO2+H2O
CaCO3+2H+=Ca2++CO2+H2O
;
烧杯中反应的离子方程式为
SiO32-+CO2+H2O═H2SiO3↓+CO32-(CO2不足),或SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-(CO2过量)
SiO32-+CO2+H2O═H2SiO3↓+CO32-(CO2不足),或SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-(CO2过量)
;
根据图2回答:
(3)乙同学的实验原理是
强氧化剂生成弱氧化剂或活泼的非金属单质置换出较不活泼的非金属单质
强氧化剂生成弱氧化剂或活泼的非金属单质置换出较不活泼的非金属单质
;
(4)B处的实验现象是
湿润的淀粉KI试纸变蓝
湿润的淀粉KI试纸变蓝
;
(5)B处的反应的离子方程式:
2I-+Cl2?I2+2Cl-
2I-+Cl2?I2+2Cl-
.