
25℃,水的电离平衡:H2O H++OH- ΔH>0,下列叙述正确的是
H++OH- ΔH>0,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,c(H+)不变,pH不变
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源:2016-2017学年黑龙江省高二上学期期中化学试卷(解析版) 题型:选择题
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s) NH3(g)+HI(g)
NH3(g)+HI(g)
②2HI(g) H2(g)+I2(g)
H2(g)+I2(g)
达到平衡时,c(H2)=0.5 mol/L,c(HI)=4 mol/L,则此温度下反应①的平衡常数为( )
A.20 B.16 C.9 D.25
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:填空题
煤化工中常需研究不同温度下平衡常数、投料比等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数K随温度的变化如下表:
H2(g)+CO2(g)平衡常数K随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
回答下列问题
(1)该反应的平衡常数表达式K= ,△H 0(填“<”、“>”、“=”)
(2)已知在一定温度下,C(s)+CO2(g) 2CO(g)平衡常数K1
2CO(g)平衡常数K1
C(s)+H2O(g) H2(g)+CO(g)平衡常数K2,
H2(g)+CO(g)平衡常数K2,
则K、K1、K2,之间的关系是 。
(3)800℃时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时 间后反应达到平衡,此时CO的转化率为 ;若保持其他条件不变,向平衡体系中再通入0.10molCO和0.40mol CO2,此时v正 v逆 (填“>”、“=”或“<”).
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省邯郸市、永年二中高二上期中化学卷(解析版) 题型:选择题
已知;(NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9kJ·mol﹣1,下列说法中正确的是( )
A.该反应中熵变、焓变皆 大于0
大于0
B.该反应是吸热反应,因此一定不能自发进行
C.碳酸盐分解反应中熵增加,因此任何条件下所有碳酸盐分解一定自发进行
D.能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上期中化学试卷(解析版) 题型:选择题
在相同温度时,100mL0.01mol·L-1的醋酸溶液和与10mL 0.1mol•L-1的醋酸溶液相比较,下列数据中,前者大于后者的是
A.H+的物质的量 B.醋酸电离常数
C.中和时所需氢氧化钠溶液的量 D.醋酸的物质的量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上期中化学试卷(解析版) 题型:选择题
用某种仪器量一液体体积时,平视读数为V1mL,仰视读数为V2mL,俯视读数为V3mL,若V3>V1>V2,则所使用仪器可能是
A. 容量瓶 B. 量筒 C. 碱式滴定管 D. 以上仪器均可
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上期中化学试卷(解析版) 题型:选择题
氢气燃烧的热化学方程式,可用下列两种方程式表示:
①2H2(g)+O2(g)=2H2O(l)+Q1kJ
②H2(g)+1/2O2(g)=H2O(g)+Q2kJ
Q1与Q2的关系为
A .Q1= Q2 B.Q2 >Q1 C.Q1>2Q2 D.Q1<2Q2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上期中化学试卷(解析版) 题型:选择题
下列叙述一定正确的是( )
A.一定温度压强下,气体体积由其分子的大小决定
B.常温常压下,1mol CO和1mol CO2所占的体积相同
C.水的摩尔质量 与1mol水分子的
与1mol水分子的 质量相等
质量相等
D.0.5mol·L-1NaOH溶液中含有0.5mol Na+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高一上期中化学试卷(解析版) 题型:选择题
已知常温下,溶液中能发生如下反应:
①2R-+Z2=R2+2Z-
②16H++10Z-+2XO4- =2X2++5Z2+8H2O
=2X2++5Z2+8H2O
③2M2++R2=2M3++2R-。由此判断,下列说法中正确的是
A.Z2+2M2+=2M3++2Z-不可以进行
B.Z元素在①②反应中发生还原反应
C.各粒子还原性由强到弱的顺序是X2+>Z->R->M2+
D.各粒子氧化性由强到 弱的顺序是XO
弱的顺序是XO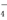 >Z2>R2>M3+
>Z2>R2>M3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com