
在恒温时,恒容的密闭容器内发生如下反应:2NO2(g) N2O4(g)达到平衡状态时,再向容器内通入一定量的NO2(g),重新达到平衡后,与原平衡相比,NO2的体积分数 ( )
N2O4(g)达到平衡状态时,再向容器内通入一定量的NO2(g),重新达到平衡后,与原平衡相比,NO2的体积分数 ( )
A. 不变 B.增大 C.减小 D.无法判断
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:2017届山东省高三上学期10月月考化学试卷(解析版) 题型:选择题
向含Al2(SO4)3和AlCl3的混合溶液中逐滴加人1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的物质的量的关系如图,下列说法不正确的是( )

A.图中C点铝元素存在形式是AlO2—
B.向D点溶液中通人C02气体,立即产生白色沉淀
C.原混合液中c[Al2(SO4)3]:c(AlCl3)=1:2
D.OA段反应的离子方程式为:3Ba2++2Al3++8OH-+3SO4=BaSO4↓+2AlO2-+4H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
已知H2(g)+Br2(g)=2HBr(g) △H=-102 kJ·mol-1,其它相关数据如下表:
H2(g) | Br2(g) | HBr(g) | ||
1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 | |
则表中a为
A.230 B.200 C.404 D.260
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
下列说法错误的是
 A.铁螺丝连接锌板时,铁不易生锈
A.铁螺丝连接锌板时,铁不易生锈
B.2NO(g)+2CO(g) N2(g)+2CO2(g)向正方向进行时,ΔS<0
N2(g)+2CO2(g)向正方向进行时,ΔS<0
C.单斜硫放出热量可转变成正交硫,由此可知正交硫更稳定
D.已知 ,则ΔH1+ΔH2=ΔH3
,则ΔH1+ΔH2=ΔH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:简答题
下图oa表示在密闭容器中反应:N2(g)+3H2(g) 2NH3(g)△H<0达到平衡过程,由于条件改变引起反应速度和化学平衡发生a~d的一系列变化,a b过程中改变的条件可能是 ;b c过程中改变的条件可能是 ;若增大压强时,将反应速度变化情况画在c~d处。(注意:画在图中,无图不给分)
2NH3(g)△H<0达到平衡过程,由于条件改变引起反应速度和化学平衡发生a~d的一系列变化,a b过程中改变的条件可能是 ;b c过程中改变的条件可能是 ;若增大压强时,将反应速度变化情况画在c~d处。(注意:画在图中,无图不给分)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:选择题
四位同学同时进行反应:A(g)+3B(g)=2C(g)+2D(g) 速率测定实验,分别测得反应速率如下:
①v(A)=1.5mol/(L·min);②v(B)=0.6mol/(L·s)
③v(C)=0.4mol/(L·s);④v(D)=0.45mol/(L·s)。
其中,反应进行得最快的是 ( )
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:选择题
下列热化学方程式中,表示燃烧热的热化学方程式的是( )
A. ═
═

B. ═
═

C. ═2CO2(g)+2H2O(l)
═2CO2(g)+2H2O(l) 
D. ═
═

查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市岐山县高三上期中化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的数值,下列说法正确的是
A.标准状况下,22.4LCCl4含有NA个分子
B.0.1molAlCl3完全转化为氢氧化铝胶体,生成0.l NA个胶体粒子
C.常温常压下46gNO2和N2O4混合气体含有3NA个原子
D.0.1molCl2与足量NaOH溶液反应,转移电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宣城市等四校高二上期中化学卷(解析版) 题型:填空题
合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1
2NH3(g) ΔH=-92.4 kJ·mol-1
一种工业合成氨的简易流程图如下:
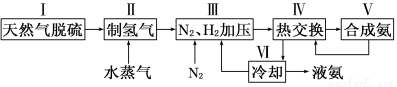
(1)在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:N2(g)+3H2(g) 2NH3(g)(正反应为放热反应)当反应达到平衡时,N2和H2的浓度比是 。升高平衡体系的温度(保持体积不变),该反应 (填“逆向移动”正向移动”或“不移动”) 。
2NH3(g)(正反应为放热反应)当反应达到平衡时,N2和H2的浓度比是 。升高平衡体系的温度(保持体积不变),该反应 (填“逆向移动”正向移动”或“不移动”) 。
(2)氨水、氯水中均存在多种微粒和多个平衡,请写出氯水中存在的一个化学平衡反应的离子方程式 。
(3)步骤Ⅱ中制氢气原理如下:
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4 kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的措施是___________。
a.升高温度 b.增大压强
c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若2 mol CO和H2的混合气体(H2的体积分数为80%)与H2O反应,得 到2.28mol CO、CO2和H2的混合气体,则CO转化率为_____________。
到2.28mol CO、CO2和H2的混合气体,则CO转化率为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com