
| A、pH=7 |
| B、c(H+)=c(OH-) |
| C、c(H+)=c(OH-)=10-7mol?L-1 |
| D、c(H+)?c(OH-)=1×10-14 |


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
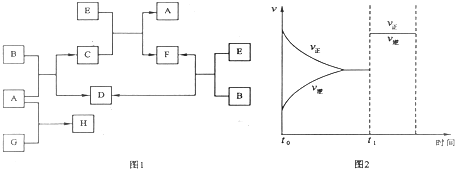
| 1 |
| 9 |
| 3 |
| 10 |
| 2 |
| 9 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2,6,3,5 |
| B、3,2,1,2 |
| C、1,3,2,2 |
| D、3,1,2,2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、普通玻璃呈淡绿色是由于含Fe2+ |
| B、坩埚、蒸发皿都属于陶瓷制品 |
| C、唐“三彩”是一种玻璃制品 |
| D、高温下硅酸钙比碳酸钙稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、高温、高压 |
| B、高温、低压 |
| C、低温、低压 |
| D、适当温度、高压 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、砷元素的相对原子质量为74.92,由此可知砷原子核内有62个中子 |
| B、在AsCl3分子中,砷原子最外层满足8个电子稳定结构 |
| C、砷的氢化物化学式为AsH3,它是一种强氧化剂 |
| D、砷酸(H3AsO4)是强酸,其酸性与硫酸相仿 |
查看答案和解析>>
科目:高中化学 来源: 题型:
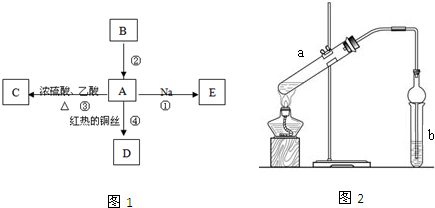
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com