
| A. | Na+、Mg2+、Al3+、Cl- | B. | Na+、AlO2-、Cl-、OH- | ||
| C. | Na+、Mg2+、Al2O-、Cl- | D. | Na+、Al3+、Al2O-、Cl- |
科目:高中化学 来源: 题型:解答题
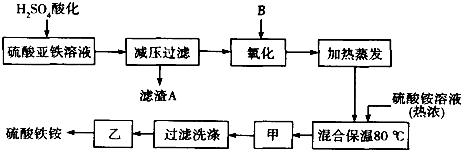
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )
如图表示的是A、B、C三种溶液两两混合发生反应的实验现象,符合该实验现象的A、B、C三种溶液依次是( )| A. | 盐酸、碳酸钠溶液、氢氧化钠溶液 | |
| B. | 氯化钠溶液、澄清石灰水、氢氧化钠溶液 | |
| C. | 盐酸、碳酸钠溶液、澄清石灰水 | |
| D. | 氢氧化钙溶液、盐酸、硫酸钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中只存在离子键 | |
| B. | 非金属元素组成的化合物中可能存在离子键 | |
| C. | 由不同种元素组成的多原子分子里,一定只存在极性共价键 | |
| D. | 含金属元素的化合物中一定存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 醋酸浓度/mol•L-1 | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
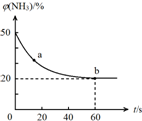 合理应用和处理氮的化合物,在生产生活中有重要意义.
合理应用和处理氮的化合物,在生产生活中有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com