
下列关于常见有机物的说法正确的是
A.乙醚和乙醇互为同分异构体
B.糖类、油脂、蛋白质均能发生水解反应
C.聚氯乙烯可用作生产食品包装材料的原料
D.分子式为C3H8O的有机物,只有2种能发生酯化反应
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源:2017届广东省深圳市三校高三上学期第一次联考化学卷(解析版) 题型:推断题
A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。

已知:H为两性氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
⑴A、B、C、D、E、F六种物质中所含的同一种元素的是 。
⑵写出反应①的化学 方程式: 。
方程式: 。
⑶写出反应③的离子方程式: 。
⑷反应⑥过程中的现象是: 。
查看答案和解析>>
科目:高中化学 来源:2017届广东省清远市清城区高三上期末B卷化学试卷(解析版) 题型:实验题
某氯化亚铁和氯化铁的混合物.现要测定其中铁元素的质量分数,按如图步骤进行实验:
请根据以上流程,回答下列问题:
(1)样品溶解过程中加入少量浓盐酸的目的是什么?
操作Ⅰ所用到的玻璃仪器除烧杯、玻璃棒外,还必须有哪些仪器?
操作Ⅱ中可用的玻璃仪器是什么仪器?
(2)请写出加入氨水发生的离子反应方程式。
(3)沉淀洗涤的方法是什么?
(4)将沉淀物灼烧,冷却到室温,用天平称量其质量为b1g,再次灼烧并冷却至室温称量其质量为b2g,若b1﹣b2=0.3g,则接下来还应进行的操作是 .若蒸发皿质量是W1g,蒸发皿与加热后固体总质量是W2g,则样品中铁元素的质量分数是 .
查看答案和解析>>
科目:高中化学 来源:2017届广东省清远市清城区高三上期末B卷化学试卷(解析版) 题型:选择题
把0.6molX、0.4molY混合后,在2L密闭容器中发生反应:3X(g)+Y(g)═nZ(g)+2W(g),5min末已生成0.2molW,并测得这段时间内v(Z)=0.01mol/(L•min).上述反应中Z的化学计量数n是( )
A.1 B.2 C.3 D.4
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三1月诊断性考试化学试卷(解析版) 题型:选择题
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是

A. a点溶液呈碱性的原因用离子方程式表示为:CO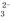 +2H2O
+2H2O H2CO3+2OH-
H2CO3+2OH-
B. c点处的溶液中c(Na+)-c(Cl-)=c(HCO )+2c(CO
)+2c(CO )
)
C. 滴定过程中使用甲基橙作为指示剂比酚酞更准确
D. d点处溶液中水电离出的c(H+)大于b点处
查看答案和解析>>
科目:高中化学 来源:2017届山东省潍坊市临朐县高三12月阶段测化学试卷(解析版) 题型:填空题
铜及其化合物在工农业生产及日常生活中应用非常广泛。
⑴由辉铜矿制取铜的反应过程为:
2Cu2S(s) + 3O2 (g) = 2Cu2O(s) + 2SO2(g) △H=-768.2kJ·mol- 1,
1,
2Cu2O(s) + Cu2S(s) = 6Cu(s) + SO2(g) △H=+116.0kJ·mol-1,
①写出Cu2S与O2生成 Cu(s) 和SO2的热化学方程式: 。
②获得的粗铜需电解精炼,精炼时粗铜作 极(选填:“阳”或“阴”)。
⑵氢化亚铜是一种红色固体,可由CuSO4溶液和H3PO2反应制备。该反应的化学方程式为 。该反应每转移3mol电子,生成CuH的物质的量为 。
⑶氯化铜溶液中含铜粒子的分布分数与c(Cl-) 的关系如图所示。①当c(Cl-)=9mol·L-1时,溶液中主要的3种含铜微粒浓度大小关系为 。
②在c(Cl-)=1mol·L-1的氯化铜溶液中,滴入AgNO3溶液,含铜微粒间转化的离子方程式为 (任写一个)。
查看答案和解析>>
科目:高中化学 来源:2017届山东省潍坊市临朐县高三12月阶段测化学试卷(解析版) 题型:选择题
短周期元素A、B、C、D的原子序数依次增大,A的最外层电子数是次外层电子数的2倍,B、D同主族且能形成两种常见的化合物,B、D质子数之和是C质子数的2倍。则下列说法中正确的是
A. 原子半径比较:A<B<C<D
B. A的氢化物沸点高于B的氢化物
C. D的氢化物比B的氢化物稳定性弱
D. 短周期所有元素中,C的最高价氧化物的水化物碱性最强
查看答案和解析>>
科目:高中化学 来源:2017届湖南省株洲市高三上教学质检一化学试卷(解析版) 题型:选择题
某温度下,将2molSO2和1molO2置于10L密闭容器中发生反应:2SO2(g)+O2(g)  2
2 SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
SO3(g);ΔH<0,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是

A.由图甲推断,B点SO2的平衡浓度为0.3 mol·L-1
B.由图甲推断,A点对应温度下该反应的平衡常数为800(L·mol-1)
C.达平衡后,若增大容器容积,则反应速率变化图像可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
查看答案和解析>>
科目:高中化学 来源:2017届湖北省荆门市高三元月调考理综化学试卷(解析版) 题型:实验题
某学习小组为研究碳素钢的性质,用铁钉(碳素钢)进行了以下探究活动:
[探究一](1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是______________________。
(2)称取碳素钢6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用_______(选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液
C.浓氨水 D.酸性KMnO4溶液
②乙同学取560 mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O===2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66 g。由此推知气体Y中SO2的体积分数为________。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中还可能含有Q1 和Q2两种气体,其中Q1气体,在标准状况下,密度为0.0893 g·L-1。为此设计了下列探究实验装置(假设有关气体完全反应)。

(3)装置B中试剂的作用是______________________。
(4)分析Y气体中的Q2气体是如何生成的 (用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加洗气瓶M于________(填序号)。
A.A之前 B.A—B间 C.B—C间 D.C—D间
(6)如果气体Y中含有Q1,预计实验现象应是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com