
 ��֪CO2����������ɫȼ�ϼ״���
��֪CO2����������ɫȼ�ϼ״���| 0.18mol/L |
| 10h |
| c(CH3OH)��c(H2O) |
| c(CO2)��c3(H2) |
| 0.20mol/L��0.20mol/L |
| 0.80mol/L��(1.0mol/L)3 |


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
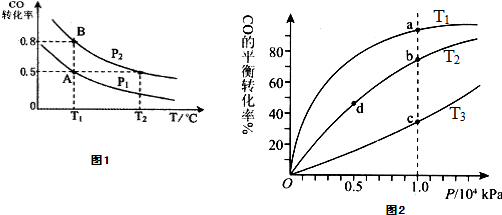
��Ŀ�����л�ѧ ��Դ���㽭ʡ��Ҧ��ѧ2011��2012ѧ��߶���ѧ�ڵ�һ���ʼ컯ѧ����(ʵ���) ���ͣ�022
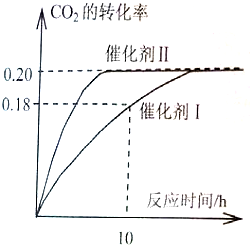
��֪CO2����������ɫȼ�ϼ״���CO2(g)��3H2(G)![]() CH3OH(g)��H2O(g)����H����187.4 kJ��mol��1��300��ʱ���ܱ������У���C(CO2)��1.00 mol��L��1C(H2)��1.60 mol��L��1��ʼ��Ӧ���������ͼ��ʾ���ش��������⣺
CH3OH(g)��H2O(g)����H����187.4 kJ��mol��1��300��ʱ���ܱ������У���C(CO2)��1.00 mol��L��1C(H2)��1.60 mol��L��1��ʼ��Ӧ���������ͼ��ʾ���ش��������⣺
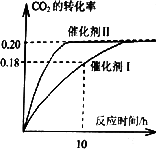
(1)ʹ�ô�����ʱ����Ӧ��10Сʱ�ڵ�ƽ����Ӧ���ʣ�V(H2)��________mol��(L��h)��1��
(2)����������ȷ����________��
A
��������������ܶȲ��ٸı�ʱ����Ӧ��һ���ﵽƽ��״̬B�������������ѹǿ���������{CO2��ת����
C
��CO2ƽ��ת���ʣ���������Ӧ�����£�������ȴ������D
����Ч�ʣ���������Ӧ�����£�������ȴ������(3)������ƽ����ϵ������400�棬ƽ�ⳣ����K(400��)________K(300��)(�������)��
(4)��֪��2H2(g)��O2(g)��2H2O(g)����H����242.8 kJ��mol��1��Ӧ2CH3OH(g)��3O2(g)��2CO2(g)��4H2O(g)����H��________kJ��mol��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��㶫ʡ�������и߶���ѧ����ĩ�������ƻ�ѧ�Ծ����������� ���ͣ������
��֪CO2����������ɫȼ�ϼ״���CO2(g) �� 3H2(g) CH3OH(g) + H2O(g) ��H����187.4 kJ/mol��3000Cʱ�ĺ����ܱ������У���C(CO2) = 1.00 mol.L-1 C(H2) =" 1.60" mol.L-1��ʼ��Ӧ���������ͼ��ʾ���ش��������⣺
CH3OH(g) + H2O(g) ��H����187.4 kJ/mol��3000Cʱ�ĺ����ܱ������У���C(CO2) = 1.00 mol.L-1 C(H2) =" 1.60" mol.L-1��ʼ��Ӧ���������ͼ��ʾ���ش��������⣺
(1)ʹ�ô���Iʱ����Ӧ��10Сʱ�ڵ�ƽ����Ӧ���ʣ�V(H2)= ______mol.(L.h)-1��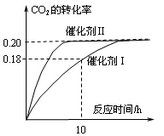
(2)����������ȷ����______����˫ѡ��
A.��������������ܶȲ��ٸı�ʱ����Ӧ��һ���ﵽƽ��״̬
B.�����������ѹǿ���������{CO2��ת����
C.CO2ƽ��ת���ʣ���������Ӧ�����£�����II�ȴ���I��
D.��Ч�ʣ���������Ӧ�����£�����II�ȴ���I��
(3)���ͼ�����ݣ�����˷�Ӧ��3000Cʱ��ƽ�ⳣ������д��������̣�
(4)������ƽ����ϵ������400��C, ƽ�ⳣ����K(4000C) ______ K(3000C) (��<��=��> )��
(5)�����������䣬��������Ӧ�ڴ�����400��C�´ﵽƽ�⣬������ͼ����CO2ת������ʱ��仯ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��㶫ʡ�߶���ѧ����ĩ�������ƻ�ѧ�Ծ��������棩 ���ͣ������
��֪CO2����������ɫȼ�ϼ״���CO2(g) �� 3H2(g) CH3OH(g) + H2O(g)
��H����187.4 kJ/mol��3000Cʱ�ĺ����ܱ������У���C(CO2) = 1.00 mol.L-1 C(H2)
=" 1.60" mol.L-1��ʼ��Ӧ���������ͼ��ʾ���ش��������⣺
CH3OH(g) + H2O(g)
��H����187.4 kJ/mol��3000Cʱ�ĺ����ܱ������У���C(CO2) = 1.00 mol.L-1 C(H2)
=" 1.60" mol.L-1��ʼ��Ӧ���������ͼ��ʾ���ش��������⣺
(1)ʹ�ô���Iʱ����Ӧ��10Сʱ�ڵ�ƽ����Ӧ���ʣ�V(H2)= ______mol.(L.h)-1��
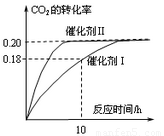
(2)����������ȷ����______����˫ѡ��
A.��������������ܶȲ��ٸı�ʱ����Ӧ��һ���ﵽƽ��״̬
B.�����������ѹǿ���������{CO2��ת����
C.CO2ƽ��ת���ʣ���������Ӧ�����£�����II�ȴ���I��
D.��Ч�ʣ���������Ӧ�����£�����II�ȴ���I��
(3)���ͼ�����ݣ�����˷�Ӧ��3000Cʱ��ƽ�ⳣ������д��������̣�
(4)������ƽ����ϵ������400��C, ƽ�ⳣ����K(4000C) ______ K(3000C) (��<��=��> )��
(5)�����������䣬��������Ӧ�ڴ�����400��C�´ﵽƽ�⣬������ͼ����CO2ת������ʱ��仯ͼ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com