平衡指的是两个相反方向的变化最后所处的运动状态;在平衡时,两种变化仍在继续进行,但是它们的速率相等;根据变化的性质可分为物理平衡和化学平衡,中学阶段涉及的平衡有可逆反应的平衡、酸碱电离平衡、水解平衡及沉淀-溶解平衡等等.
(1)现有容积为1L的恒温恒容密闭容器,向其中加入2mol A气体和2mol B气体后发生如下反应:A(g)+B(g)?C(g)△H=“-“a kJ?mol
-1,20s后,反应达到平衡状态,生成1mol C气体,放出热量Q
1kJ.回答下列问题.
①计算20s内B气体的平均化学反应速率为
.
②保持容器温度和容积不变,若改为向其中加入1molC气体,反应达到平衡时,吸收热量Q
2kJ,则Q
1与Q
2的相互关系正确的是
(填字母).
(A)Q
1+Q
2=a (B) Q
1+2Q
2<2a (C)Q
1+2Q
2>2a (D)Q
1+Q
2<a
③在原平衡基础上,保持容器温度和容积不变,向容器中再通入bmolA气体(b>0)时,v(正)
v(逆)(填“>”、“<”或“=”),重新达平衡后,C气体的平衡体积分数φ(C)=
,则b=
.
(2)常温下,将VmL、0.1000mol?L
-1氢氧化钠溶液逐滴加入到20.00mL、0.1000mol?L
-1醋酸溶液中,充分反应.回答下列问题.(忽略溶液体积的变化)
①如果溶液pH=7,此时V的取值
20.00(填“>”、“<”或“=”),而溶液中c(Na
+)、c(CH
3COO
-)、c(H
+)、c(OH
-)的大小关系为
.
②如果V=40.00,则此时溶液中c(OH
-)-c(H
+)-c(CH
3COOH)=
mol?L
-1.
(3)①某温度(t℃)时,测得0.01mol?L
-1的NaOH溶液的pH=11.在此温度下,将pH=2的H
2SO
4溶液V
aL与pH=12的NaOH溶液V
bL混合,若所得混合液为中性,则V
a:V
b=
.
②在25℃时,将cmol?L
-1的醋酸溶液与0.02mol?L
-1NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH
3COOH的电离常数K
a=
.
(4)与水的离子积Kw=C(H+)?C(OH-)相似,CuS饱和溶液中也有离了积KSP=C(Cu2+)?C(S2-).
已知t℃时CuS的离子积KSP=9.0×10
-36,又已知t℃时H2S饱和溶液中C(H+)2?C(S2-)=1.0×10-22,
①写出CuS沉淀溶解平衡的表达式
②现将适量CuS放入H2S饱和溶液中,要使C(Cu2+)达到0.01mol?L-1时,应使该溶液的C(H+)达到
.由此说明CuS在一般酸中
溶解.(填“能”或“不能”)
③PbSO
4难溶于水却可溶于醋酸溶液,你认为可能的原因是
A.醋酸铅可溶于水 B.醋酸铅是弱电解质
C.醋酸铅在水中形成电离平衡时的c(Pb
2+)小于PbSO
4的溶解平衡的c(Pb
2+)
D.因醋酸是弱酸,故反应可进行.

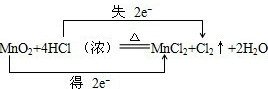 ,故答案为:
,故答案为: .
.


 和
和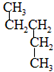
 和
和 ⑦CH3CH2CH2CH3和
⑦CH3CH2CH2CH3和